扩展功能
文章信息
- 姜杰, 冯旗, 贺鹏宸, 彭兆丰
- JIANG Jie, FENG Qi, HE Pengchen, PENG Zhaofeng
- 微生物种间直接电子传递机理及应用研究进展
- Mechanism and application of direct interspecies electron transfer
- 微生物学通报, 2023, 50(10): 4694-4704
- Microbiology China, 2023, 50(10): 4694-4704
- DOI: 10.13344/j.microbiol.china.230171
-
文章历史
- 收稿日期: 2023-03-06
- 接受日期: 2023-05-18
- 网络首发日期: 2023-07-13
微生物代谢策略之一是基于电子转移的氧化还原过程,细胞外电子转移有助于微生物的能量代谢。由于各种电子受体和供体为微生物提供了不同的能量来源,导致了微生物能量代谢方式与途径不同[1-2]。微生物可通过一系列氧化还原蛋白、电子介体或“纳米导线”将胞内产生的电子转移到胞外电子受体或将电子由胞外电子供体传递至胞内而获得能量的过程称为微生物的胞外电子传递(extracellular electron transfer, EET)[3]。
微生物与矿物间的电子传递过程是一种古老的生物地球化学过程,在漫长的地质演化过程中起着至关重要的作用。由微生物EET途径介导的胞外电子受体—微生物界面的电子传递过程,可将细胞内反应与细胞外不溶性氧化剂或还原剂(包括电极)连接起来,以获得矿物中丰富的氧化还原活性呼吸电子受体和供体(如S、Fe和Mn等),此现象不但可以促使矿物进行水解、沉降和能量转移等各种物理化学反应,同时也对微生物的繁殖、新陈代谢与协同功能起着至关重要的影响[4-6]。经研究确认的具有胞外电子传递功能的微生物种群已被广泛应用于各个领域:(1) 具有电活性微生物将有机物氧化产生的电子通过EET途径传递到电极上时化学能可被转化成电能,为发电提供新的思路;(2) 通过微生物群落协同互作对有机废物氧化进行废水处理;(3) 环境中有毒重金属污染物(铀)可被转化为溶解度更低、毒性较小的形式,实现污染物的固定,进行生物修复;(4) 厌氧消化生产生物燃料如甲烷等[7-9]。因此,探究微生物胞外电子传递的分子机制对生物修复、生物采矿、生物燃料和纳米材料的生产等生物技术应用具有重大的科学意义。
几乎所有的生物都依赖其他物种而生存,这种合作关系在所有的生命领域都是必不可少的,尤其是在微生物之间更加突出。两种微生物分别提供电子供体与电子受体,其间传递电子可形成互利共生的关系,因此可共同完成某一方微生物不能单独完成的代谢过程,将这一现象称之为微生物种间电子传递(interspecies electron transfer, IET)。IET主要分以下2种:(1) 间接种间电子传递(mediated interspecies electron transfer, MIET)。(2) 种间直接电子传递(direct interspecies electron transfer, DIET)。间接种间电子传递指微生物利用一些氧化还原物质(由微生物自身代谢产生或外部条件供给的)实现胞外电子传递。种间直接电子传递是指微生物通过纳米导线或c型细胞色素等导电介质实现与另外一种微生物发生电子直接交换的过程。以前的研究一直认为氢气(H2)和甲酸(HCOOH)[10-11]是微生物胞外电子传递的中间电子传递体,但2010年Summers等首次研究发现金属还原地杆菌(Geobacter metallireducens) GS-15和硫还原地杆菌(Geobacter sulfurreducens) PCA可通过纳米导线建立以DIET途径为主导的共培养并形成紧密的团聚体[12],这表明微生物间可以通过种间直接电子传导替代以H2或HCOOH为穿梭介质实现电子传递。
DIET作为一种新型的微生物IET途径,与MIET使用代谢中间产物(如H2/甲酸)来运送电子相比,DIET通过传导途径直接传递由外源性(捐献电子)微生物产生的电子到亲电(电子接收)微生物[13],使DIET在热力学上更有利[14],电子转移率比MIET高[15],因此在不形成或消耗中间物的情况下更节能。DIET为深入认识微生物之间的互营共生提供了新视角。
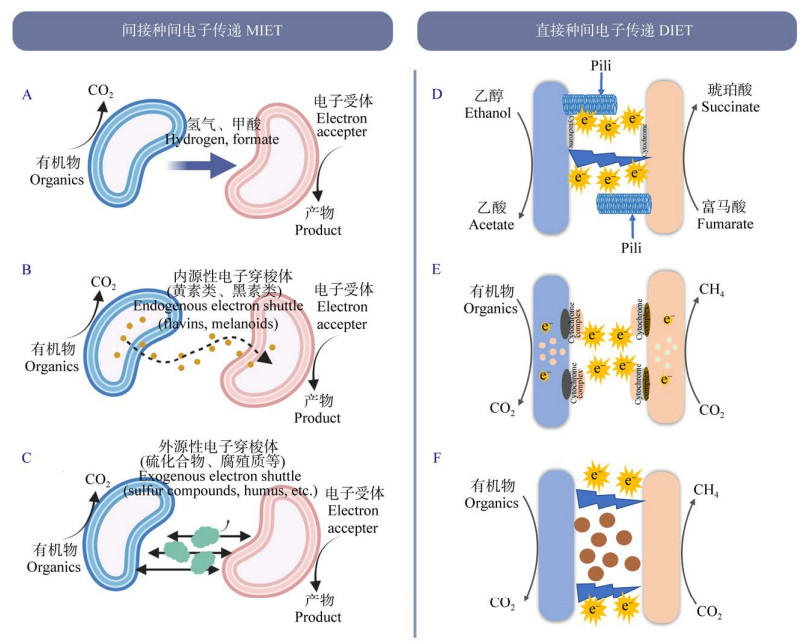
1 微生物种间电子传递分类 1.1 间接种间电子传递(MIET)研究得最透彻的微生物种间合作类型之一是氢气(H2)作为电子载体实现种间电子转移,电子供体微生物将质子还原为氢气,受体微生物再将氢气氧化捕获电子实现电子传递获得能量[16]。同样地,微生物也可通过甲酸(HCOOH)等作为电子载体实现电子转移[17-19]。例如,已有研究[20]发现沃氏共养单胞菌(Syntrophomonas wolfei)和嗜酸共养菌(Syntrophus aciditrophicus)两种微生物(都含有多种氢化酶和甲酸盐脱氢酶基因,但缺失外膜细胞色素和形成纳米导线的基因)能代谢底物产生氢气或甲酸实现电子转移(图 1A)。
|
| 图 1 微生物种间电子传递模式图 Figure 1 Diagram of the electron transfer mode between microbial species. A:H2/HCOOH介导的MIET. B:内源性电子穿梭体介导的MIET. C:外源性电子穿梭体介导的MIET. D:菌毛介导的DIET. E:外膜细胞色素介导的DIET. F:导电材料介导的DIET A: H2/HCOOH mediated MIET. B: Endogenous electron shuttle-mediated MIET. C: Exogenous electron shuttle-mediated MIET. D: Pili mediated DIET. E: Extracellular cytochrome mediated DIET. F: A conductive material mediated DIET. |
|
|
微生物也可通过具有氧化还原活性的电子穿梭体实现种间电子传递。它们可通过自身分泌的具有氧化还原活性的有机小分子(即内源性电子穿梭体)或外源存在的电子介体物质(即外源性电子穿梭体)进行电子传递。内源性电子穿梭体是由微生物自身产生具有氧化还原活性代谢物,一般是微生物的次级代谢产物,如黄素类[21]、黑素类[22]等(图 1B)。对于那些利用胞外电子受体进行呼吸并获取能量的微生物而言,内源性电子穿梭体的产生具有一定优势。外源电子穿梭体是一类由人工合成或天然存在具有氧化还原的物质。例如,硫化合物[23-24]、腐殖质[25-26]、生物炭[27]和氧化铁[28]等(图 1C)。不同的电子穿梭体,由于其氧化还原的特性不同,为种间的电子转移提供了多种可能性。外源性电子穿梭体广泛存在于自然界,可直接介导与驱动厌氧条件下微生物胞外电子传递过程,原则上,单个穿梭分子可以循环数千次,添加外源电子穿梭体可以在微生物能量代谢中开辟新的电子通道,因此这类电子穿梭体的发现和利用为微生物产电以及污染物的迁移转化产生了广泛的应用前景[29],同时为微生物在生物技术过程中的应用开辟了新的可能性。
1.2 种间直接电子传递(DIET)前人研究普遍认为微生物间合成代谢涉及代谢物转移,但在G. metallireducens和G. sulfurreducens的共培养中率先发现了DIET,G. metallireducens不能还原富马酸盐但可以利用乙醇作为电子供体,G. sulfurreducens可以利用富马酸盐作为电子受体但不能氧化乙醇,当它们同时接种在以乙醇为唯一电子供体培养基中时可形成直接电连接的合作关系。同时在共培养物中发现了被称为纳米导线的导电纤毛[30-31],编码导电菌毛的基因pilA和编码外膜c型细胞色素基因omcS被敲除后,G. sulfurreducens与G. metallireducens间难以建立共培养。但编码氢酶基因hybL的缺失并未影响以乙醇为唯一电子受体的共培养物生长。这说明微生物间合成代谢可能是通过直接电子转移而不是氢和/或甲酸盐介导的。
微生物可通过这种独特的细胞间电子转移机制使有机物的氧化过程突破热力学障碍直接依赖其导电性自发进行,从而不需要其他氧化还原类物质介导,并且由于电流介导的种间直接电子传递效率高于由中间产物介导的电子传递速率,因此DIET作为一种新型电子传递途径其传递效率和能量利用率更高。
DIET的发现对厌氧降解等重要生物地球化学过程及生态修复等研究有着极其重要的理论意义[28]。在自然生态环境中广泛存在直接的种间电子转移,包括废水聚集物的产甲烷[32]、海洋沉积物中的好氧硫化物氧化[33]和光合细菌直接电接收将光能转化为化学能[34],这些反应通过DIET介导可以彼此相隔数厘米来完成[35]。
2 DIET机理 2.1 可进行DIET的微生物能形成电连接微生物群落主要限于少数厌氧环境,因此与DIET相关的微生物主要以厌氧菌为主(表 1),其中隶属于地杆菌(Geobacter spp.)的G. metallireducens与G. sulfurreducens是最早发现能进行DIET的菌株。在处理啤酒厂废水的上流式厌氧污泥毯(upflow anaerobic sludge blanket, UASB)反应器中,首次发现了联合甲烷丝菌(Methanosaeta concilii)与Geobacter之间的DIET证据[36]。
DIET主要通过纳米导线(nanowires)、细胞外膜表面c型细胞色素、导电材料[颗粒活性炭(granular activated carbon, GAC)、生物炭、石墨、磁铁纳米颗粒和碳基纳米材料]进行[36-40]。
2.2.1 纳米导线介导的DIET纳米导线在微生物的呼吸作用和种间电子交换的远距离细胞外电子转移中起着关键作用。目前,G. sulfurreducens被认为能产生两种类型的纳米导线,它们分别由导电菌毛(e-pili)蛋白[41]和胞外细胞色素蛋白[40]组成。
其中,e-pili是研究最深入的蛋白质纳米导线,它最初被认为是由Ⅳ型菌毛蛋白单体PilA-N组装而成。在π轨道重叠或电子脱域的作用下,e-pili可以作为电子导管输送电子[42](图 1D)。但在最新研究中,Wang等[42]通过高分辨率冷冻电镜观察Ⅳ型菌毛的原子结构,认为Ⅳ型菌毛实际上是聚合的细胞色素(其堆叠的血红素基团形成了连续的导电线)或者是细胞外的DNA。
2019、2020和2022年有研究者在G. sulfurreducens中分别发现了3种细胞色素纳米导线,并确定它们分别是由omcS、omcZ和omcE基因编码的c型细胞色素单体组成[43]。附着在电极表面的G. sulfurreducens高电导率生物膜中OmcS和OmcZ均有被诱导表达,与e-pili类似,OmcZ对于G. sulfurreducens生物膜的形成和电极上电流的产生具有至关重要的作用,敲除基因omcZ将极大地抑制G. sulfurreducens将电子传递至电极[44]。然而有研究者提出,OmcS对G. sulfurreducens的生物膜产生电流来说不是必要的,因为当基因omcS被敲除时其产电能力并未降低[45]。也有研究者提出,由于omcS与omcZ表达时的互补关系,在omcS敲除株的微生物燃料电池(microbial fuel cells, MFCs)试验中OmcS的作用可能被忽略了[41, 44]。近期有报道G. sulfurreducens的细胞外导电丝由c型细胞色素OmcE亚基组成,冷冻电子显微镜观察结果显示,尽管OmcE和OmcS亚基无总体序列或结构相似性,但聚合后两者都形成共享保守血红素堆积排列的细丝,其中血红素由相邻亚基中的组氨酸配位,与OmcS细丝不同,OmcE细丝是高度糖基化的[39, 45]。
已有研究表明地杆菌纳米导线-导电菌毛(e-pili)蛋白及OmcS细胞色素纳米导线蛋白参与DIET[12, 46],但由其他细胞色素(OmcZ、OmcE)组成的纳米导线是否参与DIET尚且未知。目前本实验室正致力于研究这一问题。
2.2.2 细胞色素介导的DIET在硫还原地杆菌和金属还原地杆菌共培养物中,已发现并证实细胞色素对于DIET是十分重要的,金属还原地杆菌的Gmet_2896细胞色素在DIET中起至关重要的作用,而导电菌毛对促进DIET并不重要,即使导电菌毛正常表达也不能弥补细胞色素OmcS或Gmet_2896细胞色素表达缺失,因此推测细胞色素本身可以促进DIET,细胞色素不仅可以在密切接触的物种之间介导DIET,而且可以在空间分离的物种之间介导DIET,电子可在细胞色素蛋白间跳跃完成DIET[46-47]。
在G. metallireducens与Methanosarcinales的DIET过程中,G. metallireducens同样需要传导性菌毛[48-49]和外膜c型细胞色素[49]进行胞外电子传递。而且在许多接受细胞外电子的自养生物中,电子摄取的过程通常涉及c型细胞色素[50]。因此,Methanosarcinales作为唯一具有c型细胞色素的产甲烷菌,预计也会类似地利用电子[51]。然而并非所有能够进行DIET的Methanosarcinales都在其基因组中过量表达c型细胞色素[52]。有研究发现Methanosarcina虽具有细胞色素Mma_0663,但在进行DIET或摄取电极的细胞外电子生长时该细胞色素并不发挥作用[52],预测Methanosarcinales可能使用了前所未有的电子摄取机制,而这些机制还需进一步探索(图 1E)。
2.2.3 导电材料介导的DIET由于2种微生物间的电子转移由导电菌毛或电子转移蛋白之间的直接接触发生,因此这种电子转移路径可以通过碳材料(如活性炭)或导电的金属材料与2个不同物种的细胞接触来实现。碳材料和磁铁矿是文献中研究最多的导电材料(图 1F)。
活性炭等碳材料的尺寸通常大于微生物的尺寸,因此,附在碳材料上的微生物可作为生物膜有利于电子输送[53]。例如,在G. metallireducens与Methanosarcinales的DIET过程中可通过添加活性炭促进电子转移[54]。Zhang等认为[55],碳基材料的存在可以增强微生物的活性和厌氧菌之间的电子传递,为微生物细胞提供有利的固定化基质。然而由于部分磁铁矿的尺寸比微生物小得多,因此磁铁矿纳米颗粒被聚集成导线进行细胞间链接或黏附在胞外纤毛上形成导电通路,从而加强电子传输[56-57]。
导电材料的应用可以通过调节DIET机制以促进厌氧消化(anaerobic digestion, AD)的性能。AD是最广泛采用的具有可再生能源生产的生物废物处理过程。添加Fe3O4等金属纳米颗粒对改善消化性能的影响已得到广泛研究,因此这一技术对可再生能源的生产具有十分重要的意义。
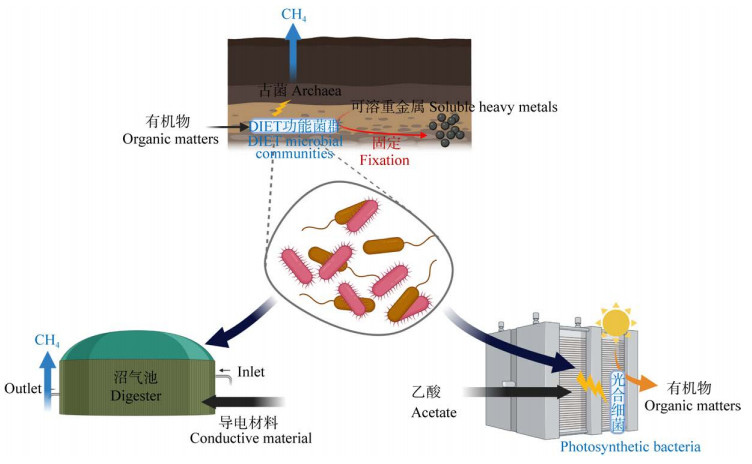
3 DIET的应用DIET的应用模型见图 2。
|
| 图 2 种间直接电子传递潜在应用模型图 Figure 2 Potential application model diagram of direct interspecies electron transfer. |
|
|
自然界中许多污染物的生物地球化学循环常常与铁元素生物地球化学循环耦合,异化铁还原菌(dissimilatory iron reducing bacteria, DIRB)是地层中广泛存在的具有EET功能的微生物,在氧化地下的有机污染物(如芳香烃)方面具有重要作用,也可以通过将污染物还原成难溶的低毒形式实现重金属污染的固定[58]。最近有研究表明,从Fe(Ⅲ)还原菌G. sulfurreducens中纯化出一种膜结合的还原型辅酶Ⅱ (nicotinamide adenine dinucleotide phosphate, NADPH)依赖性Fe(Ⅲ)还原酶[59-60],能将有毒的Cr(Ⅵ)还原成Cr(Ⅲ)[61]。在原位添加各种电子供体的条件下,可促进Geobacter spp.进行土壤Fe(Ⅲ)的还原,并将电子通过DIET传递给其他污染物降解功能菌群,从而推动其他污染物的迁移转化。
3.2 促进有机废物厌氧消化产生燃料40多年来,人们一直认为产甲烷环境中的微生物主要通过氢气的种间转移来交换电子,贡献电子的微生物通过将质子还原为氢气来处置电子,而电子接受的微生物则通过二氧化碳的还原来氧化氢气产甲烷[17]。然而现研究表明,DIET是微生物集合体将废物转化为甲烷的电子交换的主要机制[35]。许多研究[28, 32, 62]显示,在厌氧消化器中添加已知的促进DIET的材料,或在厌氧消化中代谢重要中间产物的产甲烷富集培养物,可以加速甲烷生产的速度并增加所产生气体的甲烷含量。在厌氧消化(anaerobic digestion, AD)中,把能介导生成甲烷反应的微生物称为产甲烷菌或产甲烷古菌[63]。产甲烷菌可以利用简单的有机底物如醋酸、CO2/H2、甲醇和甲酸盐。因此,产甲烷菌可与其他微生物建立合作关系,能以部分脂肪酸和醇类等为燃料生产甲烷[64]。然而通过添加电活性微生物和添加活性炭等廉价导电材料可促进DIET来提高甲烷产量实现AD性能优化。这种独特的细胞间电子传递机制在热力学和代谢上更具优势还原有机物以产甲烷[65],因此可加快转化有机废物到甲烷。
3.3 微生物电化学还原二氧化碳产能太阳辐射是最有前途的可持续能源,将光能转化为电能的光伏装置得到了广泛研究。微生物光养生物也被应用于使用专门反应器的光/电转换,称为微生物太阳能电池(microbial solar cell, MSC)[66]。许多研究表明,可以使用天然存在的微生物群落构建自我维持的MSC。为了更好地了解微生物群落中如何发生光/电转换,Nishio等[67]构建了一个由莱茵衣藻和G. sulfurreducens两种微生物组成的MSC模型,结果表明,光/电转换是通过光养生物和发电细菌之间的互营作用发生的。2017年,Ha等[68]首次证明了G. sulfurreducens和光养细菌(Prosthecochloris aestuarii)之间存在一种新形式的DIET,在这种共培养中,G. sulfurreducens氧化乙酸盐并直接向P. aestuarii提供电子,P. aestuarii在光照下而非黑暗中接受电子进行光合作用。基于这项研究,Huang等[69]于2019年构建由G. sulfurreducens和P. aestuarii组成的光合微生物燃料电池(photo-MFC),该photo-MFC的阳极和阴极隔室由质子交换膜隔开,并分别接种G. sulfurreducens和P. aestuarii,阳极和阴极通过带有外部电阻的金属丝电连接,在光照条件下,P. aestuarii接受来自G. sulfurreducens生物阳极的细胞外电子继而固定CO2,可产生的最大电流为0.6 mA/m2,同时证明了光合DIET可以由导电材料介导。该研究为DIET在微生物电化学固定二氧化碳产能方面的进一步应用提供了新的参考。
4 展望在微生物DIET中依然存在对某些关键过程及元素不清楚,如G. sulfurreducens与G. metallireducens、G. metallireducens和Methanosarcinales的DIET中是否有重要胞外细胞色素或跨膜细胞色素参与DIET过程还需进一步研究与探讨,目前本实验室正通过基因敲除方式研究这一问题。
深入地探究微生物种间电子传递机制可寻找更多的电连接的微生物群落,继而进一步推进其他方面的应用,如开发可持续的生物电子材料和生物电化学技术。其中,工程DIET是改善有机废物厌氧消化的一个新兴战略。共培养的研究探明了在简单有机废物中DIET有关的机制,而在复杂有机废物厌氧消化中的DIET方面还有很多代谢机制有待发现。在DIET中已经确定了不同的导电添加剂,使细菌和产甲烷菌之间能够进行基于DIET的合成,尽管这些导电添加剂的导电性和表面积在加速DIET动力学方面的意义尚无定论。因此,要想在厌氧消化中开发可持续的DIET工程策略,还需要在基础认识上有进一步发展。
| [1] |
PENG ZF, SHI MM, XIA KM, DONG YR, SHI L. Degradation of 2, 2′, 4, 4′-tetrabrominated diphenyl ether (BDE-47) via the Fenton reaction driven by the dissimilatory metal-reducing bacterium Shewanella oneidensis MR-1[J]. Environmental Pollution (Barking, Essex: 1987), 2020, 266(Pt 1): 115413. |
| [2] |
SHI MM, XIA KM, PENG ZF, JIANG YG, DONG YR, Shi L. Differential degradation of BDE-3 and BDE-209 by the Shewanella oneidensis MR-1-mediated Fenton reaction[J]. International Biodeterioration & Biodegradation, 2021, 158: 105165. |
| [3] |
QIU X, SHI L. Electrical interplay between microorganisms and iron-bearing minerals[J]. Acta Chimica Sinica, 2017, 75(6): 583-593. (in Chinese) 邱轩, 石良. 微生物和含铁矿物之间的电子交换[J]. 化学学报, 2017, 75(6): 583-593. |
| [4] |
PENG ZF, LIU ZY, JIANG YG, DONG YR, SHI L. In vivo interactions between Cyc2 and Rus as well as Rus and Cyc1 of Acidithiobacillus ferrooxidans during extracellular oxidization of ferrous iron[J]. International Biodeterioration & Biodegradation, 2022, 173: 105453. |
| [5] |
LIU J, LI XX, LIU F, ZHANG YX. Research advantages on molecular mechanisms of interfacial electron transfer between iron oxide and microbe[J]. Bulletin of Mineralogy, Petrology and Geochemistry, 2018, 37(1): 39-47, 159. (in Chinese) 刘娟, 李晓旭, 刘枫, 张逸潇. 铁氧化物-微生物界面电子传递的分子机制研究进展[J]. 矿物岩石地球化学通报, 2018, 37(1): 39-47, 159. DOI:10.19658/j.issn.1007-2802.2018.37.015 |
| [6] |
SHI L, DONG HL, REGUERA G, BEYENAL H, LU AH, LIU J, YU HQ, FREDRICKSON JK. Extracellular electron transfer mechanisms between microorganisms and minerals[J]. Nature Reviews Microbiology, 2016, 14(10): 651-662. DOI:10.1038/nrmicro.2016.93 |
| [7] |
VERMA J, KUMAR D, SINGH N, KATTI SS, SHAH YT. Electricigens and microbial fuel cells for bioremediation and bioenergy production: a review[J]. Environmental Chemistry Letters, 2021, 19(3): 2091-2126. DOI:10.1007/s10311-021-01199-7 |
| [8] |
JONATHAN R, LOVLRY DR. Microbial detoxification of metals and radionuclides[J]. Current Opinion in Biotechnology, 2001, 12(3): 248-253. DOI:10.1016/S0958-1669(00)00207-X |
| [9] |
BARUA S, DHAR B. Advances towards understanding and engineering direct interspecies electron transfer in anaerobic digestion[J]. Bioresource Technology, 2017, 244: 698-707. DOI:10.1016/j.biortech.2017.08.023 |
| [10] |
SIEBER JR, MCINERNEY MJ, GUNSALUS RP. Genomic insights into syntrophy: the paradigm for anaerobic metabolic cooperation[J]. Annual Review of Microbiology, 2012, 66: 429-452. DOI:10.1146/annurev-micro-090110-102844 |
| [11] |
JIANG HM, WANG LL, LI X. Advances in co-culture stoichiometrically producing methane via direct interspecies electron transfer within microbes[J]. Journal of Chemical Engineering of Chinese Universities, 2019, 33(6): 1303-1313. (in Chinese) 蒋海明, 王路路, 李侠. 微生物种间直接电子传递方式耦合产甲烷研究进展[J]. 高校化学工程学报, 2019, 33(6): 1303-1313. |
| [12] |
SUMMERS ZM, FOGARTY HE, LEANG C, FRANKS AE, MALVANKAR NS, LOVLEY DR. Direct exchange of electrons within aggregates of an evolved syntrophic coculture of anaerobic bacteria[J]. Science, 2010, 330(6009): 1413-1415. DOI:10.1126/science.1196526 |
| [13] |
ZHAO ZQ, LI Y, ZHANG YB, LOVLEY DR. Sparking anaerobic digestion: promoting direct interspecies electron transfer to enhance methane production[J]. iScience, 2020, 23(12): 101794. DOI:10.1016/j.isci.2020.101794 |
| [14] |
DANTAS JM, MORGADO L, AKLUJKAR M, BRUIX M, LONDER YY, SCHIFFER M, POKKULURI PR, SALGUEIRO CA. Rational engineering of Geobacter sulfurreducens electron transfer components: a foundation for building improved Geobacter-based bioelectrochemical technologies[J]. Frontiers in Microbiology, 2015, 6: 752. |
| [15] |
STORCK T, VIRDIS B, BATSTONE DJ. Modelling extracellular limitations for mediated versus direct interspecies electron transfer[J]. The ISME Journal, 2016, 10(3): 621-631. DOI:10.1038/ismej.2015.139 |
| [16] |
MCINERNEY MJ, SIEBER JR, GUNSALUS RP. Syntrophy in anaerobic global carbon cycles[J]. Current Opinion in Biotechnology, 2009, 20(6): 623-632. DOI:10.1016/j.copbio.2009.10.001 |
| [17] |
STAMS AJM, PLUGGE CM. Electron transfer in syntrophic communities of anaerobic bacteria and archaea[J]. Nature Reviews Microbiology, 2009, 7(8): 568-577. DOI:10.1038/nrmicro2166 |
| [18] |
MORRIS BEL, HENNEBERGER R, HUBER H, MOISSL-EICHINGER C. Microbial syntrophy: interaction for the common good[J]. FEMS Microbiology Reviews, 2013, 37(3): 384-406. DOI:10.1111/1574-6976.12019 |
| [19] |
LOVLEY DR, UEKI T, ZHANG T, MALVANKAR NS, SHRESTHA PM, FLANAGAN KA, AKLUJKAR M, BUTLER JE, GILOTEAUX L, ROTARU AE, HOLMES DE, FRANKS AE, ORELLANA R, RISSO C, NEVIN KP. Geobacter[M]// Advances in Microbial Physiology. Amsterdam: Elsevier, 2011: 1-100.
|
| [20] |
SIEBER JR, LE HM, McINERNEY MJ. The importance of hydrogen and formate transfer for syntrophic fatty, aromatic and alicyclic metabolism[J]. Environmental Microbiology, 2014, 16(1): 177-188. DOI:10.1111/1462-2920.12269 |
| [21] |
OKAMOTO A, NAKAMURA R, NEALSON KH, HASHIMOTO K. Bound flavin model suggests similar electron-transfer mechanisms in Shewanella and Geobacter[J]. ChemElectroChem, 2014, 1(11): 1808-1812. DOI:10.1002/celc.201402151 |
| [22] |
HERNANDEZ ME, KAPPLER A, NEWMAN DK. Phenazines and other redox-active antibiotics promote microbial mineral reduction[J]. Applied and Environmental Microbiology, 2004, 70(2): 921-928. DOI:10.1128/AEM.70.2.921-928.2004 |
| [23] |
FLYNN TM, O'LOUGHLIN EJ, MISHRA B, DICHRISTINA TJ, KEMNER KM. Sulfur-mediated electron shuttling during bacterial iron reduction[J]. Science, 2014, 344(6187): 1039-1042. DOI:10.1126/science.1252066 |
| [24] |
FRIEDRICH MW, FINSTER KW. How sulfur beats iron[J]. Science, 2014, 344(6187): 974-975. DOI:10.1126/science.1255442 |
| [25] |
LOVLEY DR, COATES JD, BLUNT-HARRIS EL, PHILLIPS EJP, WOODWARD JC. Humic substances as electron acceptors for microbial respiration[J]. Nature, 1996, 382(6590): 445-448. DOI:10.1038/382445a0 |
| [26] |
ZHENG Y, KAPPLER A, XIAO Y, YANG F, MAHADEVA GD, ZHAO F. Redox-active humics support interspecies syntrophy and shift microbial community[J]. Science China Technological Sciences, 2019, 62(10): 1695-1702. DOI:10.1007/s11431-018-9360-5 |
| [27] |
KAPPLER A, WUESTNER ML, RUECKER A, HARTER J, HALAMA M, BEHRENS S. Biochar as an electron shuttle between bacteria and Fe(Ⅲ) minerals[J]. Environmental Science & Technology Letters, 2014, 1(8): 339-344. |
| [28] |
KATO S, HASHIMOTO K, WATANABE K. Microbial interspecies electron transfer via electric currents through conductive minerals[J]. Proceedings of the National Academy of Sciences of the United States of America, 2012, 109(25): 10042-10046. |
| [29] |
ZHANG YL, CHEN XL, WU YD. Electron shuttle-mediated microbial extracellular electron transfer: mechanisms and geochemical implications[J]. Ecology and Environment Sciences, 2021, 30(1): 213-222. (in Chinese) 张玉龙, 陈雪丽, 吴云当. 电子穿梭体及其介导的环境与地球化学过程研究进展[J]. 生态环境学报, 2021, 30(1): 213-222. DOI:10.16258/j.cnki.1674-5906.2021.01.025 |
| [30] |
REGUERA G, MCCARTHY KD, MEHTA T, NICOLL JS, TUOMINEN MT, LOVLEY DR. Extracellular electron transfer via microbial nanowires[J]. Nature, 2005, 435(7045): 1098-1101. DOI:10.1038/nature03661 |
| [31] |
ZHAO Z, SUN C, LI Y, PENG H, ZHANG YB. Upgrading current method of anaerobic co-digestion of waste activated sludge for high-efficiency methanogenesis: establishing direct interspecies electron transfer via ethanol-type fermentation[J]. Renewable Energy, 2020, 148: 523-533. DOI:10.1016/j.renene.2019.10.058 |
| [32] |
KOUZUMA A, KATO S, WATANABE K. Microbial interspecies interactions: recent findings in syntrophic consortia[J]. Frontiers in Microbiology, 2015, 6: 477. |
| [33] |
MORITA M, MALVANKAR NS, FRANKS AE, SUMMERS ZM, GILOTEAUX L, ROTARU AE, ROTARU C, LOVLEY DR. Potential for direct interspecies electron transfer in methanogenic wastewater digester aggregates[J]. mBio, 2011, 2(4): e00159-11. |
| [34] |
NIELSEN LP, RISGAARD-PETERSEN N, FOSSING H, CHRISTENSEN PB, SAYAMA M. Electric currents couple spatially separated biogeochemical processes in marine sediment[J]. Nature, 2010, 463(7284): 1071-1074. DOI:10.1038/nature08790 |
| [35] |
PFEFFER C, LARSEN S, SONG J, DONG MD, BESENBACHER F, MEYER RL, KJELDSEN KU, SCHREIBER L, GORBY YA, EL-NAGGAR MY, LEUNG KM, SCHRAMM A, RISGAARD-PETERSEN N, NIELSEN LP. Filamentous bacteria transport electrons over centimetre distances[J]. Nature, 2012, 491(7423): 218-221. DOI:10.1038/nature11586 |
| [36] |
ZHANG DR, NIE ZY, LIU LZ, YANG HY, XIA JL. Mechanisms of microbial extracellular electron transfer and its application[J]. China Industrial Economics, 2018, 30(6): 680-689. (in Chinese) 张多瑞, 聂珍媛, 刘李柱, 杨洪英, 夏金兰. 微生物胞外电子传递过程及其应用研究进展[J]. 生命科学, 2018, 30(6): 680-689. DOI:10.13376/j.cbls/2018080 |
| [37] |
INOUE K, LEANG C, FRANKS AE, WOODARD TL, NEVIN KP, LOVLEY DR. Specific localization of the c-type cytochrome OmcZ at the anode surface in current-producing biofilms of Geobacter sulfurreducens[J]. Environmental Microbiology Reports, 2011, 3(2): 211-217. DOI:10.1111/j.1758-2229.2010.00210.x |
| [38] |
LIU X, ZHAN J, JING XY, ZHOU SG, LOVLEY DR. A pilin chaperone required for the expression of electrically conductive Geobacter sulfurreducens pili[J]. Environmental Microbiology, 2019, 21(7): 2511-2522. DOI:10.1111/1462-2920.14638 |
| [39] |
WANG FB, GU YQ, O'BRIEN JP, YI SM, YALCIN SE, SRIKANTH V, SHEN C, VU D, ING NL, HOCHBAUM AI, EGELMAN EH, MALVANKAR NS. Structure of microbial nanowires reveals stacked hemes that transport electrons over micrometers[J]. Cell, 2019, 177(2): 361-369.e10. DOI:10.1016/j.cell.2019.03.029 |
| [40] |
PENG L, ZHANG Y. Cytochrome OmcZ is essential for the current generation by Geobacter sulfurreducens under low electrode potential[J]. Electrochimica Acta, 2017, 228: 447-452. DOI:10.1016/j.electacta.2017.01.091 |
| [41] |
LOVLEY DR, WALKER DJF. Geobacter protein nanowires[J]. Frontiers in Microbiology, 2019, 10: 2078. DOI:10.3389/fmicb.2019.02078 |
| [42] |
WANG FB, CRAIG L, LIU X, RENSING C, EGELMAN EH. Microbial nanowires: type Ⅳ pili or cytochrome filaments?[J]. Trends in Microbiology, 2023, 31(4): 384-392. DOI:10.1016/j.tim.2022.11.004 |
| [43] |
YALCIN S E, MALVANKAR NS. The blind men and the filament: understanding structures and functions of microbial nanowires[J]. Current Opinion in Chemical Biology, 2020, 59: 193-201. DOI:10.1016/j.cbpa.2020.08.004 |
| [44] |
FILMAN DJ, MARINO SF, WARD JE, YANG L, MESTER Z, BULLITT E, LOVLEY DR, STRAUSS M. Cryo-EM reveals the structural basis of long-range electron transport in a cytochrome-based bacterial nanowire[J]. Communications Biology, 2019, 2: 219. DOI:10.1038/s42003-019-0448-9 |
| [45] |
LOVLEY DR, NEVIN KP. A shift in the current: new applications and concepts for microbe-electrode electron exchange[J]. Current Opinion in Biotechnology, 2011, 22(3): 441-448. DOI:10.1016/j.copbio.2011.01.009 |
| [46] |
LIU X, ZHUO SY, RENSING C, ZHOU SG. Syntrophic growth with direct interspecies electron transfer between pili-free Geobacter species[J]. The ISME Journal, 2018, 12(9): 2142-2151. DOI:10.1038/s41396-018-0193-y |
| [47] |
LEANG C, QIAN XL, MESTER T, LOVLEY DR. Alignment of the c-type cytochrome OmcS along pili of Geobacter sulfurreducens[J]. Applied and Environmental Microbiology, 2010, 76(12): 4080-4084. DOI:10.1128/AEM.00023-10 |
| [48] |
ROTARU AE, SHRESTHA PM, LIU FH, SHRESTHA M, SHRESTHA D, EMBREE M, ZENGLER K, WARDMAN C, NEVIN KP, LOVLEY DR. A new model for electron flow during anaerobic digestion: direct interspecies electron transfer to Methanosaeta for the reduction of carbon dioxide to methane[J]. Energy & Environmental Science, 2014, 7(1): 408-415. |
| [49] |
ROTARU AE, SHRESTHA PM, LIU FH, MARKOVAITE B, CHEN SS, NEVIN KP, LOVLEY DR. Direct interspecies electron transfer between Geobacter metallireducens and Methanosarcina barkeri[J]. Applied and Environmental Microbiology, 2014, 80(15): 4599-4605. DOI:10.1128/AEM.00895-14 |
| [50] |
GUPTA D, GUZMAN MS, BOSE A. Extracellular electron uptake by autotrophic microbes: physiological, ecological, and evolutionary implications[J]. Journal of Industrial Microbiology and Biotechnology, 2020, 47(9/10): 863-876. |
| [51] |
THAUER RK, KASTER AK, SEEDORF H, BUCKEL W, HEDDERICH R. Methanogenic Archaea: ecologically relevant differences in energy conservation[J]. Nature Reviews Microbiology, 2008, 6(8): 579-591. DOI:10.1038/nrmicro1931 |
| [52] |
YEE MO, ROTARU AE. Extracellular electron uptake in Methanosarcinales is independent of multiheme c-type cytochromes[J]. Scientific Reports, 2020, 10: 372. DOI:10.1038/s41598-019-57206-z |
| [53] |
LU J, CHANG J, LEE D. Adding carbon-based materials on anaerobic digestion performance: a mini-review[J]. Bioresource Technology, 2020, 300: 122696. DOI:10.1016/j.biortech.2019.122696 |
| [54] |
CHEN SS, ROTARU AE, SHRESTHA PM, MALVANKAR NS, LIU FH, FAN W, NEVIN KP, LOVLEY DR. Promoting interspecies electron transfer with biochar[J]. Scientific Reports, 2014, 4: 5019. DOI:10.1038/srep05019 |
| [55] |
ZHANG JS, ZHAO WQ, ZHANG HW, WANG ZJ, FAN CF, ZANG LH. Recent achievements in enhancing anaerobic digestion with carbon-based functional materials[J]. Bioresource Technology, 2018, 266: 555-567. DOI:10.1016/j.biortech.2018.07.076 |
| [56] |
YIN QD, WU GX. Advances in direct interspecies electron transfer and conductive materials: electron flux, organic degradation and microbial interaction[J]. Biotechnology Advances, 2019, 37(8): 107443. |
| [57] |
LOVLEY DR. Syntrophy goes electric: direct interspecies electron transfer[J]. Annual Review of Microbiology, 2017, 71: 643-664. DOI:10.1146/annurev-micro-030117-020420 |
| [58] |
LOVLEY DR, ANDERSON RT. Influence of dissimilatory metal reduction on fate of organic and metal contaminants in the subsurface[J]. Hydrogeology Journal, 2000, 8(1): 77-88. |
| [59] |
MAGNUSON TS, HODGES-MYERSON AL, LOVLEY DR. Characterization of a membrane-bound NADH-dependent Fe3+ reductase from the dissimilatory Fe3+-reducing bacterium Geobacter sulfurreducens[J]. FEMS Microbiology Letters, 2000, 185(2): 205-211. |
| [60] |
NEVIN KP, LOVLEY DR. Lack of production of electron-shuttling compounds or solubilization of Fe(Ⅲ) during reduction of insoluble Fe(Ⅲ) oxide by Geobacter metallireducens[J]. Applied and Environmental Microbiology, 2000, 66(5): 2248-2251. |
| [61] |
NEVIN KP, LOVLEY DR. Potential for nonenzymatic reduction of Fe(Ⅲ) via electron shuttling in subsurface sediments[J]. Environmental Science & Technology, 2000, 34(12): 2472-2478. |
| [62] |
WANG W, LEE D. Direct interspecies electron transfer mechanism in enhanced methanogenesis: a mini-review[J]. Bioresource Technology, 2021, 330: 124980. |
| [63] |
THAUER RK. Biochemistry of methanogenesis: a tribute to marjory stephenson: 1998 marjory stephenson prize lecture[J]. Microbiology, 1998, 144(9): 2377-2406. |
| [64] |
SHIN SG, HAN G, LIM J, LEE C, HWANG S. A comprehensive microbial insight into two-stage anaerobic digestion of food waste-recycling wastewater[J]. Water Research, 2010, 44(17): 4838-4849. |
| [65] |
CHENG QW, CALL DF. Hardwiring microbes via direct interspecies electron transfer: mechanisms and applications[J]. Environmental Science: Processes & Impacts, 2016, 18(8): 968-980. |
| [66] |
NISHIO K, HASHIMOTO K, WATANABE K. Light/electricity conversion by a self-organized photosynthetic biofilm in a single-chamber reactor[J]. Applied Microbiology and Biotechnology, 2010, 86(3): 957-964. |
| [67] |
NISHIO K, HASHIMOTO K, WATANABE K. Light/electricity conversion by defined cocultures of Chlamydomonas and Geobacter[J]. Journal of Bioscience and Bioengineering, 2013, 115(4): 412-417. |
| [68] |
HA PT, LINDEMANN SR, SHI L, DOHNALKOVA AC, FREDRICKSON JK, MADIGAN MT, BEYENAL H. Syntrophic anaerobic photosynthesis via direct interspecies electron transfer[J]. Nature Communications, 2017, 8: 13924. |
| [69] |
HUANG LY, LIU X, TANG JH, YU LP, ZHOU SG. Electrochemical evidence for direct interspecies electron transfer between Geobacter sulfurreducens and Prosthecochloris aestuarii[J]. Bioelectrochemistry, 2019, 127: 21-25. |
 2023, Vol. 50
2023, Vol. 50