扩展功能
文章信息
- 伍茜, 李雄婕, 喻东, 吴晓仪, 程建国, 罗燕, 王印, 杨泽晓, 姚学萍
- WU Xi, LI Xiongjie, YU Dong, WU Xiaoyi, CHENG Jianguo, LUO Yan, WANG Yin, YANG Zexiao, YAO Xueping
- 林麝源支气管败血波氏杆菌FMDBb1株的分离鉴定及全基因组序列分析
- Isolation, identification and whole-genome analysis of Bordetella bronchiseptica FMDBb1 from forest musk deer (Moschus berezovskii)
- 微生物学通报, 2021, 48(12): 4731-4741
- Microbiology China, 2021, 48(12): 4731-4741
- DOI: 10.13344/j.microbiol.china.210410
-
文章历史
- 收稿日期: 2021-05-10
- 接受日期: 2021-06-10
- 网络首发日期: 2021-07-26
2. 四川养麝研究所 四川 都江堰 611800
2. Sichuan Institute of Musk Deer Breeding, Dujiangyan, Sichuan 611800, China
支气管败血波氏杆菌(Bordetella bronchiseptica)是一种广泛分布于自然界的常见病原菌,具有O、K和H抗原,能感染多种哺乳动物,引起急、慢性呼吸道炎症,常见的有犬传染性气管支气管炎、兔传染性鼻炎和猪传染性萎缩性鼻炎[1-3]。越来越多的支气管败血波氏杆菌作为人类临床分离株被报道,提示免疫抑制的人也会感染该菌[4]。由于基因水平的相似性,支气管败血波氏杆菌与同属的百日咳波氏杆菌(Bordetella pertussis)和副百日咳波氏杆菌(Bordetella parapertussis)被称为经典波氏杆菌亚种,常常将其一起研究[5]。三者携带的毒力因子基本相同,但是只有支气管败血波氏杆菌能广泛感染多种哺乳动物。不同波氏杆菌间的宿主和毒力差异由双组分转导系统BvgA/S的进化差异决定[6-8]。
林麝(Moschus berezovskii)是国家一级保护野生动物,其分泌的麝香具有极高的药用价值和经济价值[9]。自1910年首次从犬呼吸道分离至今,美国国家生物技术信息中心(National Center for Biotechnology Information,NCBI)的Gemone数据库已收录超过90株支气管败血波氏杆菌的全基因组序列,Register等[10]也报道了广泛的陆生和水生动物源支气管败血波氏杆菌分离株的基因组序列大数据,而林麝源的全基因组测序研究还处于空白阶段。据统计,呼吸系统疾病是圈养麝的常见疾病之一,主要由细菌引起,而支气管败血波氏杆菌在其中所起的作用往往被低估[11]。支气管败血波氏杆菌在侵入呼吸道后,除了通过自身的毒素发挥直接致病作用外,部分毒力因子还能破坏呼吸道的防御屏障,造成呼吸系统抵抗力下降,促进其他多种病原定殖,导致继发感染增加林麝呼吸系统疾病的发病率和严重程度[12-14]。为了保证和促进人工养麝业的发展,做好圈养麝的疾病防治十分重要。一般来说,抗生素治疗是养殖业疾病防治的重要手段,但由于药物滥用及细菌耐药性的产生,常常使治疗失效,疾病难以控制。因此本研究对一株致病性林麝源支气管败血波氏杆菌进行了分离鉴定和全基因组测序,探究其遗传进化,并结合表型分析其致病和耐药机制,以期为圈养麝防治该类疾病提供参考。
1 材料与方法 1.1 材料病料来源于四川都江堰养麝研究所一头患病林麝的鼻黏液。所用培养基、药敏纸片、细菌微量生化鉴定管等,杭州微生物试剂有限公司。48只SPF级昆明小鼠,成都达硕实验动物有限公司。
1.2 病原菌的分离和纯化培养将病料分别划线接种于麦康凯培养基和血琼脂培养基,于37 ℃培养箱放置24-48 h,根据菌落形态特征和革兰氏染色结果,挑取单菌落进一步纯化、保存。
1.3 生化试验依据细菌的理化特性,按说明书将纯化菌接种到细菌微量生化反应管中并观察结果。
1.4 药敏试验采用Kirby-Barer纸片法,选用18种抗生素,包括哌拉西林、氨苄西林、阿莫西林、头孢拉定、头孢曲松、氨曲南、亚胺培南、庆大霉素、链霉素、丁胺卡那、妥布霉素、四环素、氟苯尼考、林可霉素、诺氟沙星、左氧氟沙星、环丙沙星和利福平,参照美国临床和实验室标准协会(Clinical and Laboratory Standards Institute,CLSI)鉴定手册(2017版)筛选分离菌的药物敏感性[15]。
1.5 小鼠致病性试验将8只小鼠平均分为2组,一组腹腔注射浓度为3×108 CFU/mL的活菌液,0.4 mL/只;另一组注射等量生理盐水作为对照组。正常饲喂,观察并记录小鼠状态,以此作为预试验。同时对死亡小鼠进行剖检,观察脏器变化,并采集其肺脏组织制作病理组织切片。然后根据小鼠死亡情况用生理盐水将菌液10倍稀释5个浓度梯度,每个浓度的菌液分别注射5组小鼠,每组8只,根据注射菌液浓度由高到低依次对每组编号1、2、3、4、5,注射方法同预试验,记录7 d内每组小鼠的死亡数,并使用Bliss法计算半数致死量(LD50)。
1.6 病原菌全基因组测序及序列分析使用的测序策略为全基因组鸟枪法(Whole Genome Shotgun,WGS),样品经过质检后构建基因组上机文库,使用第二代测序技术,测序平台为Illumina NovaSeq,测序模式为双末端(Paired-End,PE)测序,并采用A5-MiSeq和SPAdes对测序数据进行拼装。基因组测序工作由上海派森诺生物科技股份有限公司完成。
1.7 基因组分析使用在线工具ANI Calculator (http://enve-omics.ce.gatech.edu/ani/index),将FMDBb1与该属其他代表菌株进行平均核苷酸一致性(Average Nucleotide Identity,ANI)比对;使用Clusters of Orthologous Groups (COG)数据库和Kyoto Encyclopedia of Genes and Genomes (KEGG)数据库对功能基因进行预测;分别采用毒力因子数据库(www.mgc.ac.cn/VFs/)和综合抗生素耐药性数据库(https://card.mcmaster.ca)对其携带的毒力基因和耐药基因进行注释;ISFinder (https://www-is.biotoul.fr/)用于检测基因组中的插入序列元素。噬菌体搜索工具(http://phast.wishartlab.com/)用于注释基因组内的前噬菌体序列;最后PubMLST数据库(https://pubmlst.org)用于FMDBb1的序列类型测定,并选取NCBI中的31株相关菌株,使用MEGA 6.0软件基于各个菌株的管家基因进行多基因联合建树分析。所有BLAST参数默认e值≤1×10-5,一致性≥40%,覆盖率≥40%。
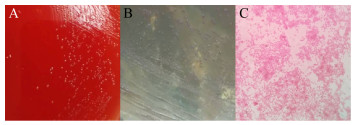
2 结果与分析 2.1 FMDBb1菌株的生物学及理化特征分离菌在血琼脂培养基上形成圆形、光滑、半透明菌落,未见明显溶血(图 1A);麦康凯培养基上形成光滑的灰色菌落,培养基着染琥珀色(图 1B)。革兰氏染色镜检,可见红色、两端钝圆的小杆菌(图 1C)。
|
| 图 1 分离菌在血琼脂培养基(A)、麦康凯培养基(B)上的菌落形态与革兰氏染色镜检结果(C) Figure 1 The colony morphology of isolated bacteria on blood agar medium (A) and McConkey medium (B) and the result of Gram staining microscopy (C) |
|
|
生化试验结果(表 1)显示,该菌株不分解糖类;不产生H2S;能还原硝酸盐;枸橼酸盐、氧化酶、脲酶试验阳性;MR-VP试验阴性。菌落形态和生化结果均符合支气管败血波氏杆菌的鉴别特征。
| 试验项目 Test items | 结果 Results |
| Glucose | - |
| Lactose | - |
| Sucrose | - |
| Maltose | - |
| H2S | - |
| Nitrate | + |
| Oxidase | + |
| Citrate | + |
| Urease | + |
| MR-VP | - |
| 注:+:阳性;-:阴性 Note: +: Positive; -: Negative |
|
如表 2所示,药敏试验结果表明,该菌株对四环素、氟苯尼考、少数β-内酰胺类药物(哌拉西林、亚胺培南)、多种氨基糖苷类药物(庆大霉素、丁胺卡那、妥布霉素)和喹诺酮类药物敏感,对林可霉素、利福平和多种β-内酰胺类药物(氨苄西林、阿莫西林、头孢拉定、氨曲南)耐药。
| 抗生素类别 Antibiotic category |
药物名称 Drug names |
抑菌圈直径 Inhibition zone diameters (mm) |
结果 Results |
| β-lactam antibiotics | Piperacillin | 36 | S |
| Ampicillin | 6 | R | |
| Amoxicillin | 6 | R | |
| Cefradine | 6 | R | |
| Ceftriaxone | 20 | I | |
| Aztreonam | 6 | R | |
| Imipenem | 25 | S | |
| Tetracycline | Tetracycline | 31 | S |
| Amphenicols | Florfenicol | 31 | S |
| Aminoglycosides | Amikacin | 29 | S |
| Tobramycin | 25 | S | |
| Gendamycin | 30 | S | |
| Streptomycin | 13 | I | |
| Lincosamide | Lincomycin | 6 | R |
| Quinolones | Norfloxacin | 26 | S |
| Levofloxacin | 31 | S | |
| Ciprofloxacin | 30 | S | |
| Rifamycin | Rifampicin | 6 | R |
| 注:S:敏感;I:中介;R:耐药 Note: S: Sensitive; I: Intermediary; R: Resistance |
|||
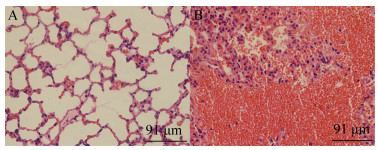
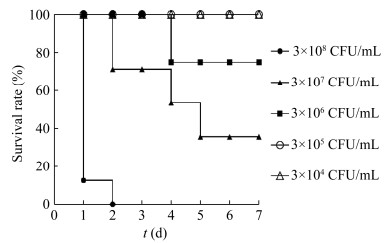
试验组注射3×108 CFU/mL的活菌菌液后,4只小鼠在2 h内呈现萎靡状,6 h左右出现明显抱团昏睡,食欲饮欲不振,10-12 h内全部死亡。对照组小鼠均存活。剖检并对比2组小鼠,可见试验组肺脏有明显出血及肉变。病理组织切片见图 2,结果显示肺脏严重出血,肺泡内大量红细胞、淋巴细胞和中性粒细胞浸润。对照组未见明显异常。使用不同浓度梯度的菌液攻毒小鼠后,7 d内每组小鼠的生存情况如图 3所示。采用Bliss法计算得知,该菌对小鼠的LD50为8.55×106 CFU。
|
| 图 2 FDMBb1菌株感染小鼠的肺脏HE染色结果(40×) Figure 2 HE staining of strain FDMBb1 infected mice lung tissues (40×) 注:A:对照组;B:实验组 Note: A: The control group; B: The experimental group |
|
|
|
| 图 3 攻毒小鼠7 d内生存曲线 Figure 3 Survival curve of challenged mice within 7 d |
|
|
测序后得到FMDBb1菌株全基因组大小为5 133 936 bp,Contig数量39 (N50为265 744 bp),Scaffold数量37 (N50为268 483 bp),GC含量为68.21%,编码4 813个基因,包含tRNA 53个,rRNA 3个。将FASTQ格式的原始数据上传至NCBI的SRA数据库,登录号为SRR10199526;拼装后的序列以FASTA形式上传至Genome数据库,登录号为WAGZ00000000。
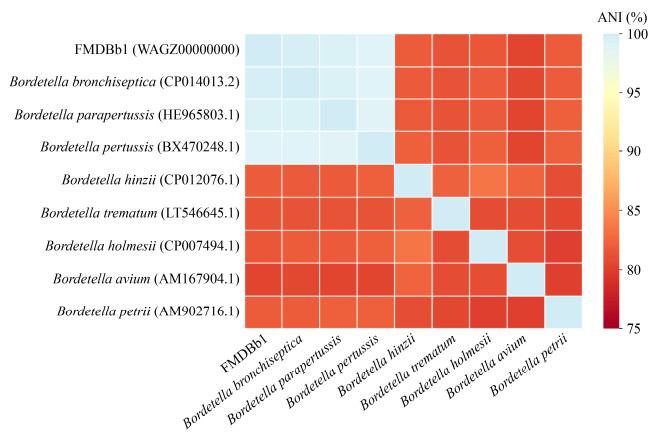
2.5 ANI分析以95%的ANI作为物种划分与物种聚类的标准[16],由图 4可知,FMDBb1、FDAARGOS_176、Bpp5和Tohama I菌株之间的ANI值均高于95%的分类阈值且十分相近,其余菌株之间的ANI值均小于90%,因此根据ANI比对结果只能判断FMDBb1菌株属于经典波氏杆菌,同时结果显示了经典波氏杆菌亚种间极其相近的亲缘关系。
|
| 图 4 FDMBb1与波氏杆菌属代表菌株的ANI比对 Figure 4 ANI results among FMDBb1 and representative strains of Bordetella 注:括号内为该菌株的NCBI登录号 Note: The NCBI accession number of the strain is shown in brackets |
|
|
通过与数据库的比对分析,共有4 458个基因被注释到21组COG的功能中,其中3 317个蛋白与已知蛋白或已知的假设蛋白同源,1 141个蛋白功能未知,约占总数的25.6%,其余数量最多的是氨基酸转运与代谢相关蛋白和转录相关蛋白,分别是472个和430个。同时,5 316个蛋白被注释到KEGG功能分类中,9个一级分类里与新陈代谢有关的蛋白数量最多,共2 096个,占总数的39.4%,子类别中则是Brite层级中的信号转导和细胞进程蛋白家族数量最多,共926个,占17.4%。另外,有147个蛋白因缺乏特征而未被包含在通路和Brite数据库中。
2.6.2 毒力因子注释在FMDBb1菌株的基因组中检测到了多个基因分别编码FMDBb1的不同毒力因子,包括了介导黏附、分泌、抗血清作用和直接作为毒素存在的蛋白。支气管败血波氏杆菌的特征性毒力因子被检测到的有丝状血凝素(Filamentous Hemagglutinin,FHA)、百日咳素(Pertacin,PRN)、气管定殖因子(Tracheal Colonization Factor)、腺苷酸环化酶溶血素(Adenylate Cyclase-Haemolysin,AC-Hly)和皮肤坏死毒素(Dermonecrotic Toxin,DNT),气管细胞毒素和骨毒素并未在该菌株中检测到。相关结果如表 3所示。
| 功能 Function |
毒力因子 Virulence factors |
相关基因 Related genes |
| Adherence | Fimbriae | fimA, fimB, fimC, fimD, fimX, fim2 |
| Pertactin | prn | |
| Filamentous hemagglutinin | fhaB, fhaC | |
| Tracheal colonization factor | tcfA* | |
| Endotoxin | Lipopolysaccharide (LPS) | bplA, bplB, bplC, bplD, bplE, bplF, bplG, bplH, bplI, bplL |
| Secretion system | Ptl type Ⅳ secretion system | ptlA, ptlC, ptlD, ptlE, ptlF, ptlG, ptlH |
| Type Ⅲ secretion system (T3SS) | bscF, bscE, bscD, bcrD, bcrH1, bcrH2, bcr4, bscI, bscJ, bscK, bscL, bscN, bscO, bscP, bscQ, bscR, bscS, bscT, bscU, bscW, bscC | |
| TTSS secreted proteins | bopB, bopC, bopD, bopN, bsp22 | |
| Serum resistance | BrkAB system | brkA*, brkB |
| Toxin | Pertussis toxin (PT) | ptxA, ptxB, ptxC, ptxE |
| Dermonecrotic toxin (DNT) | dnt | |
| Adenylate cyclase | cyaE, cyaD, cyaB, cyaA, cyaC | |
| 注:*:假基因 Note: *: Pseudogene |
||
在FMDBb1菌株的基因组中发现有多种耐药基因,其中仅有2个基因为靶向的抗性基因,分别与粉霉素、利福平相关,其余绝大多数耐药基因注释为多药耐药外排泵。结果见表 4。
| 耐药基因种类 Resistant gene category |
耐药基因 Resistant gene |
| Anti-pulvomycin | EF-Tu |
| Anti-rifampicin | rpoB |
| Efflux pump conferring antibiotic resistance | adeF, acrB, mdtB, ceoB, oprM, AxyY, MexB, MexD, mexI, mexW, mexN, MuxB, MuxC, smeB, smeE |
如表 5所示,FMDBb1菌株共发现19个属于6个IS家族的IS元件,并且这些IS元件的起源各异,大多数与百日咳波氏杆菌有关,其中起源于百日咳波氏杆菌的IS1663数目有5个,其余种类的IS元件数目均只发现1个。
| 家族 Family |
名称 Name |
起源 Origin |
数量 Number |
| IS110 | IS1663 | Bordetella pertussis | 5 |
| IS3 | ISXac4 | Xanthomonas axonopodis | 1 |
| Tn3 | ISAzs17 | Azospirillum sp. | 1 |
| ISShes11 | Shewanella sp. | 1 | |
| IS1182 | ISThsp16 | Thiomonas sp. | 1 |
| ISL3 | IS1001 | Bordetella parapertussis | 1 |
| ISRta1 | Ralstonia taiwanensis | 1 | |
| ISRso15 | Ralstonia solanacearum | 1 | |
| ISThsp14 | Thiomonas sp. | 1 | |
| ISBma1 | Burkholderia mallei | 1 | |
| IS481 | IS481v2 | Bordetella pertussis | 1 |
| IS481v1 | Bordetella pertussis | 1 | |
| IS481 | Bordetella pertussis | 1 | |
| ISBcen26 | Burkholderia cenocepacia | 1 | |
| ISCte4 | Comamonas testosteroni | 1 |
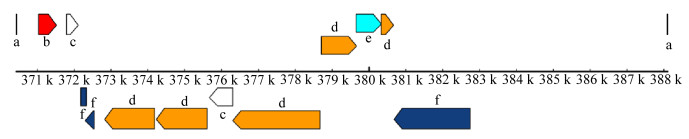
通过PHAST预测,FMDBb1基因组中仅发现一个噬菌体区域存在,位于Contig3的370 428-388 089 bp处,如图 5所示,该区域长度为17.6 kb,包含12个CDS,GC含量为67.8%,其中发现的与噬菌体相关的蛋白质类型为整合酶和末端酶。由于该区域的总分(分配给该区域的数字以及该区域的核苷酸序列的长度,以bp为单位)小于70,因此认为该区域不完整。
|
| 图 5 FMDBb1菌株的前噬菌体视图及其噬菌体元件注释 Figure 5 The prophage view and phage elements annotated of strain FMDBb1 注:a:附着位点;b:整合酶;c:其他;d:其他噬菌体样蛋白;e:末端酶;f:假设蛋白 Note: a: Attachment site; b: Integrase; c: Others; d: Other phage-like proteins; e: Terminal enzyme; f: Hypothetical protein |
|
|
基于PubMLST数据库,波氏杆菌属有7个管家基因,分别是adk、fumC、glyA、tyrB、icd、pepA、pgm。根据7个位点的等位基因,得到FMDBb1菌株的序列类型为ST33,克隆复合体类型为CC6。
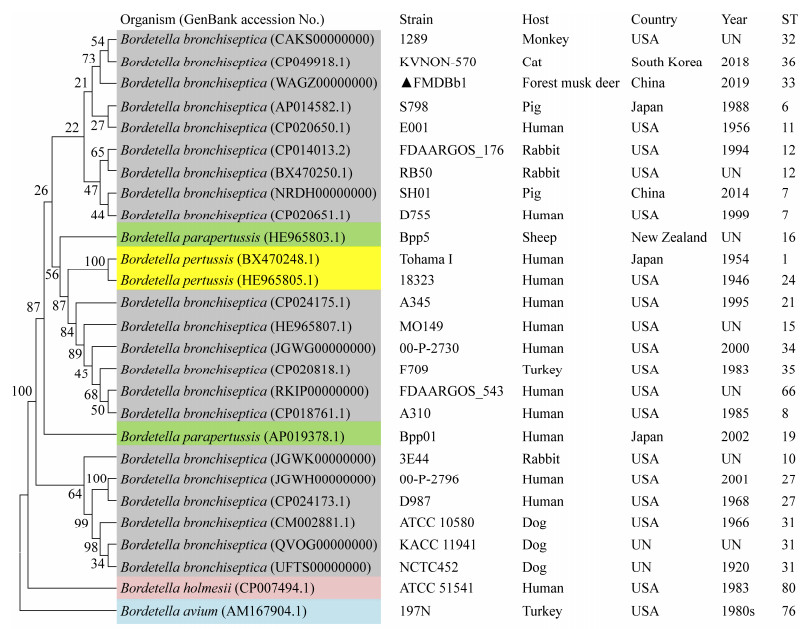
由管家基因串联建立的系统进化树如图 6所示,与其余波氏杆菌菌种不同,百日咳波氏杆菌和副百日咳波氏杆菌在进化树上均不独立成簇,而且与支气管败血波氏杆菌的系统发育距离非常接近。系统发育研究表明,林麝分离株FMDBb1与2018年分离于韩国短毛猫的KVNON-570菌株亲缘关系较近。
|
| 图 6 波氏杆菌的基于管家基因构建的系统发育树 Figure 6 Phylogenetic tree of Bordetella based on housekeeping genes 注:▲:本研究分离的FDMBb1菌株;UN:未知;ST:序列类型。分支点上的数字表示Bootstrap检验的置信度。不同颜色代表不同的波氏杆菌 Note: ▲: The FDMBb1 strain isolated in this study; UN: Unknown; ST: Sequence type. The number on each node represents the confidence value of the bootstrap test. Each species were marked in different colors |
|
|
支气管败血波氏杆菌作为一种人畜共患病原菌,常与其他病原体协同作用提高呼吸道疾病发病率并加重其严重程度,给人和动物的健康都造成威胁[13]。由于林麝品种的独特性,目前缺乏麝源支气管败血波氏杆菌相关报道。本研究的FMDBb1菌株在麦康凯培养基和血琼脂培养基均能良好生长,可见其营养需求简单。全基因组测序显示该序列属于大型基因组,结合COG和KEGG注释可知,FMDBb1菌株拥有强新陈代谢能力和抗逆性。目前,与16S rRNA基因和DNA-DNA杂交等传统的物种鉴定方法相比,ANI分析简单、快速、准确,被认为是确定所研究菌种的分类信息最佳且必要的方法之一[16-18]。但值得注意的是,本研究中经典波氏杆菌间的ANI值均大于分类阈值,倡导的ANI分析作为菌种分类方法无法准确到经典波氏杆菌亚种,菌种鉴定时仍需结合菌落特征和生化等其他结果判断。
从对小鼠的攻毒情况可推知,该菌株对小鼠具有较强的致病性,而细菌的致病性通常与其毒力因子之间有着密切的联系。一般来说,细菌与宿主组织的黏附是成功定殖和感染的第一步,而FMDBb1菌株的毒力因子中,菌毛、FHA、PRN和气管定殖因子等蛋白均具有免疫逃避和黏附宿主细胞等生物学活性[12]。多种黏附素协同作用使其拥有强大的定殖功能。此外,百日咳毒素能引起急性感染,抑制中性粒细胞迁移以及对抗抗体,是最复杂的细菌蛋白毒素之一,同时也是百日咳波氏杆菌的主要毒力因子,但支气管败血波氏杆菌相应启动子未激活,因此虽携带编码该蛋白的基因,最终却并不产生百日咳毒素[19]。除此之外,其余直接导致宿主病理损伤的因子中,DNT可通过损坏呼吸道保护层上皮细胞致其坏死而间接地促进菌株的黏附作用,是支气管败血波氏杆菌导致猪发生鼻甲骨萎缩的直接致病因子,研究显示,产生DNT的菌株比不产生DNT的菌株具有更强的致病力[20-22]。同样,AC-Hly除了裂解红细胞外,也可作为腺苷环化酶催化cAMP大量产生,导致肺泡巨噬细胞和免疫效应细胞吞噬作用被破坏,是支气管败血波氏杆菌杀死肺泡巨噬细胞最有可能的工具[12, 23]。本研究中,攻毒浓度为108 CFU/mL的小鼠均短期死亡,推测DNT和AC-Hly这2种直接导致宿主病理损伤的因子在感染过程中的表达可能是造成该结果的重要原因。
由药物敏感表型可知,FMDBb1菌株对林可霉素、利福平以及大多数β-内酰胺类抗生素耐药,对四环素、氟苯尼考、氟喹诺酮类和大多数氨基糖苷类药物敏感。但对于耐药基因,除了多药耐药外排泵外,仅预测到2个基因分别对粉霉素和利福平有明确抗性。可以看到,对于β-内酰胺类的抗性,出现了表型和基因型不一致的结果。对于β-内酰胺类表型耐药,基因型未检出的情况,推测原因有多种情况。首先,耐药基因预测得到的外排泵基因均属于Resistance-Nodulation-Division (RND)家族,而RND外排泵家族介导了对多种抗菌药物的耐药性,包括β-内酰胺类[24-25]。其次,生物膜的形成也增加了对生物和非生物因子的耐受性。也有研究表明,低的膜渗透性可能有助于支气管败血波氏杆菌对β-内酰胺的抵抗[26]。根据以往的报道,β-内酰胺类在人类临床上作为首选抗生素的使用并未在其感染中获得成功的治疗,相反,与β-内酰胺酶抑制剂联用的治疗是成功的[27]。支气管败血波氏杆菌中存在具有物种特异性的β-内酰胺酶基因blaBOR-1[28]。因此也可能该基因位于移动遗传元件,由于其不稳定性,导致测序深度不充分而未被组装出来。
细菌基因组中的移动遗传元件(Mobile Genetic Element,MGE),不仅影响基因组的多样性和可塑性,而且还通过改变毒力或耐药性来增强细菌对环境的适应性[29]。大多数抗性基因都位于质粒上,除质粒外,支气管败血波氏杆菌还利用基因盒作为MGE,β-内酰胺抗性基因已被描述为基因盒的一部分[30]。此外,IS元件和噬菌体也是波氏杆菌重要的MGE,它们不仅能遗传给下一代细菌,还可以通过转化、转导、接合等方式转移给其他种属的细菌,是引起耐药性散播的主要原因[31]。Liu等[32]对一组波氏杆菌温和噬菌体的研究也进一步支持了编码蛋白质结构域、单个基因或基因块的区域在细菌基因组和噬菌体基因组之间容易交换的观点。Wang等[33]的研究发现,分离到的菌株中拥有最多IS元件的SH01株同时拥有最大的耐药性。FMDBb1菌株存在的19个IS元件,其中有9个起源于经典波氏杆菌,这些IS元件的多样性及存在的噬菌体区域,都可能有助于细菌基因组的多样性和进化。
本研究中,ANI和系统发育分析都清楚地表明了经典波氏杆菌的种间高度相关性,而在这些亚种间均存在人类分离株。Parkhill等[34]的研究发现,这些宿主局限的菌株大概率都由支气管败血波氏杆菌进化而来,而且宿主的适应似乎是功能丧失而不是获得的结果,毒力的差异可能也与调节或控制功能的丧失有关,这表明来自不同物种宿主的分离株可能越过物种屏障而导致人类感染。支气管败血波氏杆菌造成的呼吸道疾病具有传染性,病原体往往又在症状初显前就已携带,并在动物甚至免疫低下的人类之间传播,还能继发其他疾病感染。鉴于目前林麝源支气管败血波氏杆菌研究领域的空白情况,FMDBb1菌株的基因组测序和注释将有助于该病原菌感染的预防和控制措施的制定,为将来的进一步研究提供了宝贵的遗传信息。
| [1] |
Day MJ, Carey S, Clercx C, Kohn B, MarsilIo F, Thiry E, Freyburger L, Schulz B, Walker DJ. Aetiology of canine infectious respiratory disease complex and prevalence of its pathogens in Europe[J]. Journal of Comparative Pathology, 2020, 176: 86-108. DOI:10.1016/j.jcpa.2020.02.005 |
| [2] |
Zimmerman JJ, Karriker LA, Ramirez A, Schwartz KJ, Stevenson GW, Zhang JQ. Diseases of Swine[M]. 11th ed. USA: John Wiley & Sons, 2019: 767-777.
|
| [3] |
Wang XF, Liu Y, Xiao CW, Bao GL, Cui YS, Li JL, Ji QA, Wei Q. Isolation, identification and detection of drug resistant genes of rabbit Bordetella bronchiseptica[J]. China Animal Husbandry & Veterinary Medicine, 2015, 42(3): 544-548. (in Chinese) 王晓芳, 刘燕, 肖琛闻, 鲍国连, 崔言顺, 李建亮, 季权安, 韦强. 兔支气管败血波氏杆菌的分离鉴定及耐药基因检测[J]. 中国畜牧兽医, 2015, 42(3): 544-548. |
| [4] |
Ducours M, Rispal P, Danjean MP, Imbert Y, Dupont E, Traissac EM, Grosleron S. Bordetella bronchiseptica infection[J]. Medecine et Maladies Infectieuses, 2017, 47(7): 453-458. DOI:10.1016/j.medmal.2017.05.012 |
| [5] |
Park J, Zhang Y, Buboltz AM, Zhang XQ, Schuster SC, Ahuja U, Liu M, Miller JF, Sebaihia M, Bentley SD, et al. Comparative genomics of the classical Bordetella subspecies: the evolution and exchange of virulence-associated diversity amongst closely related pathogens[J]. BMC Genomics, 2012, 13: 545. DOI:10.1186/1471-2164-13-545 |
| [6] |
Lu CP. Veterinary Microbiology[M]. 5th ed. Beijing: China Agriculture Press, 2012: 152-153. (in Chinese) 陆承平. 兽医微生物学[M]. 5版. 北京: 中国农业出版社, 2012: 152-153. |
| [7] |
Nicholson TL. Construction and validation of a first-generation Bordetella bronchiseptica long- oligonucleotide microarray by transcriptional profiling the Bvg regulon[J]. BMC Genomics, 2007, 8: 220. DOI:10.1186/1471-2164-8-220 |
| [8] |
Cotter PA, Jones AM. Phosphorelay control of virulence gene expression in Bordetella[J]. Trends in Microbiology, 2003, 11(8): 367-373. DOI:10.1016/S0966-842X(03)00156-2 |
| [9] |
Luo Y, Wang Y. Common Bacterial Diseases and the Prevention of Musk[M]. Chengdu: Sichuan Scientific & Technical Publishers, 2018: 208-212. (in Chinese) 罗燕, 王印. 麝常见细菌性疾病及其防治[M]. 成都: 四川科学技术出版社, 2018: 208-212. |
| [10] |
Register KB, Ivanov YV, Jacobs N, Meyer JA, Goodfield LL, Muse SJ, Smallridge WE, Brinkac L, Kim M, Sanka R, et al. Draft genome sequences of 53 genetically distinct isolates of Bordetella bronchiseptica representing 11 terrestrial and aquatic hosts[J]. Genome Announcements, 2015, 3(2): e00152-e00115. |
| [11] |
Liu CY. A study on reasons of death and physiological features for breeding forest musk deer (Moschus berezovskii)[D]. Shanghai: Doctoral Dissertation of East China Normal University, 2008 (in Chinese) 刘春燕. 林麝Moschus berezovskii养殖种群死亡原因及其生命生理特征研究[D]. 上海: 华东师范大学博士学位论文, 2008 |
| [12] |
Pei J, He H, Zhao ZQ, Wu B. Research progress of Bordetella bronchiseptica[J]. Chinese Journal of Animal Husbandry and Veterinary Medicine, 2006(2): 4-6. (in Chinese) 裴洁, 何华, 赵战勤, 吴斌. 支气管败血波氏杆菌的研究进展[J]. 畜牧兽医科技信息, 2006(2): 4-6. DOI:10.3969/j.issn.1671-6027.2006.02.002 |
| [13] |
García-De-La-Fuente C, Guzmán L, Cano ME, Agüero J, Sanjuán C, Rodríguez C, Aguirre A, Martínez-Martínez L. Microbiological and clinical aspects of respiratory infections associated with Bordetella bronchiseptica[J]. Diagnostic Microbiology and Infectious Disease, 2015, 82(1): 20-25. DOI:10.1016/j.diagmicrobio.2015.01.011 |
| [14] |
Brockmeier SL. Prior infection with Bordetella bronchiseptica increases nasal colonization by Haemophilus parasuis in swine[J]. Veterinary Microbiology, 2004, 99(1): 75-78. DOI:10.1016/j.vetmic.2003.08.013 |
| [15] |
CLSI. Performance Standards for Antimicrobial Susceptibility Testing[M]. 27th ed. Wayne, PA: Clinical and Laboratory Standards Institute, 2017: 54-55.
|
| [16] |
Jain C, Rodriguez-R LM, Phillippy AM, Konstantinidis KT, Aluru S. High throughput ANI analysis of 90K prokaryotic genomes reveals clear species boundaries[J]. Nature Communications, 2018, 9: 5114. DOI:10.1038/s41467-018-07641-9 |
| [17] |
Goris J, Konstantinidis KT, Klappenbach JA, Coenye T, Vandamme P, Tiedje JM. DNA-DNA hybridization values and their relationship to whole-genome sequence similarities[J]. International Journal of Systematic and Evolutionary Microbiology, 2007, 57(Pt 1): 81-91. |
| [18] |
Kim M, Oh HS, Park SC, Chun J. Towards a taxonomic coherence between average nucleotide identity and 16S rRNA gene sequence similarity for species demarcation of prokaryotes[J]. International Journal of Systematic and Evolutionary Microbiology, 2014, 64(Pt 2): 346-351. |
| [19] |
Li X, Zhang XC, Xie GL. Advances in research of pertussis toxin[J]. Chinese Journal of Biologicals, 2018, 31(2): 215-219, 224. (in Chinese) 李鑫, 张新创, 谢贵林. 百日咳毒素的研究进展[J]. 中国生物制品学杂志, 2018, 31(2): 215-219, 224. |
| [20] |
Xiao L, Wu XL, Wang Y, Yang ZX, Yao XP, Hu L, Lin XY, Ren MS, Luo ZY, Zeng XJ. Isolation and identification of Bordetella bronchiseptica from swine and skin virulence test of DNT crude extraction to mice[J]. Journal of China Agricultural University, 2016, 21(7): 85-91. (in Chinese) 肖璐, 邬旭龙, 王印, 杨泽晓, 姚学萍, 胡凌, 林星宇, 任梅渗, 罗忠永, 曾相杰. 猪源支气管败血波氏杆菌的分离鉴定及其皮肤坏死素(DNT)粗提液的小鼠皮肤毒性试验[J]. 中国农业大学学报, 2016, 21(7): 85-91. |
| [21] |
Zhu MX, Zhang HR, Zhang B, Xu F. Isolation, identification and biological characterization of Bordetella bronchiseptica from swine[J]. Chinese Veterinary Science, 2017, 47(3): 341-345. (in Chinese) 诸明欣, 张焕容, 张斌, 徐凤. 猪支气管败血波氏杆菌的分离鉴定及部分生物学特性的研究[J]. 中国兽医科学, 2017, 47(3): 341-345. |
| [22] |
Brockmeier SL, Register KB, Magyar T, Lax AJ, Pullinger GD, Kunkle RA. Role of the dermonecrotic toxin of Bordetella bronchiseptica in the pathogenesis of respiratory disease in swine[J]. Infection and Immunity, 2002, 70(2): 481-490. DOI:10.1128/IAI.70.2.481-490.2002 |
| [23] |
Hibrand-Saint Oyant L, Bourges D, Chevaleyre C, Raze D, Locht C, Salmon H. Role of Bordetella bronchiseptica adenylate cyclase in nasal colonization and in development of local and systemic immune responses in piglets[J]. Veterinary Research, 2005, 36(1): 63-77. DOI:10.1051/vetres:2004056 |
| [24] |
Pages JM, Lavigne JP, Leflon-Guibout V, Marcon E, Bert F, Noussair L, Nicolas-Chanoine MH. Efflux pump, the masked side of beta-lactam resistance in Klebsiella pneumoniae clinical isolates[J]. PLoS One, 2009, 4(3): e4817. DOI:10.1371/journal.pone.0004817 |
| [25] |
Li XZ, Plésiat P, Nikaido H. The challenge of efflux-mediated antibiotic resistance in Gram-negative bacteria[J]. Clinical Microbiology Reviews, 2015, 28(2): 337-418. DOI:10.1128/CMR.00117-14 |
| [26] |
Kadlec K, Wiegand I, Kehrenberg C, Schwarz S. Studies on the mechanisms of beta-lactam resistance in Bordetella bronchiseptica[J]. The Journal of Antimicrobial Chemotherapy, 2007, 59(3): 396-402. DOI:10.1093/jac/dkl515 |
| [27] |
Wernli D, Emonet S, Schrenzel J, Harbarth S. Evaluation of eight cases of confirmed Bordetella bronchiseptica infection and colonization over a 15-year period[J]. Clinical Microbiology and Infection, 2011, 17(2): 201-203. DOI:10.1111/j.1469-0691.2010.03258.x |
| [28] |
Lartigue MF, Poirel L, Fortineau N, Nordmann P. Chromosome-borne class A BOR-1 beta-lactamase of Bordetella bronchiseptica and Bordetella parapertussis[J]. Antimicrobial Agents and Chemotherapy, 2005, 49(6): 2565-2567. DOI:10.1128/AAC.49.6.2565-2567.2005 |
| [29] |
Frost LS, Leplae R, Summers AO, Toussaint A. Mobile genetic elements: the agents of open source evolution[J]. Nature Reviews Microbiology, 2005, 3(9): 722-732. DOI:10.1038/nrmicro1235 |
| [30] |
Kadlec K, Schwarz S. Antimicrobial resistance in Bordetella bronchiseptica[J]. Microbiology Spectrum, 2018, 6(4): 10.1128/microbiolspec. ARBA-0024-2017
|
| [31] |
Yang L. Isolation, identification and characterization of Bordetella bronchiseptica and its bacteriophage[D]. Wuhan: Master's Thesis of Huazhong Agricultural University, 2019 (in Chinese) 杨斓. 支气管败血波氏杆菌及其噬菌体的分离鉴定与特性研究[D]. 武汉: 华中农业大学硕士学位论文, 2019 |
| [32] |
Liu M, Gingery M, Doulatov SR, Liu Y, Hodes A, Baker S, Davis P, Simmonds M, Churcher C, Mungall K, et al. Genomic and genetic analysis of Bordetella bacteriophages encoding reverse transcriptase-mediated tropism-switching cassettes[J]. Journal of Bacteriology, 2004, 186(5): 1503-1517. DOI:10.1128/JB.186.5.1503-1517.2004 |
| [33] |
Wang ZT, Zhang YB, Wang LY, Wei JC, Liu K, Shao DH, Li BB, Liu LH, Widén F, Ma ZY, et al. Comparative genomic analysis of Bordetella bronchiseptica isolates from the lungs of pigs with porcine respiratory disease complex (PRDC)[J]. Infection, Genetics and Evolution, 2020, 81: 104258. DOI:10.1016/j.meegid.2020.104258 |
| [34] |
Parkhill J, Sebaihia M, Preston A, Murphy LD, Thomson N, Harris DE, Holden MTG, Churcher CM, Bentley SD, Mungall KL, et al. Comparative analysis of the genome sequences of Bordetella pertussis, Bordetella parapertussis and Bordetella bronchiseptica[J]. Nature Genetics, 2003, 35(1): 32-40. DOI:10.1038/ng1227 |
 2021, Vol. 48
2021, Vol. 48




