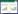扩展功能
文章信息
- 詹艺舒, 李婕, 褚秀丹, 蔡志英, 纪鹏伟, 陈炳智, 江玉姬
- ZHAN Yi-Shu, LI Jie, CHU Xiu-Dan, CAI Zhi-Ying, JI Peng-Wei, CHEN Bing-Zhi, JIANG Yu-Ji
- 一株真菌拮抗细菌Z21的筛选与鉴定及其发酵条件优化
- Screen, identification and fermentation optimization of an antifungal bacterium Z21
- 微生物学通报, 2020, 47(5): 1503-1514
- Microbiology China, 2020, 47(5): 1503-1514
- DOI: 10.13344/j.microbiol.china.190622
-
文章历史
- 收稿日期: 2019-07-29
- 接受日期: 2019-12-18
- 网络首发日期: 2020-01-06
2. 福建省龙海市农业局 福建 龙海 363101;
3. 漳州市新发生物科技有限公司 福建 漳州 363107;
4. 福建农林大学生命科学学院菌物研究中心 福建 福州 350002
2. Longhai Agricultural Bureau of Fujian Province, Longhai, Fujian 363101, China;
3. Zhangzhou XinFa Biotechnology Company Limited, Zhangzhou, Fujian 363107, China;
4. Center for Fungi Research, College of Life Sciences, Fujian Agriculture and Forestry University, Fuzhou, Fujian 350002, China
大量使用的化学农药和抗生素给食品安全和环境保护带来了巨大的压力,开发新型肽类、脂肽类抗生素在农业生产以及食品防腐保鲜中的应用越来越重要[1]。1945年Johnson等[2]首次发现枯草芽孢杆菌代谢产物具有抗菌功能,之后陆续有专家学者从芽孢杆菌属的细菌中分离出抗菌蛋白、抗菌肽等代谢产物[3]。芽孢杆菌属(Bacillus)具有高效、广谱、安全等特性,是目前研究较为成熟且应用较为广泛的重要生防微生物[4],其中以枯草芽孢杆菌(B. subtilis)、解淀粉芽孢杆菌(B. amyloliquefaciens)、地衣芽孢杆菌(B. licheniformis)以及短小芽孢杆菌(B. pumilus)的研究和应用最多[5-6]。
2010年,Madhaiyan等[7]首次从韩国传统种植的水稻根际土壤中分离得到一株新的芽孢杆菌,经过鉴定命名为甲基营养型芽孢杆菌(B. methylotrophicus)。在分类学上,甲基营养型芽孢杆菌属于厚壁菌门芽孢杆菌纲芽孢杆菌目芽孢杆菌科芽孢杆菌属,广泛分布于自然界中[8]。杨德昌等[9]从渤海海域海泥中分离到一株甲基营养型芽孢杆菌,证明其对于防治黄瓜、番茄、烟草的灰霉、苹果树腐烂病等多种真菌病害有很好的效果。魏新燕等[10]从沧州渤海海域分离得到一株甲基营养型芽孢杆菌BH21,研究表明该菌株的无菌发酵液对葡萄灰霉病菌有较强的抑制作用。吕倩等[11]从南海深海中分离得到一株具有较强抗真菌活性的细菌,鉴定为甲基营养型芽孢杆菌。尹向田等[12]在山东省葡萄研究院的实验室葡萄园根际土壤中分离得到一株菌,试验表明该菌株为甲基营养型芽孢杆菌。王松等[13]从浓香型白酒发酵糟培中分离到一株产细菌素的甲基营养型芽孢杆菌J2B-74,并对其产细菌素的发酵条件进行了优化。
本试验从空气中分离到一株对多种霉菌具有较强抑制作用的细菌Z21,通过16S rRNA基因序列分析、形态学特征、生理生化特征进行鉴定,确定其为甲基营养型芽孢杆菌;并对其抑菌效果进行探究,对其发酵条件进行了优化,为该菌株开发成天然的食品防腐剂提供参考。
1 材料与方法 1.1 材料 1.1.1 供试菌种供试真菌为康氏木霉(Trichoderma koningii)、绿色木霉(Trichoderma atroviride) ATCC 30153、赭绿青霉(Penicillium ochrochloron)、黑曲霉(Aspergillus niger)、易脆毛霉(Mucor fragilis) ATCC 3093、少根根霉(Rhizopus arrhizus),均为福建农林大学食品微生物实验室保藏。
1.1.2 培养基牛肉膏蛋白胨琼脂培养基(BPAD) (g/L):牛肉膏3.0,蛋白胨10.0,NaCl 5.0,琼脂15.0,pH 7.4−7.6;马铃薯葡萄糖琼脂培养基(PDA) (g/L):马铃薯200.0,葡萄糖20.0,琼脂15.0,pH 7.2−7.4;马铃薯液体培养基(PDL):马铃薯200.0 g/L,pH 7.2−7.4;缓冲蛋白胨水:蛋白胨10.0 g/L,pH 7.2−7.4。所有培养基1×105 Pa灭菌30 min,备用。
1.1.3 主要试剂和仪器可溶性淀粉、蔗糖、葡萄糖、果糖等分析纯试剂,国药化学试剂有限公司;PCR引物由生工生物工程(上海)股份有限公司合成。PCR仪,Bio-Rad公司;恒温生化培养箱,上海一恒实业有限公司。
1.2 方法 1.2.1 拮抗细菌的初筛拮抗菌的分离:将凝固好的BPDA培养基分别放置在室内和室外空气中暴露30 min,盖上盖子,28 ℃培养24 h。挑取不同菌落形态的细菌用平板划线法进行分离纯化,并保存于牛肉膏蛋白胨试管斜面供筛选。竹子内生菌由福建农林大学生命科学学院微生物实验室提供。
拮抗菌的初筛:采用平板对峙法,取一环细菌,在距离平板中央圆心左右各3 cm处分别划线接种细菌,28 ℃培养72 h,让细菌产生代谢产物并扩散,用无菌打孔器(直径8 mm)在已活化好的康氏木霉平板上打孔,菌块接入含有细菌的PDA平板中央点,28 ℃培养4 d后用游标卡尺分别测量细菌对康氏木霉的抑菌带宽度,筛选拮抗效果强的细菌,每个处理重复3皿。抑菌带宽度为霉菌菌落边缘到细菌菌苔边缘之间的距离(mm)。
1.2.2 拮抗细菌的复筛从初筛结果中选取一株抑制效果最好的细菌进行复筛,接种一环该细菌于PDL培养基中,28 ℃、130 r/min培养72 h后,4 500 r/min离心20 min,上清液过无菌滤膜(孔径0.22 μm),取其中0.2 mL滤液均匀涂布于PDA平板培养基,以等体积无菌水作为对照,在平板中央分别接入8 mm康氏木霉菌块,28 ℃培养4 d后测定菌丝的生长直径,每个处理重复3皿。霉菌菌落直径采用十字交叉法进行测量,并计算菌丝生长抑制率,其中抑制率(%)=[(对照霉菌菌落直径−处理霉菌菌落直径)/(对照霉菌菌落直径−菌块直径)]×100。
1.2.3 拮抗菌Z21的抑菌谱测定抑菌实验参照1.2.1步骤中方法,每种指示霉菌重复3皿,确定Z21的抑菌谱。
1.2.4 Z21的鉴定16S rRNA基因序列分析:利用细菌通用引物27F (5′-AGAGTTTGATCATGGCTCAG-3′)和1492F (5′-AAGGAGGTGATCCAACCGCA-3′)进行PCR扩增。PCR反应体系(30 μL):DNA模板1 μL,10×Buffer 3 μL,dNTPs (10 mmol/L) 2 μL,27F和1492R (10 μmol/L)各1 μL,rTaq酶(5 U/μL) 0.3 μL,ddH2O补足至30 μL。PCR反应条件:95 ℃ 3 min;95 ℃ 30 s,50 ℃ 30 s,72 ℃ 1.5 min,35个循环;72 ℃ 10 min。PCR扩增产物经1%琼脂糖凝胶电泳检测后送生工生物工程(上海)股份有限公司测序,测序后的拼接结果在NCBI上进行BLAST相似序列检索比对,采用Clustal软件和MEGA软件进行多序列同源性分析,并构建系统进化树。
形态学和生理生化实验:取0.1 mL菌液用100 mL无菌水稀释后涂布于BPDA培养基,37 ℃培养18 h,观察菌落形态、大小、边缘、表面、凹凸度、透明度等,并进行革兰氏染色、简单染色和芽孢染色,具体方法参考《常见细菌鉴定手册》[14]。生理生化实验步骤参照参考文献[14-15]。部分理化指标委托中国工业菌种保藏中心测定(Vitek上机测定)。
透射电镜观察:收集在BPDA培养基中培养18 h的拮抗菌进行固定、脱水,后用1%磷钨酸负染1 min前处理后上镜进行观察。
1.2.5 发酵条件优化(1) 种子液制备:挑取一环Z21接种于装有100 mL PDL培养基的三角瓶中,28 ℃、130 r/min培养18 h。
(2) 不同碳、氮源、金属离子对Z21发酵液抑菌活性的影响:以PDL培养基为对照,采用单因素试验法分别研究添加量为2% (质量体积比)的不同碳源(蔗糖,葡萄糖,可溶性淀粉,甘露醇,乳糖,果糖)、添加量为2% (质量体积比)的不同氮源(大豆蛋白胨,牛肉膏,酵母膏,硫酸铵,柠檬酸铵,NaNO3)、添加量为0.2% (质量体积比)的不同无机盐(NaCl,CaCl,FeSO4,MgSO4,K2HPO4,ZnSO4),以3%接种量接入各培养基,28 ℃、130 r/min培养72 h,按照1.2.2复筛中的方法计算菌丝生长抑制率。采用缓冲蛋白胨水将发酵液进行10倍系列稀释法计算细菌数,确定最佳碳、氮源和无机盐。
(3) 正交试验:根据上述结果,设计3因素4水平的正交试验(表 1)。
| 水平 Levels |
因素Factors | ||
| A Glucose (%) | B NaNO3 (%) | C MgSO4 (%) | |
| 1 | 1 | 2 | 0.20 |
| 2 | 2 | 3 | 0.30 |
| 3 | 3 | 4 | 0.40 |
(4) 发酵条件优化:采用最佳培养基,测定不同发酵条件对Z21生长以及发酵滤液对康氏木霉菌丝生长的抑菌效果。培养温度分别设计为20、28、32、40 ℃;培养时间分别为24、36、48、60、72、84、96 h,以确定最佳培养温度和时间。
2 结果与分析 2.1 拮抗菌的初筛结果空气中分离的细菌和竹子内生菌一共38株细菌经过多次的分离纯化后编号为Z1–Z38。其中有9株细菌对康氏木霉有很强的抑制作用,这些细菌对康氏木霉的拮抗实验结果见表 2。其中菌株Z21具有很强的抑制康氏木霉菌丝生长的作用,抑菌带宽度达到25.82±0.66 mm,比另外8株细菌的抑制效果强,差异显著,并且经过连续多次传代后抑菌效果依然稳定,所以对菌株Z21进行进一步的研究。
| 供试菌株 Test strains |
重复1 Repeat 1 |
重复2 Repeat 2 |
重复3 Repeat 3 |
平均值 Average value |
| CK | 0 | 0 | 0 | 0.00±0.00 |
| Z21 | 25.05 | 25.55 | 26.85 | 25.82±0.66a |
| Z20 | 21.25 | 22.45 | 23.89 | 22.53±0.93b |
| Z34 | 20.34 | 22.44 | 22.38 | 21.72±0.85c |
| Z32 | 17.55 | 18.31 | 17.88 | 17.91±0.27d |
| Z13 | 17.76 | 15.00 | 15.95 | 16.24±0.99de |
| Z15 | 14.55 | 15.95 | 16.35 | 15.62±0.67e |
| Z3 | 6.05 | 7.09 | 7.99 | 7.04±0.69f |
| Z4 | 6.78 | 8.05 | 7.56 | 7.46±0.45f |
| Z8 | 5.55 | 6.75 | 6.88 | 6.39±0.52f |
| 注:数据后不同小写字母表示在P < 0.05水平差异显著.
Note: Significant difference at P < 0.05 level was reflected in different lowercase letters following the figures. |
||||
从表 3和图 1可以看出,Z21的发酵滤液对康氏木霉具有很强的抑制作用,菌丝生长抑制率达到42.83%。说明Z21在发酵过程中产生具有抑菌效果的活性物质,并分泌至发酵液中,而且抑菌效果稳定。
| 试验号Test No. | CK | Z21 |
| 1 | 76.96 | 48.43 |
| 2 | 78.07 | 47.23 |
| 3 | 80.28 | 49.16 |
| 平均值Average value (mm) | 78.44±1.69 | 48.27±0.98 |
| 抑制率Inhibition rate (%) | − | 42.83 |
| 注:−:没有抑制.
Note: −: No inhibition. |
||

|
| 图 1 Z21发酵滤液对康氏木霉的抑菌效果 Figure 1 Inhibition effect of Z21 fermentation fitrate on T. koningii 注:A:对照组;B:处理组. Note: A: Control group; B: Treatment group. |
|
|
从图 2可以看出,Z21除了对康氏木霉具有很强的抑制效果外,对食品中常见的黑曲霉、少根根霉、赭绿青霉、易脆毛霉、绿色木霉均具有一定的抑制效果。与对照组相比,康氏木霉在含有Z21的平板上其菌丝生长明显受到抑制,在Z21和康氏木霉之间有一条明显的透明带,即抑菌带。从表 4可以看出,Z21的抑菌谱较广、抑菌能力较强,对食品中常见的少根根霉、赭绿青霉、易脆毛霉、绿色木霉、康氏木霉、黑曲霉都具有很好的菌抑制效果。其中,对康氏木霉和黑曲霉抑制效果最好,抑菌带宽度分别达到了24.13±1.06 mm和18.80±0.23 mm,对绿色木霉和易脆毛霉的抑制效果次之,抑菌带宽度为16.39±0.55 mm和14.39±0.69 mm,对少根根霉、赭绿青霉也有一定的抑制效果。从图 2和表 4可知:Z21对许多真菌生长具有较强的抑制作用,可开发成食品天然防腐剂,具有潜在的应用价值。
|
| 图 2 Z21的抑菌谱 Figure 2 Antibacterial spectrum of Z21 注:A–F:赭绿青霉、易脆毛霉、康氏木霉、少根根霉、绿色木霉、黑曲霉. Note: A–F: Penicillium versicolor, Mucor fragile, Trichoderma koningii, Rhizopus fuligrum, Trichoderma viride, Aspergillus niger. |
|
|
| 指示霉菌 Indicating mold |
重复1 Repeat 1 |
重复2 Repeat 2 |
重复3 Repeat 3 |
平均值 Average value |
| Trichoderma koningii | 24.67 | 22.91 | 24.82 | 24.13±1.06a |
| Aspergillus niger | 18.58 | 18.79 | 19.04 | 18.80±0.23b |
| Penicillium ochrochloron | 6.33 | 6.35 | 6.05 | 6.24±0.17e |
| Trichoderma atroviride | 16.49 | 16.88 | 15.80 | 16.39±0.55c |
| Mucor fragilis | 13.59 | 14.80 | 14.78 | 14.39±0.69d |
| Rhizopus arrhizus | 2.02 | 2.21 | 2.02 | 2.08±0.11f |
| 注:数据后不同小写字母表示在P < 0.05水平差异显著.
Note: Significant difference at P < 0.05 level was reflected in different lowercase letters following the figures. |
||||
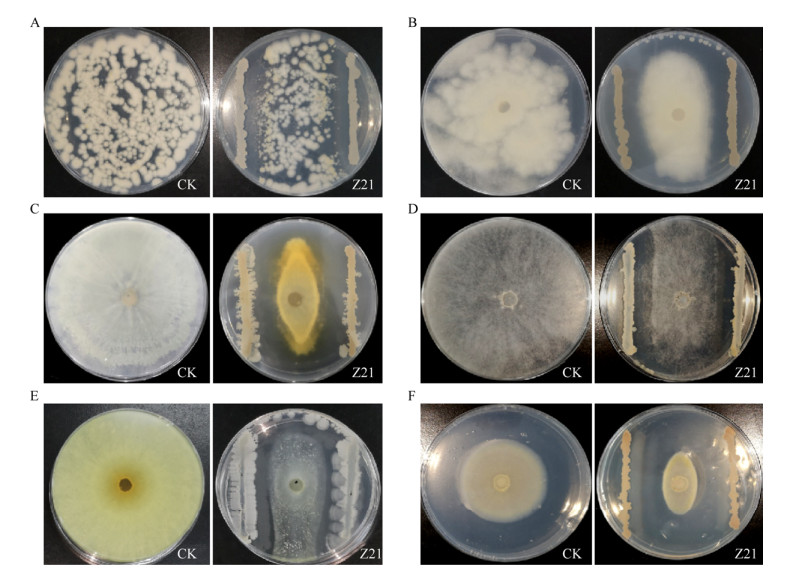
16S rRNA基因PCR产物电泳结果(图 3)显示,PCR产物约为1.8 kb,符合常规的16S rRNA基因序列长度。
|
| 图 3 Z21 16S rRNA基因PCR产物的琼脂糖凝胶电泳 Figure 3 Agarose gel electrophoresis of 16S rRNA gene PCR product of Z21 Note: M: DL2000 DNA Marker: 1, 2: Z21. |
|
|
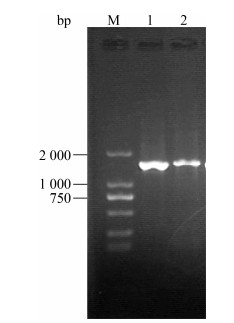
测序所得16S rRNA基因碱基序列已提交GenBank (登录号:MN 240443),并在NCBI数据库上进行BLAST比对,发现Z21与Bacillus methylotrophicus strain CBMB205T (NR16240.1)相似性最高,为99.69%。分析显示Z21与B. methylotrophicus strain CBMB205T (NR16240.1)聚在同一系统分支上(图 4)。因此,初步鉴定Z21为甲基营养型芽孢杆菌(Bacillus methylotrophicus)。
|
| 图 4 基于16S rRNA基因序列构建的Z21及相关菌株系统发育树 Figure 4 Phylogenetic tree of Z21 and other related strains based on 16S rRNA gene sequence 注:Bootstrap次数设置为1 000,邻接法构建系统发育树;括号内代表序列GenBank登录号;分支处的数字表示Bootstrap支持率;标尺表示0.5%的序列进化差异. Note: The number at branch nodes are the percentage bootstrap support based on neighbor-joining analysis of 1 000 resample data sets. Numbers in parentheses are GenBank accession number. The numbers in each branch point denote the percentages supported by bootstrap. The scale presents 0.5% sequence variance. |
|
|
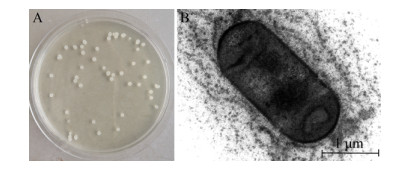
由图 5可以看出,Z21在PDBA培养基上于37 ℃培养18 h后,菌落直径约3.1−3.9 mm,呈淡黄色,圆形,微微隆起,不透明,边缘整齐,质地粘稠,3 d后菌落表面会出现皱褶。Z21革兰氏染色阳性,有荚膜和芽孢,芽孢圆形。透射电镜观察显示Z21体呈杆状(图 5),两端钝圆,大小为(0.8−1.0)×(1.8−2.4) μm,周生鞭毛。
|
| 图 5 Z21的菌落(A)及扫描电镜形态(B) Figure 5 Colony (A) and scanning electron morphology (B) of Z21 |
|
|
Z21的主要生理生化特征见表 5。由表 5可知,Z21好氧,接触酶、明胶水解、脲酶、吲哚产生、淀粉水解、硝酸盐还原、β-木糖苷酶、苯丙氨酸芳胺酶、丙酮酸盐、L-吡咯烷酮芳胺酶、α-葡萄糖苷酶、β-葡糖苷酶、竹桃霉素耐药、七叶苷水解、多粘菌素B耐药、α-半乳糖苷酶、丙氨酸芳胺酶、丙氨酸-苯丙氨酸-脯氨酸芳胺酶、甲基-α-D-吡喃葡萄糖苷酸化和甘氨酸芳胺酶均为阳性,能利用较多种糖类进行发酵。从表 5中可以看出,当pH低于3.0时Z21不生长,生长的pH范围为5.0−9.0;当温度低于4 ℃和高于55 ℃时,Z21不生长,生长温度范围为20−45 ℃;盐耐受范围小于7% (质量体积比)。与参考文献[4, 7, 11]对比,Z21的这些生理生化特征与甲基营养型芽孢杆菌的生理生化特征和生物学特性相符。综合形态特征、生理生化特征以及16S rRNA基因序列分析,基本确定Z21属于甲基营养型芽孢杆菌(B. methylotrophicus)。
| 项目 Items |
结果 Results |
| Oxygen | + |
| Glucose | + |
| Lactose | + |
| Methyl red | − |
| Voges-Proskauer test | − |
| Nitrate utilization | + |
| Indole production | − |
| H2S | − |
| Gelatin | + |
| Citrate utilization | − |
| Oxidase | + |
| Catalase | + |
| Urease | + |
| Starch | + |
| β-xylosidase | + |
| L-lysine arylamine enzyme | − |
| L-aspartate arylamine enzyme | − |
| Leucine arylaminese | − |
| Phenylalanine arylaminese | + |
| L-proline arylamine enzyme | − |
| α-galactosidase | + |
| Alanine arylaminese | + |
| Tyrosine arylase | − |
| β-N-acetylglucosidase | − |
| Alanine-phenylalanine-proline arylamine enzyme | + |
| Cyclodextrin | − |
| D-galactose | − |
| Glycogen | + |
| Inositol | + |
| Methyl-α-D-glucopyranylation | + |
| Ellman | − |
| Methyl-D-xylosin | − |
| α-mannosidase | − |
| Maltotriose | + |
| Glycine arylaminese | + |
| D-mannitol | + |
| D-mannose | + |
| D-melose | − |
| N-acetyl-D-glucosamine | − |
| Ancient sugar | + |
| β-mannosidase | − |
| L-pyrrolidone arylamine enzyme | + |
| Phosphorylcholine | − |
| Pyruvate | + |
| α-glucosidase | + |
| D-tagatose | − |
| Inulin | − |
| D-ribose | − |
| Putrescine assimilation | − |
| L-rhamnose | − |
| β-glucosidase | + |
| D-trehalose | + |
| Ambomycin resistance | + |
| Aescin hydrolysis | + |
| Red tetrazolium | + |
| Polymyxin B resistance | + |
| Kanamycin resistance | − |
| Temperature (℃) | 20−45 |
| pH | 5.0−9.0 |
| NaCl concentration | < 7% |
| 注:+:阳性;−:阴性.
Note: +: Positive; −: Negative. |
|
Z21利用6种不同碳源发酵获得的发酵液(无菌)对康氏木霉有一定的抑制作用(图 6),其中葡萄糖作为碳源的发酵液抑菌率最高为58.56%,显著高于其他碳源。乳糖、蔗糖稍差,果糖、甘露醇、可溶性淀粉和对照组无显著性差异,抑菌效果不理想。葡萄糖作为碳源时Z21数量为8.35 lgCFU/mL,高于其他碳源。从图 6中可以看出,添加不同碳源对细菌生长的数量影响较小,只有乳糖为碳源时,Z21的生长数量明显较少。但碳源对抑菌率的影响较大,可能是抑菌物质的合成与碳源物质有关系,因此葡萄糖是液体发酵培养基的最佳碳源。

|
| 图 6 不同碳源对Z21的生长和发酵液抑菌活性的影响 Figure 6 Effects of different carbon sources on the growth and inhibition activity of submerged cultured of Z21 注:不同小写字母表示在P < 0.05水平差异显著. Note: Significant difference at P < 0.05 level was reflected in different lowercase. |
|
|
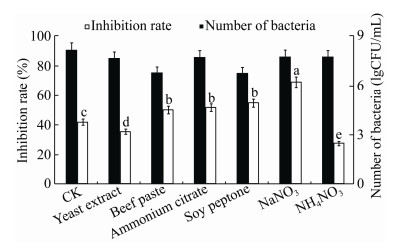
6种氮源发酵液均对木霉菌丝生长有一定的抑制作用(图 7),其中抑菌效果较好的是无机氮源NaNO3,抑菌率为69.31%,显著高于其他氮源。在NaNO3中Z21数量不是最高,比不添加氮源组低,为7.77 lgCFU/mL,添加牛肉膏和大豆蛋白胨对Z21的生长有一定的抑制,说明Z21生长不必外加氮源。从图 7可知,不同的氮源对抑菌效果有明显的影响,说明添加不同氮源对抑菌物质的产生会有较大影响。
|
| 图 7 不同氮源对Z21的生长和发酵液抑菌活性的影响 Figure 7 Effects of different nitrogen sources on the growth and inhibition activity of submerged cultured of Z21 注:不同小写字母表示在P < 0.05水平差异显著. Note: Significant difference at P < 0.05 level was reflected in different lowercase letters. |
|
|
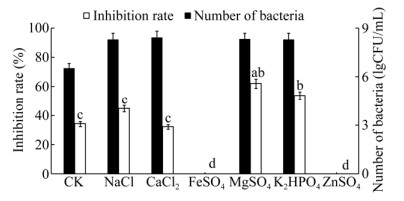
6种不同无机盐发酵液对康氏木霉的抑制作用差异较大(图 8),其中添加了MgSO4的发酵液抑菌率最高,为62.12%,显著高于其他无机盐。拮抗菌Z21在几种无机盐的培养基中生长有显著差异,在FeSO4和ZnSO4的发酵培养基上Z21无法生长,并且对康氏木霉完全没有抑制作用。NaCl、CaCl、MgSO4、K2HPO4对细菌的生长没有很大的影响,但是对康氏木霉的抑制效果有很明显的差异,这可能与抑菌物质的结构或代谢途径有关,有待进一步深入研究。
|
| 图 8 不同无机盐对Z21的生长和发酵液抑菌活性的影响 Figure 8 Effects of different inorganic salt on the growth and inhibition activity of submerged cultured of Z21 注:不同小写字母表示在P < 0.05水平差异显著. Note: Significant difference at P < 0.05 level was reflected in different lowercase letters. |
|
|
根据碳源、氮源以及无机盐的单因素试验结果,选择葡萄糖(A)、NaNO3 (B)、MgSO4 (C) 3个因素进行3因素4水平正交试验(表 6)。因为之前的实验结果显示,在添加不同碳源、氮源和无机盐的培养基中Z21生长无显著性差异,因此正交试验只以抑菌活性为指标,确定最优发酵培养基的配方。正交试验结果表明,3个因素对康氏木霉抑制率的影响顺序为B > C > A,最佳水平组合为A2B1C2,方差分析表明B因素对康氏木霉抑制率的影响显著高于其他几个因素,验证实验证明此组合的抑菌率高于其他组,达到74.06%。综合结果,最佳组合为A2B1C2,即1 L发酵培养基中含葡萄糖20.0 g、NaNO3 20.0 g、MgSO4 3.0 g。
| 试验号 | Glucose | NaNO3 | MgSO4 | Empty | 抑菌率 |
| Test No. | (A) | (B) | (C) | column | Inhibition |
| (D) | rate (%) | ||||
| 1 | 1 | 1 | 1 | 1 | 62.40 |
| 2 | 1 | 2 | 2 | 2 | 67.91 |
| 3 | 1 | 3 | 3 | 3 | 56.83 |
| 4 | 2 | 1 | 2 | 3 | 74.06 |
| 5 | 2 | 2 | 3 | 1 | 66.44 |
| 6 | 2 | 3 | 1 | 2 | 58.56 |
| 7 | 3 | 1 | 3 | 2 | 68.15 |
| 8 | 3 | 2 | 1 | 3 | 65.11 |
| 9 | 3 | 3 | 2 | 1 | 61.34 |
| K1j | 187.14 | 204.6 | 186.06 | 190.17 | |
| K2j | 199.05 | 199.47 | 203.31 | 194.61 | |
| K3j | 194.61 | 176.73 | 191.43 | 195.99 | |
| K1J | 62.38 | 68.2 | 62.02 | 63.39 | |
| K2J | 66.35 | 66.49 | 67.77 | 64.87 | |
| K3J | 64.87 | 58.91 | 63.81 | 65.33 | |
| Rj | 3.97 | 9.29 | 5.75 | 1.94 | |
| 最优方案 Optimum parameters |
A2B1C2 | ||||
采用上述最佳发酵培养基配方,对发酵条件进行优化。从图 9可以看出温度对抑菌效果的影响很大,随着温度升高,抑菌率先增大后减小,其中32 ℃的发酵液抑菌率最高,达到78.13%;当温度为20 ℃时抑菌效果最差,可能是因为此时细菌生长缓慢,代谢产物生产少;28 ℃时,虽然细菌数量较多,但产生的代谢物较少;36 ℃时,细菌生长受到影响,抑菌活性也较弱,说明温度对抑菌物质的产生有较大的影响。在最佳发酵温度的基础上对发酵时间进行研究,从图 10可以看出,抑菌率随培养时间的延长先增大后减小,发酵48 h时达到最高,为86.21%,随后抑菌率开始下降。从细菌数量分析,24 h时细菌数最高但抑菌率最低,可能是因为此时抑菌物质产生较少,随后细菌的数量呈现稳定,但抑菌率明显下降了,可能后期培养液环境会影响细菌抑菌物质的活性,或抑菌物质在后期被分解。以Z21抑菌率为指标,参考Z21的生长速度,确定最优的发酵条件为培养温度为32 ℃、培养时间为48 h,此条件下抑菌活性最高,比优化前抑菌率提高了43.38%。

|
| 图 9 不同温度对Z21的生长和发酵液抑菌活性的影响 Figure 9 Effect of different temperature on growth and inhibition activity of submerged cultured of Z21 注:不同小写字母表示在P < 0.05水平差异显著. Note: Significant difference at P < 0.05 level was reflected in different lowercase letters. |
|
|

|
| 图 10 不同时间对Z21的生长和发酵液抑菌活性的影响 Figure 10 Effect of different time on growth and inhibition activity of submerged cultured of Z21 注:不同小写字母表示在P < 0.05水平差异显著. Note: Significant difference at P < 0.05 level was reflected in different lowercase letters. |
|
|
甲基营养型芽孢杆菌是芽孢杆菌属的一个新种,对人、畜及环境安全,因此,其作为芽孢杆菌属的“后起之秀”,被应用于环境保护、植保、园艺、食品防腐等各行业中[16]。本试验综合了细菌的16S rRNA基因序列、生理生化特征和形态学特征,确定Z21为甲基营养型芽孢杆菌(B. methylotrophicus)。随后对培养基和发酵条件进行优化,经过优化的无菌发酵液其抑菌率比未优化前提高了43.38%,对康氏木霉生长的抑菌率达到了86.21%,优化效果非常明显,对甲基营养型芽孢杆菌在抑菌条件优化方面提供了一定的借鉴。
木霉、黑曲霉、青霉、根霉以及毛霉是粮食贮藏中主要的风险因素,产生发热霉变,加快粮食有机物的消耗,造成粮食腐败发霉。吴红萍等[17]和李新社等[18]针对海南和湖南等地的粮库调查发现根霉、青霉、木霉、毛霉和曲霉等真菌为优势菌。本实验筛选得到的甲基营养型芽孢杆菌Z21具有广谱的抑菌效果,尤其对木霉、黑曲霉和毛霉的抑菌效果非常好,抑菌带清晰,最大宽度达到24.13±1.06 mm (细菌与真菌接种位置距离为30 mm)。同时,甲基营养型芽孢杆菌在抑制植物病原菌方面的研究比较多[4, 10]且已经应用于生产[9],广泛用于田间治理黄瓜灰霉病等植物病害,是安全的菌种,但是该菌应用在粮食储藏方面的研究比较少[19]。王燕等[20]筛选得到一株具有降解黄曲霉毒素AFB1的甲基芽孢杆菌WZ-4,有望开发成新的微生物新型饲料和食品添加剂。本文研究结果为甲基营养型芽孢杆菌开发成食品防腐剂等方面利用提供一定的参考。
芽孢杆菌属细菌的抑菌机理主要是通过分泌一些次生代谢产物来抑制病原菌的生长[21]。Babad等首次从枯草芽孢杆菌培养液中分离出抗真菌肽[22]。吴燕燕等[23]研究发现,使用甲基营养型芽孢杆菌中抗菌肽对罗非鱼片进行保鲜,结果表明抗菌肽具有很好的保鲜防腐效果,明显延长了罗非鱼片的保鲜时间。Sharma等[24]从孟加拉拉杰沙希大学土壤中分离得到一株甲基营养型芽孢杆菌(Bacillus methylotrophicus-SCS2012),并发现其粗提物对痢疾志贺氏菌、大肠杆菌、蜡状芽孢杆菌、无乳链球菌等食品中常见的细菌具有很好的抑制效果。因此,甲基营养型芽孢杆菌不仅具有广谱的杀菌抑菌效果,而且对人、环境较安全,是开发新活性物质的一类有益菌[4]。本文的研究结果为Z21活性物质的分离鉴定以及开发为天然品防腐剂应用提供了参考。
| [1] |
Bale JS, van Lenteren JC, Bigler F. Biological control and sustainable food production[J]. Philosophical Transactions of the Royal Society B: Biological Sciences, 2008, 363(1492): 761-776. DOI:10.1098/rstb.2007.2182 |
| [2] |
Johnson BA, Anker HS, Meleney FL. Bacitracin: a new antibiotic produced by a member of the B. subtilis group[J]. Science, 1945, 102(2650): 376-377. DOI:10.1126/science.102.2650.376 |
| [3] |
Hu YH, Chen W, Liu YZ, et al. Production and Application of Probiotic Bacillus[M]. Beijing: Chemical Industry Press, 2015: 176-191. (in Chinese) 胡永红, 陈卫, 刘邮洲, 等. 益生菌芽孢杆菌生产与应用[M]. 北京: 化学工业出版社, 2015: 176-191. |
| [4] |
Zhou DB, Chen YF, Jing T, et al. Identification and colonization of Bacillus methylotrophicus against banana Fusarium wilt disease[J]. Chinese Agricultural Science Bulletin, 2017, 33(36): 145-151. (in Chinese) 周登博, 陈宇丰, 井涛, 等. 抗香蕉枯萎病甲基营养型芽孢杆菌的鉴定及定殖[J]. 中国农学通报, 2017, 33(36): 145-151. DOI:10.11924/j.issn.1000-6850.casb17090141 |
| [5] |
Zhang B. Purification, identification and machanism of action of lipopeptide antibiotic bacillomycin L produced by Bacillus amyloliquefaciens[D]. Beijing: Doctoral Dissertation of China Agricultural University, 2014 (in Chinese) 张宝.解淀粉芽孢杆菌抗菌脂肽bacillomycin L的纯化鉴定及抑菌机理研究[D].北京: 中国农业大学博士学位论文, 2014 |
| [6] |
Wang J, Cao JM, Chen DX, et al. Antimicrobial effect and components analysis of volatile organic compounds from Bacillus pumilus AR03[J]. Scientia Agricultura Sinica, 2018, 51(10): 1908-1919. (in Chinese) 王静, 曹建敏, 陈德鑫, 等. 短小芽孢杆菌AR03挥发性有机物的抑菌活性及其组分分析[J]. 中国农业科学, 2018, 51(10): 1908-1919. DOI:10.3864/j.issn.0578-1752.2018.10.010 |
| [7] |
Madhaiyan M, Poonguzhali S, Kwon SW, et al. Bacillus methylotrophicus sp. nov., a methanol-utilizing, plant-growth-promoting bacterium isolated from rice rhizosphere soil[J]. International Journal of Systematic and Evolutionary Microbiology, 2010, 60(10): 2490-2495. DOI:10.1099/ijs.0.015487-0 |
| [8] |
Liu B, Tao TS, Wang JP, et al. Bacillus (Volume Ⅱ): Taxonony of Bacollus[M]. Beijing: Science Press, 2016: 383-384. (in Chinese) 刘波, 陶天申, 王阶平, 等. 芽胞杆菌(第2卷):芽胞杆菌分类学[M]. 北京: 科学出版社, 2016: 380-384. |
| [9] |
Yang DC, Li XH, Hu JC, et al. A methylotrophic Bacillus wettable powder and its preparation method and application: CN, CN104222076A[P]. 2014-12-24 (in Chinese) 杨德昌, 李学红, 胡江春, 等.一种甲基营养型芽孢杆菌可湿性粉剂及其制备方法和应用: 中国, CN104222076A[P]. 2014-12-24 |
| [10] |
Wei XY, Huang YY, Huang YL, et al. Antagonism of Bacillus methylotrophicus strain BH21 to Botrytis cinerea[J]. Scientia Agricultura Sinica, 2018, 51(5): 883-892. (in Chinese) 魏新燕, 黄媛媛, 黄亚丽, 等. 甲基营养型芽孢杆菌BH21对葡萄灰霉病菌的拮抗作用[J]. 中国农业科学, 2018, 51(5): 883-892. |
| [11] |
Lü Q, Hu JC, Wang N, et al. Anti-fungal Lipopeptides produced by Bacillus methylotrophicus SHB114 isolated from south China sea[J]. Chinese Journal of Biological Control, 2014, 30(1): 113-120. (in Chinese) 吕倩, 胡江春, 王楠, 等. 南海深海甲基营养型芽孢杆菌SHB114抗真菌脂肽活性产物的研究[J]. 中国生物防治学报, 2014, 30(1): 113-120. |
| [12] |
Yin XT, Yang Y. Optimization of fermentation conditions for antibacterial active substances produced by Bacillus methylotrophicus GSBM05[J]. Jiangsu Agricultural Sciences, 2018, 46(20): 89-93. (in Chinese) 尹向田, 杨阳. 甲基营养型芽孢杆菌GSBM05产抗菌活性物质发酵条件优化[J]. 江苏农业科学, 2018, 46(20): 89-93. |
| [13] |
Wang S, You L, Chen J, et al. Optimization of fermentation conditions of Bacillus methylotrophicus J2B-74 for bacteriocin production by response surface methodology[J]. China Brewing, 2017, 36(6): 42-46. (in Chinese) 王松, 游玲, 陈杰, 等. 响应面法优化甲基营养型芽孢杆菌J2B-74代谢产细菌素的发酵条件[J]. 中国酿造, 2017, 36(6): 42-46. |
| [14] |
Dong XZ, Cai MY. Common Bacterial System Identification Manual[M]. Beijing: Science Press, 2001: 166-171. (in Chinese) 东秀珠, 蔡妙英. 常见细菌系统鉴定手册[M]. 北京: 科学出版社, 2001: 166-171. |
| [15] |
Zhao B, He SJ. Microbiology Experiment[M]. Beijing: Science Press, 2002: 26-120. (in Chinese) 赵斌, 何绍江. 微生物学实验[M]. 北京: 科学出版社, 2002: 26-120. |
| [16] |
Zhang MY, Yun TY, Zhou DB, et al. Research advances on Bacillus methylotrophicus[J]. Chinese Journal of Tropical Agriculture, 2017, 37(9): 66-71. (in Chinese) 张妙宜, 云天艳, 周登博, 等. 甲基营养型芽胞杆菌的研究进展[J]. 热带农业科学, 2017, 37(9): 66-71. |
| [17] |
Wu HP, Zhai SB, Du CH, et al. Diversity of fungi in stored rice in Hainan province[J]. Guizhou Agricultural Sciences, 2015, 43(4): 138-141. (in Chinese) 吴红萍, 翟世博, 杜晨辉, 等. 海南省储粮稻谷的霉菌多样性分析[J]. 贵州农业科学, 2015, 43(4): 138-141. DOI:10.3969/j.issn.1001-3601.2015.04.034 |
| [18] |
Li XS, Lu BS. Study on the contamination of mould in paddy stored in barn[J]. Journal of Changde Teachers University (Natural Science Edition), 2000, 12(2): 75-77. (in Chinese) 李新社, 陆步诗. 仓储稻谷霉菌污染情况调查[J]. 常德师范学院学报:自然科学版, 2000, 12(2): 75-77. |
| [19] |
Wang K. Research on screening and identification of biological control bacteria against aflatoxins and mechanism of strain JPP1for biocontrol[D]. Harbin: Doctoral Dissertation of Harbin Institute of Technology, 2013 (in Chinese) 王凯.黄曲霉生防菌的筛选鉴定及高效菌株JPP1的生防机制[D].哈尔滨: 哈尔滨工业大学博士学位论文, 2013 |
| [20] |
Wang Y, Zhang ML, Mao Y, et al. Isolation and identification of an aflatoxin B1 degradation bacterial strain and optimization of its culture conditions[J]. Journal of Henan Agricultural Sciences, 2015, 44(4): 139-143. (in Chinese) 王燕, 张美丽, 毛勇, 等. 黄曲霉毒素B1降解菌的分离鉴定及培养条件优化[J]. 河南农业科学, 2015, 44(4): 139-143. |
| [21] |
Leclère V, Marti R, Béchet M, et al. The lipopeptides mycosubtilin and surfactin enhance spreading of Bacillus subtilis strains by their surface-active properties[J]. Archives of Microbiology, 2006, 186(6): 475-483. DOI:10.1007/s00203-006-0163-z |
| [22] |
Babad J, Pinsky A, Turner-Graff R, et al. An antifungal polypeptide produced by Bacillus subtilis[J]. Nature, 1952, 170(4328): 618-619. DOI:10.1038/170618a0 |
| [23] |
Wu YY, Zhang Y, Li LH, et al. Study on fresh-keeping effect of antimicrobial peptides from Bacillus methylotrophilus in Tilapia fillet preservation[J]. Science and Technology of Food Industry, 2013, 34(2): 315-318. (in Chinese) 吴燕燕, 张岩, 李来好, 等. 甲基营养型芽孢杆菌抗菌肽对罗非鱼片保鲜效果的研究[J]. 食品工业科技, 2013, 34(2): 315-318. |
| [24] |
Sharma SCD, Shovon MS, Jahan MGS, et al. Antibacterial and cytotoxic activity of Bacillus methylotrophicus-Scs2012 isolated from soil[J]. Journal of Microbiology, Biotechnology and Food Sciences, 2013, 2(4): 2293-2307. |
 2020, Vol. 47
2020, Vol. 47