扩展功能
文章信息
- 赵立君, 刘云根, 王妍, 赵蓉, 任伟, 徐鸣洲
- ZHAO Li-Jun, LIU Yun-Gen, WANG Yan, ZHAO Rong, REN Wei, XU Ming-Zhou
- 典型高原湖滨带底泥细菌群落结构及多样性特征
- Bacterial community structure and diversity of sediments in a typical plateau lakeshore
- 微生物学通报, 2020, 47(2): 401-410
- Microbiology China, 2020, 47(2): 401-410
- DOI: 10.13344/j.microbiol.china.190270
-
文章历史
- 收稿日期: 2019-03-31
- 接受日期: 2019-09-24
- 网络首发日期: 2019-10-17
2. 西南林业大学生态与环境学院 云南 昆明 650224
2. College of Ecology and Environment, Southwest Forestry University, Kunming, Yunnan 650224, China
近年来,随着环境资源不断开发利用,含氮、磷等污染物大量排入湖泊、河流等,使湖泊水体的营养负荷持续增加,导致一些国家和地区的湖泊面临着水体富营养化的威胁[1],如非洲的Victoria[2]、加拿大的Erie[3]等湖泊。2007–2010年,杨桂山等[4]研究了中国的138个湖泊的营养盐状况,发现有85.4%的湖泊处于富营养状态,其中面临着重度富营养化危险的湖泊有40.1%,严重影响了附近区域的湖泊生态健康。富营养化水体的有效防治成为亟需解决的环境问题。
湖滨带是湖泊天然的保护屏障,对于氮、磷等污染物具有拦截、净化等作用,是健康湖泊生态系统的重要组成部分和评价指标[5]。湖泊底泥是湖滨生态系统中最活跃和最有影响的组成部分,与水体富营养化密切相关。在湖泊水体-底泥系统中,底泥作为水体的养分库和污染物迁移转化的载体,成为物质的蓄积库[6],与水体不断进行物质和能量交换。细菌是受环境影响最为敏感的生物类群之一,也是湖滨生态系统中的重要组成部分,影响整个湖滨生态系统的物质循环和营养传递过程[7]。底泥细菌群落通过驱动水体和底泥的物质能量循环来调控营养物质的储存、分布,对水体营养水平的调节有重要作用[8]。
目前,对不同区域湖泊的富营养演化过程已有大量研究[9-10],但针对高原湖泊湖滨带底泥细菌群落及与水体富营养化程度的响应关系鲜有研究。阳宗海4个湖滨带中东岸、西岸、北岸湖滨带退化严重,仅南岸湖滨带保存较为完整,具有研究价值[11]。本研究以阳宗海南岸湖滨带为研究对象,利用16S rRNA基因高通量测序技术,对阳宗海南岸不同区域底泥细菌群落结构及多样性进行分析,旨在揭示阳宗海湖滨带底泥细菌群落特征与水体富营养化之间的联系,为高原湖泊的富营养化防治提供借鉴。
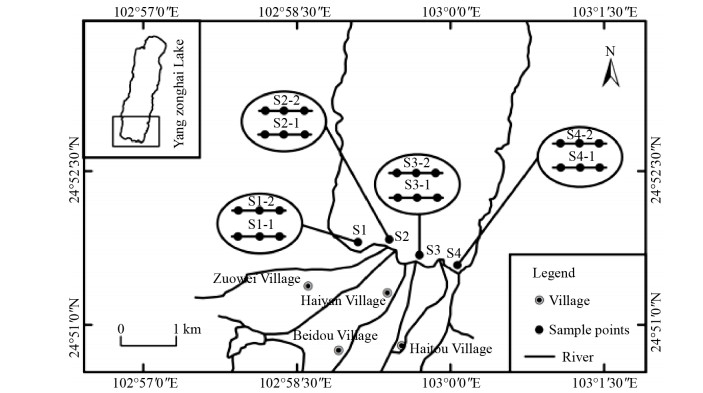
1 材料与方法 1.1 样品采集与处理采样点位置如图 1所示,2017年7月下旬,于阳宗海南岸选取4组区域湖滨带采样,分别为:S1样带,周边无外源河流汇入,有少量村落;S2样带,入湖河流经过阳宗海湿地公园汇入,该区域表层底泥较软,颜色呈黄褐色;S3样带为阳宗大河入湖附近,伴随大量的生活污水汇入阳宗海,底泥表层为颜色青灰色的淤泥;S4样带周边为高速公路无人口聚集,底泥表层为黄棕色沙质土壤。每条样带另设距湖岸5 m的近岸点(S-1)和距湖岸约15 m的远岸点(S-2)。使用全球定位系统GPS (佳明GPS72)定位。使用有机玻璃采水器采集1 L水样于样品瓶中,用柱状底泥采样器同步采集湖泊表层(1-10 cm)底泥样品,每个样点采集3个平行水样与底泥样品,水样存放在有冰袋的泡沫箱,回实验室后立即检测,底泥样品用无菌的聚乙烯薄膜自封袋包装,存放在有干冰的泡沫箱后放入-80 ℃冰箱保存,待测。
|
| 图 1 采样点分布 Figure 1 Sketch of the sampling positions |
|
|
水样测定指标:化学需氧量(chemical oxygen demand,COD)、总磷(total phosphorus,TP)、总氮(total nitrogen,TN)、叶绿素a (chlorophylla,Chla)。COD采用重铬酸盐法测定(HJ 828-2017);TP采用钼酸铵分光光度法测定(GB 11893-1989);TN采用过硫酸钾消解紫外分光光度法测定(HJ 636-2012);Chla采用分光光度法测定(HJ 897-2017)。
采用综合营养状态指数法评价阳宗海湖滨带富营养化程度。
综合营养状态指数计算公式:
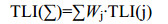
|
式中:TLI(∑)为综合营养状态指数;Wj为第j种参数的营养状态指数的相关权重。TLI(j)为代表第j种参数的营养状态指数。
采用0–100的一系列连续数字对湖泊(水库)营养状态进行分级:
TLI(∑) < 30贫营养(oligotropher);
30≤TLI(∑)≤50中营养(mesotropher);
TLI(∑) > 50富营养(eutropher);
50 < TLI(∑)≤60轻度富营养(light eutropher);
60 < TLI(∑)≤70中度富营养(middle eutropher);
TLI(∑) > 70重度富营养(hyper eutropher)。
1.3 主要试剂和仪器FastDNA Spin Kit for Soil DNA提取试剂盒,MPbio公司;建库试剂盒TruSeq™ DNA Sample Prep Kit,Illumina公司。PCR仪,Promega公司;MiSeq PE300测序平台,Illumina公司。
1.4 样品16S rRNA基因测序底泥16S rRNA基因测序委托上海美吉生物信息科技有限公司完成,以FastDNA Spin Kit for Soil DNA提取试剂盒对样本的基因组DNA进行提取。选择V3-V4可变区,使用338F (5′-ACTCCTAC GGGAGGCAGCAG-3′)/806R (5′-GGACTACHVGG GTWTCTAAT-3′)引物和高效高保真酶进行PCR[12],确保扩增效率和准确性。使用TruSeq™ DNA Sample Prep Kit进行文库构建,构建好的文库经过QuantiFluor™-ST定量,文库合格后使用MiSeq PE300进行上机测序。然后对所有样品的全部序列进行聚类,以97%的相似度将序列聚类成OTU,然后对OTU的代表序列利用SILVA的SSUrRNA数据库进行物种注释,确定16S rRNA[13]基因序列对应的细菌名称。
1.5 生物信息处理在测序得到的原始数据的基础上,进行拼接、过滤,排除干扰数据[14]。基于有效数据进行OTU聚类和物种分类分析,并将OTU和物种注释结合,从而得到每个样品的OTU和分类谱系的基本分析结果。利用EXCEL、SPSS和CANOCE软件对OTU进行物种的丰富及多样性指数等分析,然后对不同样品之间的细菌群落组成和组间差异进行统计分析,并结合水体的富营养指标探寻湖滨底泥细菌与水体富营养化之间的联系。
2 结果与分析 2.1 水体理化指标分析阳宗海南岸湖滨带由于物质输入条件及距湖岸距离不同,造成阳宗海南岸水质状况存在差异(表 1)。结果显示:阳宗海南岸湖滨带8个样点的水体均存在不同程度的富营养化状况,其中S1-1、S1-2、S2-2和S4-2为轻度富营养化,S2-1、S3-1、S3-2和S4-1为中度富营养化。S1-1样点水质条件最好,富营养化指数为55.16,其中Chla和COD分别为2.626 mg/m3和24.0 mg/L,均低于其他7个样点,属于轻度富营养化区域;S3-1样点水质条件最差,富营养化指数为69.12,其中TP和COD分别为0.141 mg/L和57.6 mg/L,为8个样点中最高,属于中度富营养化区域。远岸区域水质状况优于近岸区域,S1样带水质状况优于其他3条样带。
| 样点 Sample |
叶绿素a Chla (mg/m3) |
总磷 TP (mg/L) |
总氮 TN (mg/L) |
透明度 SD (m) |
化学需氧量 COD (mg/L) |
富营养化指数 Eutrophication index (E) |
富营养化等级 Eutrophication level |
| S1-1 | 2.626 | 0.090 | 1.170 9 | 1.0 | 24.0 | 55.16 | 轻度Light |
| S1-2 | 5.383 | 0.077 | 1.213 4 | 0.6 | 27.0 | 59.27 | 轻度Light |
| S2-1 | 12.042 | 0.073 | 1.200 6 | 0.3 | 54.6 | 67.29 | 中度Middle |
| S2-2 | 5.427 | 0.075 | 1.193 1 | 0.5 | 25.6 | 59.56 | 轻度Light |
| S3-1 | 10.437 | 0.141 | 1.188 4 | 0.3 | 57.6 | 69.12 | 中度Middle |
| S3-2 | 8.470 | 0.092 | 1.183 0 | 0.5 | 54.3 | 65.09 | 中度Middle |
| S4-1 | 10.789 | 0.077 | 1.187 3 | 0.4 | 54.3 | 66.04 | 中度Middle |
| S4-2 | 6.009 | 0.055 | 1.186 0 | 0.9 | 48.3 | 59.86 | 轻度Light |
利用16S rRNA基因高通量测序技术对阳宗海南岸湖滨带底泥细菌进行基因测序,共得到有效序列187 056条(表 2)。利用UPARSE软件[15]对测序样品的有效条带按照97%的一致性进行聚类为OTU。虽然16S rRNA基因高通量测序技术已被广泛用于微生物生态学研究中,但鉴于16S rRNA基因内部基因组存在异质性,会导致过高估计微生物多样性的情况,很少有研究考虑了基因组内异质性的影响[16]。该研究选择V3-V4区间,作为细菌目标靶向,而V4区域作为基因组内异质性最小的区域,被认为是细菌理想的靶标,从而确保微生物数据的准确性,进而对阳宗海南岸底泥微生物多样性进行正确的计算。
| 样点Sample | 有效序列Effective reads | 操作分类单元OTU | Chaol index | Shannon index | Simpson index | Coverage index |
| S1-1 | 21 182 | 730 | 937.28 | 4.79 | 0.027 5 | 0.992 |
| S1-2 | 22 271 | 1 376 | 1 525.50 | 6.37 | 0.003 4 | 0.991 |
| S2-1 | 28 490 | 1 107 | 1 383.79 | 5.27 | 0.023 5 | 0.991 |
| S2-2 | 28 736 | 1 037 | 1 276.19 | 5.18 | 0.030 5 | 0.992 |
| S3-1 | 19 338 | 1 473 | 1 654.13 | 6.30 | 0.004 2 | 0.986 |
| S3-2 | 22 655 | 1 286 | 1 415.79 | 5.73 | 0.014 6 | 0.990 |
| S4-1 | 22 391 | 1 392 | 1 570.88 | 5.88 | 0.015 5 | 0.989 |
| S4-2 | 21 993 | 1 227 | 1 445.93 | 6.13 | 0.004 2 | 0.989 |
S1-1样点包含21 182条有效序列(730个OTU),S1-2样点包含22 271条(1 376个OTU);S2-1样点包含28 490条(1 107个OTU),S2-2样点包含28 736条(1 037个OTU);S3-1样点包含19 338条(1 473个OTU),S3-2样点包含22 655条(1 286个OTU);S4-1样点包含22 391条(1 392个OTU),S4-2样点包含21 993条(1 227个OTU)。OTU分属44门、99纲、192目、311科、479属。
阳宗海南岸底泥细菌的丰富度由于外源营养输入条件及距湖岸距离的不同,使得不同样点间细菌丰富度存在差异。其中,S3样带底泥细菌丰富度较高,S2样带底泥细菌丰富度相对较低;在近岸样点中,样点S3-1底泥细菌丰富度最高,OTU数为1 473,样点S1-1底泥细菌丰富度最低,OTU数为730,两者OTU相差743,差异幅度高达50.4%。在同一条样带的近远岸底泥中细菌的丰富度也存在差异,近岸点S1-1 OTU数为730,远岸点S1-2 OTU数为1 376,两者OTU数相差646,相差47%。
本研究采用Chaol指数、Shannon指数和Simpson指数(表 2)用以表征细菌丰富度和群落多样性。结果显示:阳宗海南岸湖滨带底泥细菌丰富度最高的是样点S3-1,Chaol指数为1 654.13,丰富度最低的是样点S1-1,Chaol指数为937.28;Shannon指数表明底泥细菌群落多样性最高的是样点S1-2和S3-1,底泥细菌群落多样性最低的是样点S1-1。外源河流汇入为S3湖滨带带来大量营养物质,致使底泥中细菌大量繁殖,细菌丰富度较高;而无外源河流的S1湖滨带细菌丰富度水平较低,同时周边村落的人为活动也会影响湖滨带底泥细菌的丰富度。8组样品的Coverage指数均在0.989以上,表明本次测序的结果具有代表性,反映了底泥样本中细菌的真实情况。
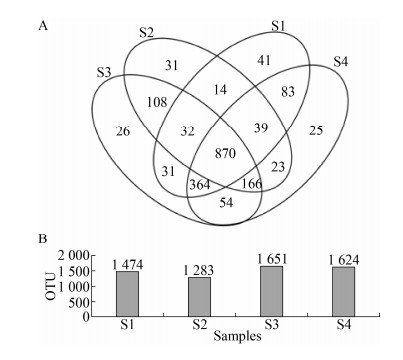
Venn图可以表现出多样本中的特有及共有的物种数(图 2)。结果表明:4条样带中,S3样带细菌丰富度最高,含1 651个OTU。丰富度最低的是S2样带,OTU数为1 283。S2和S3样带虽都有外源河流汇入,但S2样带河流汇入前会流经阳宗海湿地公园,人工湿地拦截了大量的营养物质,导致样带S2底泥细菌的OTU水平相对较低。4条样带相同OTU为870,占各条样带OTU数的一半以上,表明4条样带中细菌组成基本相似。S1的特有OTU为41;S2的特有OTU为31;S3的特有OTU为26;S4的特有OTU为25。阳宗海南岸湖滨带底泥细菌特有OTU较少。
|
| 图 2 样品OTU分布韦恩图 Figure 2 Venn of samples on OTU level |
|
|
对OTU代表序列进行物种注释,用Mothur方法[17]与SILVA的SSUrRNA数据库进行物种注释分析(设定阈值为0.8-1.0),得到门(phylum)水平上分类学信息统计和各样本的群落组成。
在4条样带中,底泥细菌的群落差异明显。在门水平上(图 3),S2样带中变形菌门(Proteobacteria)占比较大,近岸为41.8%,远岸为49.4%,占比接近1/2,其次为绿弯菌门(Chloroflexi),近岸为29.9%,远岸为27.1%。由于人工湿地对外来营养物质的拦截作用,致使S2样带的近、远岸点的营养输入条件相似,导致S2样带的群落结构相似度较高。S3样带中,近岸绿弯菌门(Chloroflexi)占比较大,比重为44.1%,变形菌门(Proteobacteria)为25.1%。远岸绿弯菌门(Chloroflexi)比重降低,为26.2%,变形菌门(Proteobacteria)比重增加为39.2%。表明在河流汇入的活跃环境中,伴随着河流带来的大量营养物质,刺激了底泥中Chloroflexi的生长。

|
| 图 3 门水平微生物群落组成 Figure 3 Microbial community composition on phylum level |
|
|
阳宗海南岸8个样点细菌群落组成主要以变形菌门(Proteobacteria)和绿弯菌门(Chloroflexi)为主,含有少量的放线菌门(Actinobacteria)、酸杆菌门(Acidobacteria)和厚壁菌门(Firmicutes)。阳宗海南岸4条样带,由近岸到远岸区域,变形菌门(Proteobacteria)的比重均有不同程度的增加。变形菌门(Proteobacteria)对近远岸造成营养输入条件的变化较为敏感。4条样带中均存在大量的绿弯菌门(Chloroflexi),在中度富营养化区域(S3-1)绿弯菌门(Chloroflexi)占比接近1/2。
利用PCA分析结果见图 4。结果显示,PC1贡献率为72.07%,PC2贡献率为19.56%,总贡献率为91.63%。在4条样带中,S1样带的近远岸和S2样带的近远岸底泥中细菌群落组成相似度高,S3样带的近远岸和S4样带的近远岸底泥细菌群落组成相似度较低。S1样带与S2样带由于外部环境相对封闭,稳定,而S3样带位处河流湖泊交汇处,物质交换活跃,致使近岸与远岸底泥中细菌丰富度和群落差异较大。表明湖滨带底泥细菌对外部环境干扰较为敏感。

|
| 图 4 样品PCA分析 Figure 4 Principal coordinate analysis of samples |
|
|
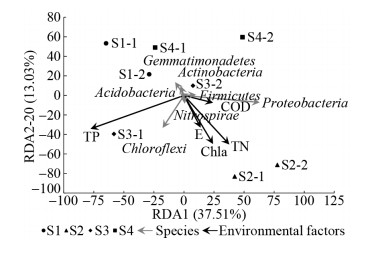
基于采样点水体理化性质数据(表 1)和底泥细菌的丰度数据,对细菌群落与水体富营养化指标进行冗余分析(图 5)。结果表明,水体总磷(TP)对阳宗海南岸湖滨带底泥中细菌群落影响最大,其次是总氮(TN)和叶绿素a (Chla),化学需氧量(COD)对底泥中细菌群落的影响较小。其中总氮(TN)、叶绿素a (Chla)和化学需氧量(COD)呈正相关。总磷(TP)与总氮(TN)、叶绿素a (Chla)和化学需氧量(COD)呈负相关。绿弯菌门(Chloroflexi)与总磷(TP)呈正相关,而变形菌门(Proteobacteria)与总氮(TN)、叶绿素a (Chla)和化学需氧量(COD)呈正相关。
|
| 图 5 环境因子关联分析图 Figure 5 Environmental factor correlation analysis diagram |
|
|
不同区域富营养化水平的差异等因素造成阳宗海湖滨带底泥细菌多样性存在差异。阳宗海湖滨带轻度富营养化区域底泥中细菌的丰富度较低,而在中度富营养化区域底泥中细菌丰富度最高。表明阳宗海底泥细菌的丰富度对水体的营养状况存在响应特征。Wan等[18]研究发现东湖不同富营养化区域的细菌种类丰富。随着水环境中营养水平的升高,细菌的多样性也会随之增加[19]。Liu等[20]研究发现,底泥中Firmicutes、Alphaproteobacteria菌群的丰度与富营养化程度存在响应关系,会随水体的富营养化程度菌群数发生变化。在阳宗海南岸湖滨带中,细菌丰富度虽存在差异,但各样本的共有OTU占各条样带OTU的一半以上,说明阳宗海南岸湖滨带底泥细菌的组成相似,造成底泥细菌丰富度差异的原因可能是各样带所处的位置。S3样带为阳宗大河入湖附近,同时带来了大量的生活、农业污水,水体磷含量高,为底泥中的细菌带来丰富的营养物质,促使底泥中的细菌生长繁殖,丰富度高。而S2样带上游的人工湿地对于入湖的外源污染进行了拦截净化,同时也减少了外源营养物质进入湖泊底泥,致使底泥中细菌丰富度相对偏少。赵思颖等[21]研究了鄱阳湖流域底泥细菌多样性差异,原因主要是由于入河口和湖区底泥中营养成分不同及某些重金属元素胁迫导致。陶怡乐等[22]对北京大学未名湖研究发现,底泥细菌多样性与水体营养盐含量呈显著正相关关系。
随着农业的发展和人类生产活动的干扰,大量污染物通过污水排放和雨淋等各种方式进入水体,使底泥受到污染。污染物的富集改变了底泥的微环境,影响细菌群落的结构和功能。湖泊底泥细菌的群落结构在湖泊碳、氮、磷、硫的物质循环中具有重要作用,而且能指示湖泊生态系统的环境状况[23]。Liu等[24]利用DGGE技术研究了梅梁湖、湖心区、东太湖等水域沉积物的细菌群落结构,结果表明细菌群落结构与营养水平和植被情况相关,在营养水平较高的位点发现疣微菌目(Verrucomicrobiales)。Zhang等[25]研究发现在云南高原湖泊沉积物中细菌丰度最高的门类为变形菌门(Proteobacteria)、酸杆菌门(Acidobacteria)和放线菌门(Actinobacteria)的占比也较大。由于水环境条件的改变及营养水平的差异,不同的区域底泥中细菌群落结构发生了变化,但菌群种类大体相似。从阳宗海南岸湖滨湿地底泥细菌群落中也可以发现相似的特征。但不同的是本研究中绿弯菌门(Chloroflexi)在阳宗海南岸湖滨带中均占比较大,S3-1样点中绿弯菌门(Chloroflexi)的比重达到了44%。王鹏等[26]研究鄱阳湖发现绿弯菌门在鄱阳湖湿地泥滩带和藜蒿带中占比较大。可能绿弯菌门(Chloroflexi)是光能自养菌,利用3-羟基丙酸途径固定CO2产生能量[27],使它能在不同营养程度的环境中生存,但富营养化程度高的区域绿弯菌门(Chloroflexi)更丰富,表明绿弯菌门(Chloroflexi)更倾向生活在营养充足的环境中。阳宗海南岸湖滨带外源河流入湖时带来大量的营养元素有利于绿弯菌门(Chloroflexi)生长繁殖,致使绿弯菌门 (Chloroflexi)成为优势细菌类群。
3.2 阳宗海湖滨带底泥细菌群落的影响因素微生物作为地球物质循环的主要推动力,在水-沉积物界面的碳、氮、磷等营养物质循环过程中也发挥着重要作用,进而影响水体的富营养化程度[28]。细菌在沉积物营养物质的积累和释放过程中发挥重要作用,能够将有机营养物质分解后转换为无机营养,并释放进入水体以供藻类等生物利用[29]。细菌对湖滨湿地生态系统的环境具有调控作用,也受到环境变化的影响并很敏感[30-31]。底泥中细菌多样性在不同季节和空间上存在差异,随着水体环境因子的差异形成自己特定生态位的群落结构[32]。
通过阳宗海湖滨带底泥中细菌群落与环境因子的相关性分析发现,总磷(TP)、叶绿素a (Chla)和总氮(TN)是阳宗海湖滨带底泥中细菌群落主要影响因子,这与以往对于富营养化湖泊的研究中显示的总磷是影响底泥细菌群落最主要的环境因子的结果一致[33-34]。由于阳宗海南岸湖滨带作为河流主要入湖区域,河流上游村镇主要从事农业生产活动,使得水体中的磷持续过量的输入,导致南岸湖滨带长期处于富营养化状态,同时大量磷进入湖滨带底泥,对底泥中细菌产生限制作用,底泥中细菌通过调整群落结构以适应湖泊生态环境的变化。阳宗海南岸湖滨带底泥中的最优势细菌类群为变形菌门,在检测的8个底泥样品中的相对丰度在20.4%-49.4%的范围内,这应与该类细菌具有较为广泛的降解代谢[35]功能有关。Sinkko等[36]在研究波罗的海底泥细菌群落时发现α-变形菌纲(Alphaproteobacteria)对底泥中营养物质的降解和释放具有重要作用。同时,还有一些比例较高的细菌类群,包括绿弯菌门(相对丰度为15.6%-44%)、放线菌门(相对丰度为2.8%-20.4%)、酸杆菌门(相对丰度为3.2%-10.5%)和厚壁菌门(相对丰度为2.3%-11.5%)等。这些主要的细菌类群中有多种已被证实在底泥或水体中具有降解作用,如绿弯菌门参与有机质降解过程[37],酸杆菌门和厚壁菌门参与多重物质和元素的降解和转化[38-39]。在阳宗海南岸湖滨带底泥中细菌长期适应大量进入底泥的氮、磷等营养物质物,已形成了一定的对应机制。底泥中细菌影响氧化还原电位,进而影响到水-沉积物界面间的物质循环,特别是磷循环[40]。在土壤淹水后,厌氧细菌开始成为了土壤微生物的主体。在厌氧铁锰还原菌的作用下,铁锰氧化物从固体溶解,变成可溶于水的离子状态。铁锰氧化物的解体直接导致吸附在氧化物表面的磷酸根释放到土壤溶液中[41]。底泥中的磷会在细菌的作用下重新进入水体,造成湖泊的持续富营养化。研究发现绿弯菌门与湖泊富营养化的主要因子总磷之间呈正相关,底泥细菌类群中的绿弯菌门可能具有指示高原湖泊富营养化程度的潜力。
4 结论(1) 阳宗海南岸湖滨带水体呈富营养化状态,底泥中细菌对水体富营养化程度存在响应特征,富营养化程度高的S3区域,OTU为1 473,底泥细菌丰富度高。在富营养化程度低的S1区域,OTU仅为730,细菌丰富度低。阳宗海湖滨带底泥中细菌丰富度存在空间异质性。
(2) 阳宗海南岸湖滨带底泥中细菌群落结构主要以变形菌门(Proteobacteria)和绿弯菌门(Chloroflexi)为主,含有少量的放线菌门(Actinobacteria)、酸杆菌门(Acidobacteria)和厚壁菌门(Firmicutes)。绿弯菌门(Chloroflexi)倾向于生长在富营养化程度高的区域。
(3) 总磷(TP)、叶绿素a (Chla)和总氮(TN)对阳宗海南岸湖滨带底泥中细菌群落的影响较强,变形菌门(Proteobacteria)与叶绿素a (Chla)、总氮(TN)和化学需氧量(COD)呈正相关,绿弯菌门(Chloroflexi)与总磷(TP)呈正相关。
| [1] |
Paerl HW, Otten TG. Harmful cyanobacterial blooms: causes, consequences, and controls[J]. Microbial Ecology, 2013, 65(4): 995-1010. DOI:10.1007/s00248-012-0159-y |
| [2] |
Cózar A, Bruno M, Bergamino N, et al. Basin-Scale control on the phytoplankton biomass in Lake Victoria, Africa[J]. PLoS One, 2012, 7(1): e29962. DOI:10.1371/journal.pone.0029962 |
| [3] |
Stumpf RP, Wynne TT, Baker DB, et al. Interannual variability of cyanobacterial blooms in Lake Erie[J]. PLoS One, 2012, 7(8): e42444. DOI:10.1371/journal.pone.0042444 |
| [4] |
Yang GS, Ma RH, Zhang L, et al. Lake status, major problems and protection strategy in China[J]. Journal of Lake Sciences, 2010, 22(6): 799-810. (in Chinese) 杨桂山, 马荣华, 张路, 等. 中国湖泊现状及面临的重大问题与保护策略[J]. 湖泊科学, 2010, 22(6): 799-810. |
| [5] |
Liu HY, Zhao ZC, Lyu XG. A study on wetland resources and protection in China[J]. Resources Science, 1999, 21(6): 34-37. (in Chinese) 刘红玉, 赵志春, 吕宪国. 中国湿地资源及其保护研究[J]. 资源科学, 1999, 21(6): 34-37. DOI:10.3321/j.issn:1007-7588.1999.06.009 |
| [6] |
Jin XC. Sediment Pollution Chemistry[M]. Beijing: China Environmental Science Press, 1992. (in Chinese) 金相灿. 沉积物污染化学[M]. 北京: 中国环境科学出版社, 1992. |
| [7] |
Liu YY, Li F, Sun QY, et al. Review on the study of soil microorganisms in wetland ecosystems[J]. Chinese Journal of Applied & Environmental Biology, 2013, 19(3): 547-552. (in Chinese) 刘银银, 李峰, 孙庆业, 等. 湿地生态系统土壤微生物研究进展[J]. 应用与环境生物学报, 2013, 19(3): 547-552. |
| [8] |
Qu JH, Li BZ, Yuan HL. Methodology in studies of microbial resource in sediment[J]. Acta Ecologica Sinica, 2007, 27(6): 2636-2641. (in Chinese) 屈建航, 李宝珍, 袁红莉. 沉积物中微生物资源的研究方法及其进展[J]. 生态学报, 2007, 27(6): 2636-2641. DOI:10.3321/j.issn:1000-0933.2007.06.058 |
| [9] |
Perrow MR, Davy AJ. Handbook of Ecological Restoration[M]. Cambridge: Cambridge University Press, 2002.
|
| [10] |
Zhu GW. Eutrophic status and causing factors for a large, shallow and subtropical Lake Taihu, China[J]. Journal of Lake Sciences, 2008, 20(1): 21-26. (in Chinese) 朱广伟. 太湖富营养化现状及原因分析[J]. 湖泊科学, 2008, 20(1): 21-26. DOI:10.3321/j.issn:1003-5427.2008.01.003 |
| [11] |
Li MY, Zheng Y, Liu YG, et al. Effects of arsenic and organic matter on the speciation of phosphorus in the sediments of Yangzonghai lakeside wetland[J]. Journal of Agro-Environment Science, 2016, 35(11): 2171-2179. (in Chinese) 李梦莹, 郑毅, 刘云根, 等. 阳宗海湖滨湿地沉积物砷和有机质对磷赋存形态的影响[J]. 农业环境科学学报, 2016, 35(11): 2171-2179. DOI:10.11654/jaes.2016-0293 |
| [12] |
Xu N, Tan GC, Wang HY, et al. Effect of biochar additions to soil on nitrogen leaching, microbial biomass and bacterial community structure[J]. European Journal of Soil Biology, 2016, 74: 1-8. DOI:10.1016/j.ejsobi.2016.02.004 |
| [13] |
Ward DM, Bateson MM, Weller R, et al. Ribosomal RNA analysis of microorganisms as they occur in nature[A]// Marshall KC. Advances in Microbial Ecology[M]. Boston, MA: Springer, 1992: 219-286
|
| [14] |
Caporaso JG, Kuczynski J, Stombaugh J, et al. QⅡME allows analysis of high-throughput community sequencing data[J]. Nature Methods, 2010, 7(5): 335-336. DOI:10.1038/nmeth.f.303 |
| [15] |
Edgar RC. UPARSE: highly accurate OTU sequences from microbial amplicon reads[J]. Nature Methods, 2013, 10(10): 996-998. DOI:10.1038/nmeth.2604 |
| [16] |
Sun DL, Jiang X, Wu QL, et al. Intragenomic heterogeneity of 16S rRNA genes causes overestimation of prokaryotic diversity[J]. Applied and Environmental Microbiology, 2013, 79(19): 5962-5969. DOI:10.1128/AEM.01282-13 |
| [17] |
Wang Q, Garrity GM, Tiedje JM, et al. Naive Bayesian classifier for rapid assignment of rRNA sequences into the new bacterial taxonomy[J]. Applied and Environmental Microbiology, 2007, 73(16): 5261-5267. DOI:10.1128/AEM.00062-07 |
| [18] |
Wan Y, Ruan XH, Zhang YP, et al. Illumina sequencing-based analysis of sediment bacteria community in different trophic status freshwater lakes[J]. Microbiologyopen, 2017, 6(4): e00450. DOI:10.1002/mbo3.450 |
| [19] |
Feng S. Dynamics of microorganisms in eutrophic waters and their roles in phosphorus cycle[D]. Nanjing: Doctoral Dissertation of Nanjing Institute of Geography and Limnology, Chinese Academy of Sciences, 2007 (in Chinese) 冯胜.富营养化水域中微生物的动态及其在磷循环中的作用研究[D].南京: 中国科学院南京地理与湖泊研究所博士学位论文, 2007 http://d.wanfangdata.com.cn/Thesis/Y1621238 |
| [20] |
Liu YQ, Yao TD, Zhu LP, et al. Bacterial diversity of freshwater alpine Lake Puma Yumco on the Tibetan Plateau[J]. Geomicrobiology Journal, 2009, 26(2): 131-145. DOI:10.1080/01490450802660201 |
| [21] |
Zhao SY, Ni CY, Fu WC, et al. The microbial response to environmental parameters of the sediment in Poyang Lake basin[J]. Journal of Jiangxi Normal University (Natural Sciences Edition), 2016, 40(2): 194-199. (in Chinese) 赵思颖, 倪才英, 符文昌, 等. 鄱阳湖流域底泥微生物对环境变量的响应[J]. 江西师范大学学报:自然科学版, 2016, 40(2): 194-199. |
| [22] |
Tao YL, Zhang CF, Xu L, et al. Temporal and spatial variation of the water quality and the sediment bacterial community in Weiming Lake, Peking University[J]. Acta Scientiarum Naturalium Universitatis Pekinensis, 2017, 53(6): 1150-1160. (in Chinese) 陶怡乐, 张晨枫, 徐琳, 等. 北京大学未名湖水质与底泥菌群结构的时空变化[J]. 北京大学学报:自然科学版, 2017, 53(6): 1150-1160. |
| [23] |
Graham EB, Knelman JE, Schindlbacher A, et al. Microbes as engines of ecosystem function: when does community structure enhance predictions of ecosystem processes?[J]. Frontiers in Microbiology, 2016, 7: 214. |
| [24] |
Liu FH, Lin GH, Gao G, et al. Bacterial and archaeal assemblages in sediments of a large shallow freshwater lake, Lake Taihu, as revealed by denaturing gradient gel electrophoresis[J]. Journal of Applied Microbiology, 2009, 106(3): 1022-1032. DOI:10.1111/j.1365-2672.2008.04069.x |
| [25] |
Zhang JX, Yang YY, Zhao L, et al. Distribution of sediment bacterial and archaeal communities in plateau freshwater lakes[J]. Applied Microbiology and Biotechnology, 2015, 99(7): 3291-3302. DOI:10.1007/s00253-014-6262-x |
| [26] |
Wang P, Chen B, Zhang H. High throughput sequencing analysis of bacterial communities in soils of a typical Poyang Lake wetland[J]. Acta Ecologica Sinica, 2017, 37(5): 1650-1658. (in Chinese) 王鹏, 陈波, 张华. 基于高通量测序的鄱阳湖典型湿地土壤细菌群落特征分析[J]. 生态学报, 2017, 37(5): 1650-1658. |
| [27] |
Klatt CG, Liu ZF, Ludwig M, et al. Temporal metatranscriptomic patterning in phototrophic Chloroflexi inhabiting a microbial mat in a geothermal spring[J]. The ISME Journal, 2013, 7(9): 1775-1789. DOI:10.1038/ismej.2013.52 |
| [28] |
Boyle-Yarwood SA, Bottomley PJ, Myrold DD. Community composition of ammonia-oxidizing bacteria and archaea in soils under stands of red alder and Douglas fir in Oregon[J]. Environmental Microbiology, 2008, 10(11): 2956-2965. DOI:10.1111/j.1462-2920.2008.01600.x |
| [29] |
Wang J, Liang XJ, Meng XL, et al. Analysis on mechanism of transportation and conversion of total phosphor in Miyun Reservoir[J]. Global Geology, 2006, 25(1): 76-80, 85. (in Chinese) 王静, 梁秀娟, 孟晓路, 等. 密云水库中总磷迁移转化机制的分析[J]. 世界地质, 2006, 25(1): 76-80, 85. DOI:10.3969/j.issn.1004-5589.2006.01.015 |
| [30] |
Feng S, Qin BQ, Gao G. Response of bacterial communities to eutrophic water in Lake Taihu[J]. Acta Scientiae Circumstantiae, 2007, 27(11): 1823-1829. (in Chinese) 冯胜, 秦伯强, 高光. 细菌群落结构对水体富营养化的响应[J]. 环境科学学报, 2007, 27(11): 1823-1829. DOI:10.3321/j.issn:0253-2468.2007.11.012 |
| [31] |
Zhao YJ, Liu B, Zhang WG, et al. Effects of plant and influent C: N: P ratio on microbial diversity in pilot-scale constructed wetlands[J]. Ecological Engineering, 2010, 36(4): 441-449. DOI:10.1016/j.ecoleng.2009.11.011 |
| [32] |
Gao HQ, Liu L, Fang ZJ. Physicochemical properties and microbial diversity of superficial deposits of lakes in summer[J]. Journal of Hohai University (Natural Sciences), 2011, 39(4): 361-366. (in Chinese) 高慧琴, 刘凌, 方泽建. 夏季湖泊表层沉积物的理化性质与微生物多样性[J]. 河海大学学报:自然科学版, 2011, 39(4): 361-366. |
| [33] |
Zeng J, Yang LY, Liang Y, et al. Spatial distribution of bacterial communities in sediment of a eutrophic lake revealed by denaturing gradient gel electrophoresis and multivariate analysis[J]. Canadian Journal of Microbiology, 2008, 54(12): 1053-1063. DOI:10.1139/W08-098 |
| [34] |
Song H, Li Z, Du B, et al. Bacterial communities in sediments of the shallow Lake Dongping in China[J]. Journal of Applied Microbiology, 2012, 112(1): 79-89. DOI:10.1111/j.1365-2672.2011.05187.x |
| [35] |
Wilms R, Köpke B, Sass H, et al. Deep biosphere-related bacteria within the subsurface of tidal flat sediments[J]. Environmental Microbiology, 2006, 8(4): 709-719. DOI:10.1111/j.1462-2920.2005.00949.x |
| [36] |
Sinkko H, Lukkari K, Sihvonen LM, et al. Bacteria contribute to sediment nutrient release and reflect progressed eutrophication-driven hypoxia in an organic-rich continental sea[J]. PLoS One, 2013, 8(6): e67061. DOI:10.1371/journal.pone.0067061 |
| [37] |
Daniel LMC, Pozzi E, Foresti E, et al. Removal of ammonium via simultaneous nitrification–denitrification nitrite-shortcut in a single packed-bed batch reactor[J]. Bioresource Technology, 2009, 100(3): 1100-1107. DOI:10.1016/j.biortech.2008.08.003 |
| [38] |
Goffredi SK, Orphan VJ. Bacterial community shifts in taxa and diversity in response to localized organic loading in the deep sea[J]. Environmental Microbiology, 2010, 12(2): 344-363. DOI:10.1111/j.1462-2920.2009.02072.x |
| [39] |
Ward NL, Challacombe JF, Janssen PH, et al. Three genomes from the phylum Acidobacteria provide insight into the lifestyles of these microorganisms in soils[J]. Applied and Environmental Microbiology, 2009, 75(7): 2046-2056. DOI:10.1128/AEM.02294-08 |
| [40] |
Kelton N, Chow-Fraser P, Jordan I. Relationship between sediment phosphorus release rates and characteristics of the benthic microbial community in a hypereutrophic marsh[J]. Aquatic Ecosystem Health & Management, 2004, 7(1): 31-41. |
| [41] |
Peretyazhko TS, Zachara JM, Kennedy DW, et al. Ferrous phosphate surface precipitates resulting from the reduction of intragrain 6-line ferrihydrite by Shewanella oneidensis MR-1[J]. Geochimica et Cosmochimica Acta, 2010, 74(13): 3751-3767. DOI:10.1016/j.gca.2010.04.008 |
 2020, Vol. 47
2020, Vol. 47




