扩展功能
文章信息
- 陶洁, 洪天旗, 王亨, 张信军, 刘惠莉, 朱国强
- TAO Jie, HONG Tian-Qi, WANG Heng, ZHANG Xin-Jun, LIU Hui-Li, ZHU Guo-Qiang
- 我国牛病毒性腹泻流行现状与防控策略
- Epidemic status and control strategies of bovine viral diarrhea in China
- 微生物学通报, 2019, 46(7): 1850-1858
- Microbiology China, 2019, 46(7): 1850-1858
- DOI: 10.13344/j.microbiol.china.180876
-
文章历史
- 收稿日期: 2018-11-07
- 接受日期: 2019-03-25
- 网络首发日期: 2019-04-23
2. 扬州大学兽医学院 江苏 扬州 225009;
3. 江苏省动物重要疫病与人畜共患病防控协同创新中心 江苏 扬州 225009
2. College of Veterinary Medicine, Yangzhou University, Yangzhou, Jiangsu 225009, China;
3. Prevention and Control of Collaborative Innovation Center of the Important Animal Disease and Zoonosis in Jiangsu Province, Yangzhou, Jiangsu 225009, China
国际病毒分类委员会(International committee on taxonomy of viruses,ICTV)已确定牛病毒性腹泻病毒1 (Bovine viral diarrhea virus 1,BVDV-1)和牛病毒性腹泻病毒2 (Bovine viral diarrhea virus 2,BVDV-2)为牛病毒性腹泻病毒(Bovine viral diarrhea virus,BVDV)的两个种,将BVDV-1、BVDV-2、猪瘟病毒(Classical swine fever virus,CSFV)和边界病毒(Border disease virus,BDV)划为黄病毒科(Flaviviridae)瘟病毒属(Pestivirus)的四大成员[1]。BVDV宿主谱很广,包括牛、猪、羊、鹿、骆驼及多种野生动物,以腹泻、母畜繁殖障碍、免疫抑制和持续感染等症状为主[2]。近年来,我国牛群、猪群中BVDV的流行现状比较严重,也没有采取相关应对措施,导致感染模式复杂化,给养殖场带来了很大的经济损失[3-4]。本文将BVDV的危害、我国牛群和猪群中BVDV-1和BVDV-2的流行现状、及国内外BVDV净化经验等进行综述,发挥预警功效,有助于BVDV领域研究人员更好地开展科研工作。
1 关注BVDV带来的经济损失与危害BVDV感染谱日益扩大,目前已报道感染40多种动物,包括牛、羊、猪等多种经济动物,造成呼吸道、消化道和生殖道多系统疾病[5]。该病被世界动物卫生组织列为必须上报的疫病之一,我国也将其列为三类动物疫病。
根据BVDV致细胞病变类型,可将其分为致细胞病变型(Cytopathoic,CP)和非致细胞病变型(Noncytopathic,NCP) BVDV。NCP型BVDV对白细胞、淋巴器官和呼吸道具有特殊趋化性;而CP型BVDV则更易感染消化道系统[6]。两者感染牛的几率相差不大,但NCP型BVDV可致犊牛出现免疫抑制和持续感染(Persistent infection,PI),从而更易感染其他病原且终身排毒,使病原体长期暴露于周围环境中[7]。90%临床病例和持续感染都是由NCP型BVDV感染引起的[8],而CP型BVDV则主要引发黏膜病(Mucosal disease,MD)。值得注意的是,NCP型BVDV在动物体内可转变为CP型BVDV,引起持续感染,一般在6周到2年内便会出现黏膜病[9]。
BVDV感染牛群带来的直接经济损失和间接经济损失都是十分巨大的。据统计[10-13],包含BVDV-2急性暴发造成的损失在内,世界各国每年每头牛损失0-552美元,平均约46.5美元;欧洲的经济损失较高,每年达87美元/每头牛。地方性流行BVDV的牧场经济损失每年可达6.46-87美元/每头牛;BVDV急性暴发的牧场经济损失每年约28.5-2 370美元/每头牛。BVDV感染导致奶制品和牛肉市场经济损失是可视化的,各国之间的差异比较大(图 1),其中爱尔兰、新西兰和加拿大排名前三,分别为每年每头牛损失54.5、41.5和30.1美元。同时考虑到BVDV感染导致母畜流产、仔猪免疫抑制和持续感染等,这些损失都是无法和难以估量的,迫切需要重视BVDV导致的危害。但我国目前尚无BVDV感染导致经济损失的相关统计数据,这也表明我国对该病的重视程度有待提升。

|
| 图 1 各国由牛BVD造成的经济损失 Figure 1 BVD economic losses in various countries worldwide |
|
|
目前国内各省市牛场都有BVDV感染的相关报道,牛群中BVDV血清抗体阳性率普遍很高,我国西部地区牛场内阳性率高达84.38%,个体阳性率达61.88%,其中奶牛为85.37%,显著高于肉牛(47.67%)和种牛(48.62%)[14];东部地区BVDV抗体阳性率也较高,牛场内阳性率达77.8%,个体阳性率为24.64%-49.74%[15]。值得注意的是,我国BVDV基因亚型多样性问题也较为突出,各地区流行的BVDV亚型各有不同(表 1),有些地区牛群中同时流行多种亚型,如北京郊区牛场中同时存着BVDV-lm、1a、1d、1q和lb等至少5种亚型[16]。截至2004年,已确定BVDV-1有12种亚型(1a-1l)[17],且逐年都有新的基因亚型出现[18-22],目前BVDV-1已有22个基因亚型(1a-1v),其中亚洲主要流行1m、1n、1o、1p、1q、1u和1v等7个亚型[23]。
| Regions | BVDV-1 subtypes |
| Beijing | 1a, 1b, 1d, 1m, 1q |
| Jiangsu | 1b, 1m, 1u |
| Shanghai | 1m |
| Liaoning | 1b, 1m, 1u |
| Henan | 1m |
| Inner Mongolia | 1m, 1u |
| Hubei | 1b, 1m, 1u |
| Guangxi | 1m, 1u |
| Sichuan | 1b, 1m |
| Qinghai | 1b, 1m, 1u |
| Tibet | 1a, 1d |
| Xinjiang | 1c |
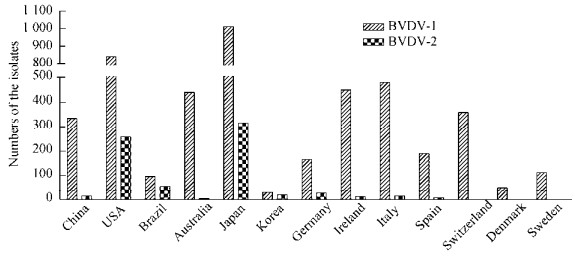
数据显示,BVDV-1感染的流行程度(88.2%)显著高于BVDV-2 (11.8%) (图 2),而且各国流行的BVDV-1亚型多样化极其明显,意大利、中国和西班牙位列前三,它们分别共同流行有15、10和9种BVDV-1亚型。多个国家流行的BVDV-1亚型超过5种,包括巴西、日本、德国、瑞士,这与疫病净化的难易程度有明显相关性。虽然BVDV-2感染流行程度较低,但它容易引起临床急性感染,以出血综合征和黏膜病为主要特征[24]。BVDV-2最早于加拿大和美国分离报道,国内在2009年首次从临床样品中分离到了CP型BVDV-2,证实BVDV-2在我国也开始流行[25]。各地区的BVDV-2流行现状存在较大差异,美国最高(39%),其次为德国(9.5%),中国约6%,而瑞士、瑞典、丹麦等国家没有BVDV-2流行的报道。世界范围内以BVDV-2a流行为主,BVDV-2c只在美国和欧洲有报道[26]。BVDV-2的流行程度直接影响BVD净化的进程和效果,瑞士、瑞典、丹麦这些国家没有BVDV-2流行,已实现了该疫病净化。因此,预警和严格控制BVDV-2感染的流行尤为重要和关键。
|
| 图 2 世界范围内BVDV-1和BVDV-2的分布情况 Figure 2 Location of BVDV-1 and BVDV-2 infections in the world |
|
|
猪也是BVDV的易感宿主之一,各年龄段猪均易感,很多国家都有BVDV感染猪群的相关报道。猪群中存在一定水平的BVDV抗体,时常会混淆猪瘟抗体监测[27]。据报道[28],澳大利亚、爱尔兰和德国等地区猪群中BVDV抗体阳性率达3%-40%,荷兰为15%-20%,挪威和丹麦分别约2.2%和6.4%,北美达2%-43%。我国也不例外,猪群中一直存在着BVDV感染现象(表 2)。自2004至2014年间,我国猪群中BVDV感染率约0-80.48%,呈现散发性和地方性流行的特点,个别地区猪群中BVDV阳性率较高[29],主要为BVDV-1,但也存在BVDV-2感染现象[25],应引起重视。
| Year | Region | Strain | Genotype | Biotype |
| 1995 | Jilin | ZM-95 | BVDV-1 | CP |
| 2008 | Shandong | SD0803 | BVDV-1 | NCP |
| 2009 | Fujian | BVDV-FJ | BVDV-1 | CP |
| 2011 | Shandong | JN-1 | BVDV-1 | NCP |
| 2011 | Shanghai | SH-28 | BVDV-2 | NCP |
| 2016 | Shanghai | SHCM06 | BVDV-1 | NCP |
虽然BVDV感染猪表现的临床症状不是很严重,但一方面,它可感染猪出现类似猪瘟的症状,混淆猪瘟的鉴别诊断;另一方面,它可引发仔猪持续性感染和免疫抑制,导致猪体免疫力下降,易诱发其他病原感染,加重疾病复杂程度[30]。鉴于猪瘟病原本身致病机制的复杂性,考虑到BVDV感染对猪群造成的危害,目前我国猪瘟流行现状复杂而严峻。基于猪瘟是我国强制性免疫疾病,现阶段最有效的措施就是要加强猪群中BVDV感染监测力度,严格淘汰阳性感染动物,逐步降低该病原的感染并净化。
4 警惕生物制品中BVDV污染BVDV感染不仅对多种动物健康造成直接影响,而且还是牛源和猪源生物制品的重要潜在污染源[31]。《中国药典》第三部(2010版)将BVDV列为犊牛血清的必检项目,也是我国活牛进口重点检疫的疫病之一[32]。但近年来,还是有不少血清和生物制品中检出BVDV污染[33-37],包括进口和国产胎牛血清、小牛血清及猪瘟疫苗等,说明我们的检测技术灵敏性以及质检工作每个环节的管理质量都有待提高。据我们不完全统计,MDBK细胞中BVDV检出率最高,其次是国产牛血清、含牛血清的细胞培养物和进口牛血清,阳性率可高达80%。大量生物制品污染BVDV,特别是胎牛血清,这就增加了猪用疫苗中污染BVDV的风险比例,也给临床带来了不确定性风险。另外,我国养殖业疫苗滥用程度比较高,很多小型养殖户经常使用一些自家疫苗,忽略了疫苗质量的重要性,往往造成得不偿失的局面。
随着生物医学技术的不断发展,动物源性生物制品的开发利用越来越广泛,这就要求生物制品质量和安全监督力度必须更上一层楼,从源头上遏制牛源生物制品包括细胞、疫苗及其他牛源制剂的污染,在确保生物制品质量安全的基础上,保障疫苗合格率,尽量避免BVDV通过直接或间接途径对人和经济动物造成危害,从而促进我国养殖业的健康持续发展。
5 BVDV-2相关研究的重要性BVDV-1和BVDV-2的流行率之所以存在如此大的差异,原因之一是两者的基因组信息明显不同,BVDV-1更易出现抗原变异,而BVDV-2病毒粒子感染性比BVDV-1更强,因此,BVDV-2感染造成的危害比BVDV-1大得多[38],我们应重视对BVDV-2的研究。
相比国外对BVDV-1和BVDV-2的研究,国内相关资料较少,特别是BVDV-2只有分离鉴定的相关报道。近年来,作者实验室对BVDV,包括BVDV-1和BVDV-2开展了较为系统的深入研究。首先,针对BVDV-1和BVDV-2在血清学有交叉反应,首次建立了BVDV-1和BVDV-2的RT-PCR鉴别诊断检测技术[39]。利用此方法,对江苏、山东、河南、新疆、青海、陕西等地牛群临床病料进行BVDV检测及病毒分离,获得了38株NCP型BVDV-2和2株CP型BVDV-2 (XJ-04和SD-06)[40];进一步鉴定XJ-04分离株全基因组序列及其细胞生物学特性[41],随后针对该病原E2蛋白,分别研制了IgM型和IgG型单克隆抗体,进而开发了BVDV-2的双抗体夹心ELISA检测方法[42],申请专利并获得授权。利用实验室建立的RT-PCR鉴别诊断方法和双抗体夹心ELISA检测方法,2008年我们从病死猪的血清样品中分离获得了16株NCP型BVDV-2,遗传特性分析表明它们与牛源BVDV-2同源性较高,考虑可能是由于使用BVDV污染的猪瘟疫苗而导致发病[43]。在此基础上,我们首次建立了猪源BVDV-2分离株SH-28的感染性克隆平台,并拯救获得了Npro缺失株,发现Npro蛋白缺失可上调细胞内抗病毒因子转录,从而抑制病毒复制[44],证实了猪源BVDV-2的Npro蛋白可以协助病毒逃逸宿主的先天免疫反应。已知BVDV的结构蛋白Erns也参与宿主先天免疫反应,我们进一步探究了Npro和Erns蛋白中影响宿主抗病毒反应的关键氨基酸位点,发现Npro蛋白中His49和Erns蛋白中K412氨基酸位点可协同抑制I型干扰素及干扰素刺激因子的表达,成功获得了猪源BVDV-2双突变减毒疫苗候选株[45]。在上述基础上,我们将继续深入研究猪源BVDV-2逃逸宿主先天免疫反应,从而探讨持续感染的作用机制。
6 国内外BVD防控和净化经验BVDV在世界范围内流行程度不一,各国对于BVD防控启动和实施也有较大差异[46-51],瑞士、挪威、丹麦等国家对BVDV的重视程度比较高,实现了在国家层面上对BVD的防控,取得了理想效果;新西兰、美国、德国等国家实现了局部地区的BVD净化。但还有很多BVDV流行比较严重的国家包括中国、巴西、澳大利亚、日本、印度、土耳其等,对BVDV感染的重视程度及防控净化措施有待加强。
BVD净化可分为3个阶段:生物安全、清除病原和监测[52]。第一个阶段,即加强养殖场生物安全防范措施,对引进种群进行全面检测,做到安全隔离,避免与外界接触,防止出现PI牛;第二个阶段,有计划地严格筛查并清除PI牛;第三个阶段,对健康群体持续监测,这是保证BVD净化成功的重要环节。总结各国成功经验,及时筛查和清除持续感染牛是BVD净化最关键的一个步骤[53]。一旦出现PI牛,健康群体中很快会出现二次感染,增加防控难度。疫苗免疫是一个可选择性方案,其主要功能是提高群体免疫力,但无法阻止PI牛的出现[54]。根据是否采用疫苗免疫,BVD净化又可分为2种方式[55],一种是“筛查-淘汰”,如奥地利、瑞士和北欧等国家;另一种是“免疫+淘汰”,如德国、比利时、爱尔兰和苏格兰等国。一般在“三高”(BVDV流行率高、动物流动频率高、养殖密度高)地区建议选择疫苗免疫。
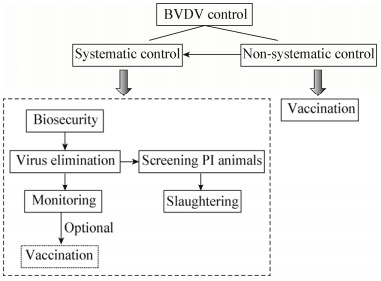
根据人们对BVD防控观念的不一致,BVD净化又可分为系统化防控(Systematic control)和非系统化防控(Non-systematic control)[56]。系统化防控是在部门、区域或国家层面上实行的,对BVDV病原和PI动物的全面监控;而非系统化防控则是由个人执行的,往往疫苗免疫是其中一个关键环节(图 3)。但很多BVD净化成功的案例表明,刚开始实施净化基本都是养殖户自发的,政府实施系统化控制,最终完成BVD净化,如瑞典和挪威[57]。因此,BVD净化效果很大程度上取决于养殖户的个人重视程度和防控观念。我们国家BVDV流行程度复杂,完全依赖政府层面的系统化控制几乎不太可能,因此,只有提高养殖户对BVDV危害的认识,自愿执行养殖场生物安全防范措施,才有可能逐步实现BVD净化。
|
| 图 3 BVDV净化方案 Figure 3 BVDV eradication scheme |
|
|
众所周知,疫病净化自然是为了获取更大的经济利益,但全面实施净化必然花费不少,包括检测费用、屠宰扑杀费用及疫苗免疫费用等。Santman-Berends等结合BVD净化的各项投入预算,预测了4种BVD净化方案在2015-2025年间的投入收益比(Benefit to cost ratio,B/C ratio)[58],图 4数据显示,“疫苗免疫”净化方式(方案2)的B/C比率最低(1.42),而“追踪-淘汰(疫苗免疫3年)”净化方式(方案3)可获得最大的B/C比率(1.47)。另外,“检测-淘汰(全程疫苗免疫)”净化方式(方案1)的B/C比率也较低,为0.55,但“个人防控-系统化控制”净化方式也能获得较好的B/C比率。这表明,疫苗免疫在BVD净化过程中不是最关键的,全程采用疫苗免疫花费太大,只有“监测-淘汰”与“免疫”合理配置才能获得最佳的B/C比率。此外,先由养殖户个体自发实施净化,而后进行全局化系统控制净化也能很大程度上减少BVD净化费用。因此各国可以此作为借鉴寻找能促进养殖业经济发展的最佳净化方案。
7 展望BVDV是对养牛业危害比较严重的病原之一,世界上很多国家已重视并较好地完成了该病的净化。我国养殖业存在多种复合模式,而且牛病研究平台尚需强化提升,疾病流行又复杂,急需提高养殖户个人和政府对BVDV危害的认识,重视防控策略的研究工作。每一种疾病的净化,起先肯定是基于养殖户的自发意识,之后才能实现区域或国家由点到面的防控。那么如何激发养殖户对BVD的防控意识?这就要求兽医界人士发挥主力军作用,多深入基层,通过沟通交流,让养殖户逐步意识到BVDV带来的危害,提高他们对疫病净化的迫切需求。其次,结合养殖场特点定制合理的净化方案,降低PI动物感染率,短期内提高养殖户经济效益以及开展疫病净化的积极性,才有可能让BVD净化得以持续性发展。我国养殖模式多样化,建议各养殖场根据BVDV流行病学监测结果实行不同的净化方案,综合考虑是否需要疫苗免疫。BVDV流行率高的养殖场可选择性采用疫苗免疫手段,而BVDV流行率较低的则不建议采用疫苗免疫,即各点各自执行净化。当然,BVD净化成功离不开系统化防控,即政府和国家层面的全面支持。只有各系统相互密切配合,才可能实现净化BVD的最终目标。
我国人口众多,随着社会经济发展,国民对奶制品和肉制品的需求量大于供货量。然而BVDV感染不仅使奶牛产奶量大幅度下降,而且牛奶和牛肉品质等也将大打折扣。一旦我国经济动物不能保证品质健康,那么进口量必然会增加,一方面不利于经济发展,另一方面也将增加新病原带入的风险。因此,我们必须重视BVDV对我国经济动物的危害,提高防控意识,加强BVD净化。
| [1] |
Yeşilbağ K, Alpay G, Becher P. Variability and global distribution of subgenotypes of bovine viral diarrhea virus[J]. Viruses, 2017, 9(6): 128. DOI:10.3390/v9060128 |
| [2] |
Bianchi MV, Silveira S, Mósena ACS, et al. Pathological and virological features of skin lesions caused by BVDV in cattle[J]. Brazilian Journal of Microbiology, 2019, 50(1): 271-277. DOI:10.1007/s42770-018-0019-0 |
| [3] |
Dong SJ, Feng M, Yu RS, et al. Establishment and application of visual LAMP detection method of infectious bovine rhinotracheitis virus[J]. Chinese Journal of Biotechnology, 2018, 34(10): 1587-1595. (in Chinese) 董世娟, 冯蒙, 于瑞嵩, 等. 牛传染性鼻气管炎可视化LAMP检测方法的建立和应用[J]. 生物工程学报, 2018, 34(10): 1587-1595. |
| [4] |
Han DG, Ryu JH, Park J, et al. Identification of a new bovine viral diarrhea virus subtype in the Republic of Korea[J]. BMC Veterinary Research, 2018, 14: 233. DOI:10.1186/s12917-018-1555-4 |
| [5] |
Khodakaram-Tafti A, Farjanikish GH. Persistent bovine viral diarrhea virus (BVDV) infection in cattle herds[J]. Iranian Journal of Veterinary Research, 2017, 18(3): 154-163. |
| [6] |
Bezek DM, Gröhn YT, Dubovi EJ. Effect of acute infection with noncytopathic or cytopathic bovine viral diarrhea virus isolates on bovine platelets[J]. American Journal of Veterinary Research, 1994, 55(8): 1115-1119. |
| [7] |
Garoussi MT, Mehrzad J, Nejati A. Investigation of persistent infection of bovine viral diarrhea virus (BVDV) in Holstein dairy cows[J]. Tropical Animal Health and Production, 2019, 55: 853-858. |
| [8] |
Schweizer M, Mätzener P, Pfaffen G, et al. "Self" and "Nonself" manipulation of interferon defense during persistent infection: bovine viral diarrhea virus resists alpha/beta interferon without blocking antiviral activity against unrelated viruses replicating in its host cells[J]. Journal of Virology, 2006, 80(14): 6926-6935. DOI:10.1128/JVI.02443-05 |
| [9] |
Peterhans E, Bachofen C, Stalder H, et al. Cytopathic bovine viral diarrhea viruses (BVDV): emerging pestiviruses doomed to extinction[J]. Veterinary Research, 2010, 41(6): 44. DOI:10.1051/vetres/2010016 |
| [10] |
Yarnall MJ, Thrusfield MV. Engaging veterinarians and farmers in eradicating bovine viral diarrhoea: a systematic review of economic impact[J]. Veterinary Record, 2017, 181(13): 347. DOI:10.1136/vr.104370 |
| [11] |
Hessman BE, Fulton RW, Sjeklocha DB, et al. Evaluation of economic effects and the health and performance of the general cattle population after exposure to cattle persistently infected with bovine viral diarrhea virus in a starter feedlot[J]. American Journal of Veterinary Research, 2009, 70(1): 73-85. DOI:10.2460/ajvr.70.1.73 |
| [12] |
Stott AW, Humphry RW, Gunn GJ, et al. Predicted costs and benefits of eradicating BVDV from Ireland[J]. Irish Veterinary Journal, 2012, 65(1): 12. DOI:10.1186/2046-0481-65-12 |
| [13] |
Richter V, Lebl K, Baumgartner W, et al. A systematic worldwide review of the direct monetary losses in cattle due to bovine viral diarrhoea virus infection[J]. The Veterinary Journal, 2017, 220: 80-87. DOI:10.1016/j.tvjl.2017.01.005 |
| [14] |
Qu P, Zhao BL, Hu DM, et al. Survey of the bovine viral diarrhea virus prevalence in the west of China[J]. Heilongjiang Animal Science and Veterinary Medicine, 2016(3): 111-113. (in Chinese) 曲萍, 赵柏林, 胡冬梅, 等. 我国西部地区牛病毒性腹泻流行情况调查[J]. 黑龙江畜牧兽医, 2016(3): 111-113. |
| [15] |
Sun WW, Meng QF, Cong W, et al. Herd-level prevalence and associated risk factors for Toxoplasma gondii, Neospora caninum, Chlamydia abortus and bovine viral diarrhoea virus in commercial dairy and beef cattle in eastern, northern and northeastern China[J]. Parasitology Research, 2015, 114(11): 4211-4218. DOI:10.1007/s00436-015-4655-0 |
| [16] |
Weng XG. Epidemiologic survey of bovine viral diarrhea in Beijing region, study of IFN-α/β response in persistently infected catttle and immunomodulatory effects of forsythoside A[D]. Beijing: Doctoral Dissertation of China Agricultural University, 2015 (in Chinese) 翁晓刚.北京市牛病毒性腹泻的流行病学调查、持续性感染牛IFN-α/β反应及连翘酯苷A免疫调节作用的研究[D].北京: 中国农业大学博士学位论文, 2015 |
| [17] |
Vilček Š, Ďurkovič B, Kolesárová M, et al. Genetic diversity of international bovine viral diarrhoea virus (BVDV) isolates: identification of a new BVDV-1 genetic group[J]. Veterinary Research, 2004, 35(5): 609-615. DOI:10.1051/vetres:2004036 |
| [18] |
Xue F, Zhu YM, Li J, et al. Genotyping of bovine viral diarrhea viruses from cattle in China between 2005 and 2008[J]. Veterinary Microbiology, 2010, 143(2/4): 379-383. |
| [19] |
Gao SD, Luo JH, Du JZ, et al. Serological and molecular evidence for natural infection of Bactrian camels with multiple subgenotypes of bovine viral diarrhea virus in Western China[J]. Veterinary Microbiology, 2013, 163(1/2): 172-176. |
| [20] |
Giammarioli M, Ceglie L, Rossi E, et al. Increased genetic diversity of BVDV-1: recent findings and implications thereof[J]. Virus Genes, 2015, 50(1): 147-151. DOI:10.1007/s11262-014-1132-2 |
| [21] |
Deng ML, Ji SK, Fei WT, et al. Prevalence study and genetic typing of bovine viral diarrhea virus (BVDV) in four bovine species in China[J]. PLoS One, 2015, 10(4): e0121718. DOI:10.1371/journal.pone.0121718 |
| [22] |
Zhu YM, Yang LX, Ma L, et al. Isolation and identification of bovine viral diarrhea virus strain LJ36/14[J]. Chinese Journal of Preventive Veterinary Medicine, 2016, 38(12): 949-952. (in Chinese) 朱远茂, 杨立新, 马磊, 等. 牛病毒性腹泻病毒LJ36/14的分离与鉴定[J]. 中国预防兽医学报, 2016, 38(12): 949-952. |
| [23] |
Evans CA, Hemmatzadeh F, Reichel MP, et al. Natural transmission of bovine viral diarrhoea virus-1c from a persistently infected neonate lamb to naïve sheep and cattle[J]. Veterinary Record, 2018, 182(12): 352. DOI:10.1136/vr.104468 |
| [24] |
Gethmann J, Homeier T, Holsteg M, et al. BVD-2 outbreak leads to high losses in cattle farms in Western Germany[J]. Heliyon, 2015, 1(1): e00019. DOI:10.1016/j.heliyon.2015.e00019 |
| [25] |
Tao J, Wang Y, Wang J, et al. Identification and genetic characterization of new bovine viral diarrhea virus genotype 2 strains in pigs isolated in China[J]. Virus Genes, 2013, 46(1): 81-87. DOI:10.1007/s11262-012-0837-3 |
| [26] |
Yeşilbağ K, Alpay G, Becher P. Variability and global distribution of subgenotypes of bovine viral diarrhea virus[J]. Viruses, 2017, 9(6): 128. DOI:10.3390/v9060128 |
| [27] |
Gatto IRH, Linhares DCL, de Souza Almeida HM, et al. Description of risk factors associated with the detection of BVDV antibodies in Brazilian pig herds[J]. Tropical Animal Health and Production, 2018, 50(4): 773-778. DOI:10.1007/s11250-017-1493-3 |
| [28] |
Mechler ML, Dos Santos Gomes F, Nascimento KA, et al. Congenital tremor in piglets: is bovine viral diarrhea virus an etiological cause?[J]. Veterinary Microbiology, 2018, 220: 107-112. DOI:10.1016/j.vetmic.2018.05.009 |
| [29] |
Bai QY, Xu L, Fu GH, et al. Establishment and monitoring analysis of fluorescence RT-PCR for detection of bovine viral diarrhea virus in swine[J]. Fujian Journal of Agricultural Sciences, 2017, 32(8): 828-832. (in Chinese) 白泉阳, 徐磊, 傅光华, 等. 检测猪源牛病毒性腹泻病毒荧光RT-PCR方法的建立与监测分析[J]. 福建农业学报, 2017, 32(8): 828-832. |
| [30] |
Tao J, Liao JH, Wang Y, et al. Bovine viral diarrhea virus (BVDV) infections in pigs[J]. Veterinary Microbiology, 2013, 165(3/4): 185-189. |
| [31] |
Pinheiro De Oliveira TF, Fonseca Jr AA, Camargos MF, et al. Detection of contaminants in cell cultures, sera and trypsin[J]. Biologicals, 2013, 41(6): 407-414. DOI:10.1016/j.biologicals.2013.08.005 |
| [32] |
Ju HB, Yang DQ, Ge FF, et al. Detection of bovine viral diarrhea virus in commercial fetal serum and classical swine fever vaccine[J]. Shanghai Journal of Animal Husbandry and Veterinary Medicine, 2015(2): 44-45. (in Chinese) 鞠厚斌, 杨德全, 葛菲菲, 等. 商品化胎牛血清及猪瘟疫苗中牛病毒性腹泻病毒污染的检测[J]. 上海畜牧兽医通讯, 2015(2): 44-45. DOI:10.3969/j.issn.1000-7725.2015.02.017 |
| [33] |
Wang JC, Wang JF, Cui Y, et al. Development and application of a one-step dual real-time RT-PCR for detection and typing of bovine viral diarrhea virus[J]. Chinese Journal of Veterinary Science, 2018, 38(2): 245-251. (in Chinese) 王建昌, 王金凤, 崔元, 等. BVDV一步法双重荧光RT-PCR检测方法的建立及应用[J]. 中国兽医学报, 2018, 38(2): 245-251. |
| [34] |
Wang J, Fu R, Li XB, et al. Establishment and application of a RT-PCR detection method for bovine viral diarrhea virus[J]. Chinese Journal of Comparative Medicine, 2017, 27(11): 68-74. (in Chinese) 王吉, 付瑞, 李晓波, 等. 牛病毒性腹泻病毒RT-PCR方法的建立及应用[J]. 中国比较医学杂志, 2017, 27(11): 68-74. |
| [35] |
Zhang SQ, Tan B, Cheng SP. Isolation and identification of bovine viral diarrhea virus-2 from the established MDCK cell line[J]. Chinese Journal of Animal Infectious Diseases, 2016, 24(3): 83-86. (in Chinese) 张淑琴, 谭斌, 程世鹏. 牛病毒性腹泻病毒基因2型毒株的分离与鉴定[J]. 中国动物传染病学报, 2016, 24(3): 83-86. DOI:10.3969/j.issn.1674-6422.2016.03.015 |
| [36] |
Shu X, Dong XY, Mao L, et al. Isolation and identification of two strains of bovine viral diarrhea virus 2[J]. Animal Husbandry & Veterinary Medicine, 2018, 50(10): 105-109. (in Chinese) 舒鑫, 董心仪, 毛立, 等. 2株牛病毒性腹泻病毒基因2型的分离鉴定[J]. 畜牧与兽医, 2018, 50(10): 105-109. |
| [37] |
Chen B, Xu CL, Dong XM, et al. Development of a method for determination of bovine viral diarrhea virus in bovine serum by direct CPE on calf kidney cells[J]. Chinese Journal of Biologicals, 2009, 22(8): 819-822. (in Chinese) 陈波, 徐程林, 董小曼, 等. 牛血清中牛腹泻病毒牛肾细胞直接病变检测方法的建立[J]. 中国生物制品学杂志, 2009, 22(8): 819-822. |
| [38] |
Zhang Q, Tao J, Zhang D, et al. Research progress of genotype 2 bovine viral diarrhea virusin China[J]. Chinese Journal of Animal Infectious Diseases, 2017, 25(1): 80-86. (in Chinese) 张倩, 陶洁, 张东, 等. 国内新型基因2型牛病毒性腹泻病毒研究进展[J]. 中国动物传染病学报, 2017, 25(1): 80-86. |
| [39] |
Ren M, Jiao HH, Jiang Y, et al. Establishment of RT-PCR assay for detection of bovine viral diarrhea virus genotype 2[J]. Chinese Journal of Preventive Veterinary Medicine, 2008, 30(9): 665-668. (in Chinese) 任敏, 焦海宏, 蒋颖, 等. 基因2型牛病毒性腹泻病毒RT-PCR检测方法的建立和初步应用[J]. 中国预防兽医学报, 2008, 30(9): 665-668. |
| [40] |
Zhu LQ, Lin YQ, Ding XY, et al. Genomic sequencing and characterization of a Chinese isolate of Bovine viral diarrhea virus 2[J]. Acta Virologica, 2009, 53(2): 197-202. |
| [41] |
Lin YQ, Zhu LQ, Tao J, et al. Genomic sequencing and characterization of bovine viral diarrhea virus genotype 2 isolate XJ-04[J]. Chinese Journal of Preventive Veterinary Medicine, 2011, 33(1): 23-27. (in Chinese) 林燕清, 朱礼倩, 陶洁, 等. 牛病毒性腹泻病毒基因2型代表株全基因组序列分析[J]. 中国预防兽医学报, 2011, 33(1): 23-27. DOI:10.3969/j.issn.1008-0589.2011.01.06 |
| [42] |
Jiang Y, Lin YQ, Tao J, et al. Preparation of monoclonal antibodies against bovine viral diarrhea virus and the double antibody sandwich ELISA development[J]. Chinese Journal of Preventive Veterinary Medicine, 2012, 34(12): 972-975. (in Chinese) 蒋颖, 林燕清, 陶洁, 等. 抗牛病毒性腹泻病毒单克隆抗体的制备及双抗夹心ELISA检测方法的建立[J]. 中国预防兽医学报, 2012, 34(12): 972-975. DOI:10.3969/j.issn.1008-0589.2012.12.10 |
| [43] |
Tao J, Zhu IQ, Lin YQ, et al. Identification and characterization of 16 recent Chinese isolates of bovine viral diarrhea virus genotype 2 (BVDV-2)[J]. African Journal of Microbiology Research, 2011, 5(11): 1272-1276. DOI:10.5897/AJMR |
| [44] |
Tao J, Liao JH, Wang JY, et al. Pig BVDV-2 non-structural protein (Npro) links to cellular antiviral response in vitro[J]. Virus Genes, 2017, 53(2): 233-239. DOI:10.1007/s11262-016-1410-2 |
| [45] |
Tao J, Li BQ, Chen JH, et al. Npro His49 and Erns Lys412 mutations in pig bovine viral diarrhea virus type 2 synergistically enhance the cellular antiviral response[J]. Virus Genes, 2018, 54(1): 57-66. DOI:10.1007/s11262-017-1506-3 |
| [46] |
Larghi M. Comparative study in the control of bovine viral diarrhea[J]. Animal Health Research Reviews, 2018, 19(2): 125-133. DOI:10.1017/S1466252318000129 |
| [47] |
Reichel MP, Lanyon SR, Hill FI. Perspectives on current challenges and opportunities for bovine viral diarrhoea virus eradication in Australia and New Zealand[J]. Pathogens, 2018, 7(1): 14. DOI:10.3390/pathogens7010014 |
| [48] |
Hult L, Lindberg A. Experiences from BVDV control in Sweden[J]. Preventive Veterinary Medicine, 2005, 72(1/2): 143-148. |
| [49] |
Løken T, Nyberg O. Eradication of BVDV in cattle: the Norwegian project[J]. Veterinary Record, 2013, 172(25): 661. DOI:10.1136/vr.101525 |
| [50] |
Ridpath J. Preventive strategy for BVDV infection in North America[J]. Japanese Journal of Veterinary Research, 2012, 60(Suppl 1): S41-S49. |
| [51] |
Wernike K, Schirrmeier H, Strebelow HG, et al. Eradication of bovine viral diarrhea virus in Germany — diversity of subtypes and detection of live-vaccine viruses[J]. Veterinary Microbiology, 2017, 208: 25-29. DOI:10.1016/j.vetmic.2017.07.009 |
| [52] |
Barrett DJ, More SJ, Graham DA, et al. Considerations on BVD eradication for the Irish livestock industry[J]. Irish Veterinary Journal, 2011, 64: 12. DOI:10.1186/2046-0481-64-12 |
| [53] |
Stalder H, Hug C, Zanoni R, et al. A nationwide database linking information on the hosts with sequence data of their virus strains: a useful tool for the eradication of bovine viral diarrhea (BVD) in Switzerland[J]. Virus Research, 2016, 218: 49-56. DOI:10.1016/j.virusres.2015.09.012 |
| [54] |
Wernike K, Gethmann J, Schirrmeier H, et al. Six years (2011-2016) of mandatory nationwide bovine viral diarrhea control in Germany — a success story[J]. Pathogens, 2017, 6(4): 50. DOI:10.3390/pathogens6040050 |
| [55] |
Kaiser V, Nebel L, Schüpbach-Regula G, et al. Influence of border disease virus (BDV) on serological surveillance within the bovine virus diarrhea (BVD) eradication program in Switzerland[J]. BMC Veterinary Research, 2016, 13: 21. DOI:10.1186/s12917-016-0932-0 |
| [56] |
Moennig V, Becher P. Control of bovine viral diarrhea[J]. Pathogens, 2018, 7(1): 29. DOI:10.3390/pathogens7010029 |
| [57] |
Truyers IGR, Mellor DJ, Norquay R, et al. Eradication programme for bovine viral diarrhoea virus in Orkney 2001 to 2008[J]. Veterinary Record, 2010, 167(15): 566-570. DOI:10.1136/vr.c4944 |
| [58] |
Santman-Berends IMGA, Mars MH, Van Duijn L, et al. Evaluation of the epidemiological and economic consequences of control scenarios for bovine viral diarrhea virus in dairy herds[J]. Journal of Dairy Science, 2015, 98(11): 7699-7716. DOI:10.3168/jds.2014-9255 |
 2019, Vol. 46
2019, Vol. 46





