扩展功能
文章信息
- 孔维亮, 周敏, 吴小芹
- KONG Wei-Liang, ZHOU Min, WU Xiao-Qin
- 水拉恩氏菌JZ-GX1产嗜铁素特性及其对林木病原菌的拮抗作用
- Characteristics of siderophores production by Rahnella aquatilis JZ-GX1 and its antagonism against forest pathogens
- 微生物学通报, 2019, 46(12): 3278-3285
- Microbiology China, 2019, 46(12): 3278-3285
- DOI: 10.13344/j.microbiol.china.190070
-
文章历史
- 收稿日期: 2019-01-22
- 接受日期: 2019-04-02
- 网络首发日期: 2019-04-22
铁是所有生物体不可或缺的营养元素之一。尽管在多数土壤中全铁含量丰富,但绝大部分铁要么是以微生物不能利用的化学形态存在,要么深埋在矿物颗粒中[1]。栖息在土壤中的病原菌需要在宿主植物被感染之前与土壤微生物群落的其他成员竞争生长所需的稀缺可用铁,因此,铁获取是许多植物病原菌完全毒力的基础[2]。许多植物根际促生细菌(Plant growth promoting rhizobacteria,PGPR)在铁缺乏的情况下自身可产生能特异性螯合Fe3+的小分子化合物——嗜铁素,研究表明,这些铁载体可以通过剥夺铁来抑制土壤中病原体的生长,从而达到控制植物病害的目的[3-4]。Tortora等利用巴西固氮螺菌(Azospirillum brasilense)产生的儿茶酚型铁载体防治由尖孢炭疽菌(Colletotrichum acutatum)引起的草莓炭疽病,取得了较好的效果[5]。陈伟等从多年生黑麦草根际土壤中分离得到一株假单胞菌属(Pseudomonas)细菌,在低铁条件下对黄瓜灰霉病菌(Botrytis cinerea)的生长抑制率高达91.2%[6]。
本实验室前期从马尾松根际分离得到一株根际促生菌水拉恩氏菌(Rahnella aquatilis)JZ-GX1,前期研究表明,该菌能够产生嗜铁素、纤维素酶和磷酸酯酶,对杨树溃疡病有一定的防治效果[7]。然而关于水拉恩氏菌JZ-GX1产嗜铁素的最优培养条件未见报道,同时该菌株对林木根部病原的拮抗作用也不清楚。鉴于嗜铁素在根际促生菌铁营养竞争中的重要地位,同时考虑到规模化生产应用的需求,本研究拟对水拉恩氏菌JZ-GX1产嗜铁素条件进行优化,并对产嗜铁素类型进行鉴定,最后对优化后的菌株发酵液对两种林木根部病原菌的拮抗效果进行初步评价,以期运用微生物产生的嗜铁素对铁的清除作用来评价由铁载体介导的土传病害防控提供新的研究思路。
1 材料与方法 1.1 材料 1.1.1 供试菌株根际促生细菌水拉恩氏菌(Rahnella aquatilis) JZ-GX1分离自广西南宁28年生马尾松根际土壤,土传病原菌:立枯丝核菌(Rhizoctonia solani)、樟疫霉(Phytophthora cinnamomi),均保存于南京林业大学森林病理实验室。
1.1.2 培养基、主要试剂和仪器MSA培养基(g/L):蔗糖20.0,天冬酰胺2.0,K2HPO4,MgSO4·7H2O 0.5。SM培养基(g/L):K2HPO4 6.0,NH4H2PO4 3.0,MgSO4·7H2O 0.2,琥珀酸钠4.0,pH 7.0−7.2。NB培养基(g/L):牛肉膏3.0,蛋白胨10.0,NaCl 5.0,pH 7.4−7.6。LB培养基(g/L):蛋白胨10.0,酵母浸出粉10.0,NaCl 10.0,pH 7.0。KMB培养基(g/L):蛋白胨20.0,甘油10 mL,K2HPO4 1.5。PDA培养基(g/L):马铃薯200.0,葡萄糖20.0。CM培养基(g/L):柠檬酸钠2.0,NH4NO3 1.0,K2HPO4 0.5。
天冬酰胺,中国惠兴生化试剂有限公司;丙三醇,南京化学试剂股份有限公司;硝酸钠,合肥科华精细化工研究所;钼酸钠,南京宁试化学试剂有限公司;其它生化试剂,国药集团化学试剂有限公司。
紫外分光光度计,珀金埃尔默股份有限公司;高速台式离心机,上海安亭科学仪器厂;pH计,梅特勒-托利多仪器(上海)有限公司。
1.2 菌株产嗜铁素的类型分析通过FeCl3实验[8]、四唑盐实验[9]、Arnow’s实验[10]及Shenkerʼs实验[11]分析和确定菌株产嗜铁素的类型。
1.3 菌株产嗜铁素的定量分析从固体NA平板上挑取单菌落,用铂金丝接种环挑取新鲜菌苔于50 mL NB培养基中,28℃、180 r/min培养过夜,之后4 ℃、10 000 r/min离心10 min收集菌体,用0.85%的生理盐水洗涤2次,调节菌悬液浓度为107 CFU/mL备用。然后将该菌悬液按上述处理接到相应的培养基中,4 ℃、10 000 r/min离心10 min取上清。按体积比1׃1加入铬天青(Chrome azurol S,CAS)检测液,充分混匀后静置1 h,测定630 nm处的吸光值(As),以双蒸水为对照调零。另取空白培养基与CAS检测液等体积混匀,以其吸光值作参比值(Ar),根据公式[(Ar–As)/Ar]×100%计算嗜铁素的相对含量[12]。
1.4 菌株产嗜铁素的最佳发酵条件筛选 1.4.1 培养基选取KMB、NB、LB、PDB、CM、MSA、LNM和SM共8种培养基[13]进行菌株嗜铁素产生的发酵培养,按照1.3中公式计算嗜铁素的相对含量,选用最优培养基进行后续实验。
1.4.2 起始pH将发酵培养基的起始pH值分别设4.0、4.5、5.0、5.5、6.0、6.5、7.0、7.5、8.0、8.5、9.0共11个处理,其他培养条件和检测方法同1.4.1。
1.4.3 发酵时间分别设6、12、24、36、48、60、72 h共7个处理进行菌株嗜铁素产生的发酵培养,其它培养条件和检测方法同1.4.1。
1.4.4 接种量分别设0.1%、0.5%、1.0%、1.5%、2.0%、3.0%共6个处理进行菌株嗜铁素产生的发酵培养,其它培养条件和检测方法同1.4.1。
1.4.5 温度分别设15、20、25、28、30、33、37 ℃共7个处理进行菌株嗜铁素产生的发酵培养,其它培养条件和检测方法同1.4.1。
1.4.6 装瓶量50 mL瓶中分别设10、20、25、30、40 mL共5个装瓶量进行菌株产生嗜铁素的发酵培养,其它培养条件和检测方法同1.4.1。
1.5 菌株产嗜铁素发酵液与病原菌拮抗作用测定将1.4中不同处理得出的最佳发酵影响因素综合起来再进行发酵,发酵液离心后,经0.22μm的微孔滤膜过滤除菌,然后分别按原液、10×、100×的稀释倍数与PDA培养基混合,制成带毒平板,待培养基凝固后,在平板中央接种直径为8 mm的各病原菌菌块,25 ℃下培养5 d后,用十字交叉法测量菌饼直径[14]。以加KMB培养基为阴性对照,以加50 mg/L的8-羟基喹啉(去除痕量铁)为阳性对照。菌饼扩展直径(mm)为菌饼的平均直径(mm)与接种菌饼直径(8 mm)之差,抑制率公式计算:抑制率(%)=(对照组菌饼扩展直径–处理组菌饼扩展直径)/对照组菌饼扩展直径×100。
1.6 数据分析试验数据利用SPSS 22.0软件进行方差分析和Duncan多重比较(P < 0.05),计算所有均值的标准误。
2 结果与分析 2.1 水拉恩氏菌JZ-GX1嗜铁素种类的特异性分析在Shenker’s实验中,由JZ-GX1制备的铁载体溶液在230 nm处出现吸收峰,说明该菌能产生羧酸型铁载体;在四唑盐实验中,溶液颜色能够立即发生变化呈深红色,说明该菌能够产生异羟肟酸型嗜铁素,因此判断水拉恩氏菌JZ-GX1的嗜铁素为复合型铁载体。
2.2 水拉恩氏菌JZ-GX1产嗜铁素的发酵条件优化 2.2.1 培养基对JZ-GX1菌株嗜铁素产量的影响由图 1可知,水拉恩氏菌JZ-GX1嗜铁素上清液的OD630值在各供试培养基中由大到小依次为:KMB > MSA > LNM > NB,各培养基之间差异达到显著水平;而在LB、CM、PDB、SM培养基中,JZ-GX1嗜铁素上清液OD630值均为负值。说明在8种供试培养基中,KMB培养基最有利于菌株JZ-GX1分泌嗜铁素。

|
| 图 1 培养基对JZ-GX1嗜铁素产量的影响 Figure 1 Effects of different medium on siderophore production 注:柱状图上不同小写字母代表在0.05水平上差异显著. Note: Columns with different letters indicate significant differences at P < 0.05. |
|
|
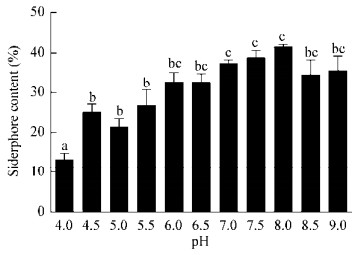
由图 2可知,环境pH值对JZ-GX1菌株嗜铁素产量的影响总趋势是:随着pH值增大呈先上升后下降的趋势,于pH值8.0时达到最大值表明JZ-GX1分泌的复合型铁载体更倾向于偏碱性的环境,这对于碱性和石灰性土壤抗缺铁营养胁迫和病原菌拮抗具有特殊意义。
|
| 图 2 初始pH值对JZ-GX1嗜铁素产量的影响 Figure 2 Effects of different initial pH value on siderophore production 注:柱状图上不同小写字母代表在0.05水平上差异显著. Note: Columns with different letters indicate significant differences at P < 0.05. |
|
|
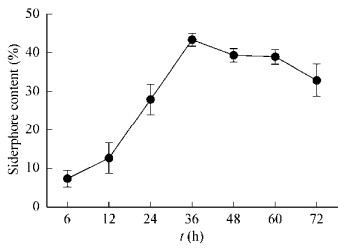
由图 3可知,发酵时间直接影响JZ-GX1菌株嗜铁素的分泌量,随着发酵时间的延长,从6 h到36 h急剧上升,于36 h达到最大分泌量,36 h到72 h之间有所下降。因此,选择36 h为最佳的产嗜铁素发酵时间。
|
| 图 3 发酵时间对JZ-GX1嗜铁素产量的影响 Figure 3 Effects of different fermentation time on siderophore production |
|
|
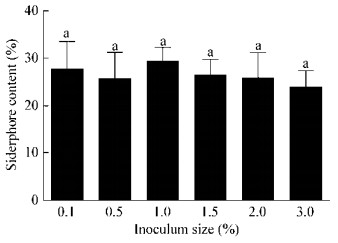
接种量的大小对发酵单位有较大影响,接种量小的时候,延迟期变长,发酵时间延长;接种量变大时,菌体迅速生长,导致培养基营养成分不够,从而降低发酵单位。由图 4可以看出以1%接种量为最佳,然而各处理间差异不显著(P > 0.05)。
|
| 图 4 接种量对JZ-GX1嗜铁素产量的影响 Figure 4 Effects of different inoculation amount on siderophore production 注:柱状图上相同小写字母代表在0.05水平上差异不显著. Note: Columns with same letters indicate no significant differences at P > 0.05. |
|
|
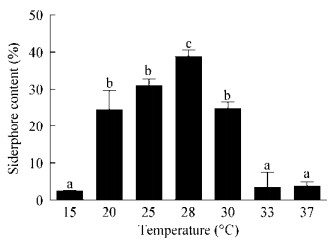
由图 5可知,JZ-GX1在供试的温度范围内培养均可获得一定量的嗜铁素,在28 ℃以下,随着温度的升高,嗜铁素产量逐渐提高,在28 ℃时达到最大值;之后随着温度升高产量逐渐下降,说明温度对嗜铁素分泌的影响较大,在最适生长温度范围(20−30℃)内,嗜铁素产量较高,温度偏低或偏高均不利于JZ-GX1分泌嗜铁素。
|
| 图 5 温度对JZ-GX1嗜铁素产量的影响 Figure 5 Effects of different temperature on siderophore production 注:柱状图上不同小写字母代表在0.05水平上差异显著. Note: Columns with different letters indicate significant differences at P < 0.05. |
|
|
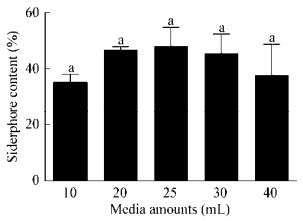
装瓶量的多少关系到发酵时的通气量,通气量是影响需氧菌菌体生长和代谢物生成的重要因素。试验结果表明,在瓶装量为25 mL/50 mL时,嗜铁素的产量最多,但与其他装瓶量处理后的嗜铁素含量相比没有显著性差异(P > 0.05) (图 6)。
|
| 图 6 装瓶量对JZ-GX1嗜铁素产量的影响 Figure 6 Effects of different media amounts on siderophore production 注:柱状图上相同小写字母代表在0.05水平上差异不显著. Note: Columns with same letters indicate no significant differences at P > 0.05. |
|
|
由图 7可以看出,水拉恩氏菌JZ-GX1嗜铁素的发酵滤液对两种病原菌具有较强的抑制作用,抑制率在26.36%−100% (表 1)。随着发酵液稀释倍数的增加,嗜铁素浓度降低,抑制率减小,当稀释倍数为10×和100×时,JZ-GX1菌株产嗜铁素发酵滤液对樟疫霉的抑制效果要强于立枯丝核菌;而原液则完全抑制樟疫霉和立枯丝核菌的生长,达到了和阳性对照(添加8-羟基喹啉)同样的效果。方差分析结果显示,对于两种林木根部病原菌,嗜铁素滤液各个浓度之间的抑制作用差异极显著(P < 0.05)。

|
| 图 7 不同水拉恩氏菌JZ-GX1嗜铁素发酵液稀释倍数的抑菌效果 Figure 7 The antagonism of different dilution times of siderophores produced by R. aquatilis JZ-GX1 against two pathogens 注:A:立枯丝核菌;B:樟疫霉;1、2、3、4、5分别代表阴性对照、阳性对照、嗜铁素发酵原液、10倍和100倍稀释液. Note: A: Rhizoctonia solani; B: Phytophthora cinnamomi; 1, 2, 3, 4, 5 represent negative control, positive control, stock solution, 10 times and 100 times dilution of siderophores respectively. |
|
|
| 病原 Pathogen |
阳性对照 Positive control |
原液 Stock solution |
10× | 100× |
| 立枯丝核菌Rhizoctonia solani | 100a | 100a | 51.08±0.48b | 26.36±3.31c |
| 樟疫霉Phytophthora cinnamomi | 100a | 100a | 93.33±1.36b | 68.98±2.23c |
| 注:表中数据为平均值±标准偏差,同一行中不同小写字母表示差异显著性(P < 0.05). Note: The datas represent means±SD, and different letters in the same line indicate significant difference (P < 0.05). |
||||
国内外已有一些关于嗜铁素产生菌筛选方面的报道,主要集中在假单胞菌属(Pseudomonas)[15-16]、芽孢杆菌属(Bacillus)[17]、伯克霍尔德菌属(Burkholderia)[18]、不动杆菌属(Acinetobacter)[19]等。微生物铁载体通常包括儿茶酚(Catchlate)、异羟肟酸(Hydroxamates)、羧酸盐型(Carboxylate-type) 3种类型[20],本研究首次鉴定拉恩氏属细菌(Rahnella aquatilis) JZ-GX1可以分泌羧酸盐型和异羟肟酸型两种嗜铁素,属于复合型铁载体,而对该铁载体的详细结构研究还需要进一步借助液质或气质联用等分析仪器进行分析。
产生嗜铁素被认为是植物根际促生菌最主要的直接和间接促进植物生长的有效途径之一,而嗜铁素的分泌受到多种因素的影响[21-22]。本试验对影响细菌嗜铁素分泌的几个因子进行了研究,发现培养基种类、初始pH、温度、发酵时间对水拉恩氏菌JZ-GX1嗜铁素产量有显著影响,说明碳氮源种类、土壤的理化性质对微生物功能的发挥起着至关重要的作用,这也就解释了一些实验室条件下拮抗效果良好的菌株在大田试验时生防效果却不稳定的现象。而接种量和装瓶量未造成JZ-GX1嗜铁素产量的显著变化,说明嗜铁素的分泌与初始接种量无关。氧的供应量在摇瓶到发酵罐的放大过程中是至关重要的[23],所以要确定合适的装瓶量还要进行大罐发酵试验。
从抑菌试验的结果可以看出,不加铁载体处理的供试病原菌生长最好,而添加去铁8-羟基喹啉之后菌丝完全没有生长,说明8-羟基喹啉将PDA培养基里的铁全部去除,病原菌的菌丝由于得不到铁营养而无法存活,水拉恩氏菌JZ-GX1产嗜铁素的发酵原液和PDA制成的带毒平板达到了相同的结果;而当稀释倍数为100×时,抑菌效果不显著,说明培养基中铁过多,有限的铁载体不能完全将铁占据,铁营养不成为病原菌生长的限制性因素,铁载体显然也没有作用。只有当细菌铁载体有能力将环境中的铁完全占据,这时候由于病原菌得不到铁,其生长就会受到影响暗示了微生物通过铁和铁载体在生态中搭建的真实关系,若病原菌和PGPR的铁载体螯合力及其分泌量相差不多时,谁优先控制了环境中的铁离子,谁就在铁营养的竞争中占据主动,而PGPR通过铁载体能够抑制病原菌的一个重要因素在于他们是土著菌,已经优先控制了周围有限的铁,如果他们主动侵入某一病原菌的领地,那么他们能否取得胜利还是一个未知数;当然,由于铁载体种类繁多,铁载体对铁的螯合能力相差很大,那些铁载体分泌能力非常强的微生物无疑在生态中占据及其明显的竞争优势[24]。
常媛等从八宝景天土壤中分离获得一株长枝木霉(Trichoderma longibrachiatum),采用平板对峙法测得该木霉对立枯丝核菌的抑菌率为58.56%[25]。罗同阳等发现产几丁质酶的枯草芽孢杆菌(Bacillus subtilis)对引起棉花立枯病的立枯丝核菌具有拮抗作用,提取的几丁质酶对菌丝生长抑制率为88.1%[26]。此次试验结果表明水拉恩氏菌JZ-GX1产嗜铁素的发酵液抑菌率更高,而关于樟疫霉的生防菌则属于首次报道。因此,水拉恩氏菌JZ-GX1在生产中抗病促生的应用潜力较大。
研究表明,利用微生物铁载体还可以防治植物在石灰性土壤上的缺铁黄化,Zhou等利用伯克霍尔德氏菌(Burkholderia cepacia)在低铁条件下有效改善黄芪的铁采集[27],进一步表明石灰性土壤上双子叶植物的缺铁失绿症状能够通过微生物分泌的铁载体缓解。有关JZ-GX1菌株对林木缺铁黄化和石灰性土壤上真菌病害的防治试验正在进行中,我们今后将对有关研究结果作进一步报道。
| [1] |
Liu YP, Teng SS, Zhao L. Identification of a siderophore-producing bacterium Pseudomonas putida A3 and its growth-promoting effects on cucumber seedlings[J]. Plant Nutrition and Fertilizer Science, 2011, 17(6): 1507-1514. (in Chinese) 刘艳萍, 滕松山, 赵蕾. 高产嗜铁素恶臭假单胞菌A3菌株的鉴定及其对黄瓜的促生作用[J]. 植物营养与肥料学报, 2011, 17(6): 1507-1514. |
| [2] |
Verbon EH, Trapet PL, Stringlis IA, et al. Iron and immunity[J]. Annual Review of Phytopathology, 2017, 55: 355-375. DOI:10.1146/annurev-phyto-080516-035537 |
| [3] |
Lin TX, Tang M, Huang MY, et al. Screening and identification of a high yield sideropho-res-producing bacteria SS05 isolated from cotton soil[J]. Microbiology China, 2012, 39(5): 668-676. (in Chinese) 林天兴, 唐梅, 黄明远, 等. 高产铁载体棉田土壤细菌SS05的筛选与鉴定[J]. 微生物学通报, 2012, 39(5): 668-676. |
| [4] |
Chen W, Shu JH, Chen Y, et al. Screening, identification and fermentation condition optimun of a siderophore-producing bacteria WN-H3 from rhizosphere of ryegrass[J]. Biotechnology Bulletin, 2016, 32(10): 219-226. (in Chinese) 陈伟, 舒健虹, 陈莹, 等. 黑麦草根际铁载体产生菌WN-H3的分离鉴定及其产铁载体培养条件的优化[J]. 生物技术通报, 2016, 32(10): 219-226. |
| [5] |
Tortora ML, Díaz-Ricci JC, Pedraza RO. Azospirillum brasilense siderophores with antifungal activity against Colletotrichum acutatum[J]. Archives of Microbiology, 2011, 193(4): 275-286. |
| [6] |
Chen W, Wang XL, Fu W, et al. Screening, identification and antagonistic against the pathogens of a siderophore-producing bacteria HMGY6B from rhizosphere of ryegrass[J]. Microbiology China, 2016, 43(10): 2207-2215. (in Chinese) 陈伟, 王小利, 付薇, 等. 黑麦草根际产铁载体细菌HMGY6B的筛选鉴定及对病原菌的拮抗作用[J]. 微生物学通报, 2016, 43(10): 2207-2215. |
| [7] |
Song FX, Wu XQ, Zhao Q. Antagonism of plant growth-promoting bacteria Rahnella aquatilis JZ-GX1 to canker in poplar[J]. Journal of Nanjing Forestry University (Natural Sciences Edition), 2017, 41(4): 42-48. (in Chinese) 宋芳旭, 吴小芹, 赵群. 水拉恩氏菌JZ-GX1对杨树溃疡病菌的拮抗作用[J]. 南京林业大学学报:自然科学版, 2017, 41(4): 42-48. |
| [8] |
Snow GA. Mycobactin. A growth factor for Mycobacterium johnei. Part Ⅱ. Degradation, and identification of fragments[J]. Journal of the Chemical Society, 1954, 2588-2596. DOI:10.1039/jr9540002588 |
| [9] |
Arnow LE. Colorimetric determination of the components of 3, 4-dihydroxyphenylalanine-tyrosine mixtures[J]. Journal of Biological Chemistry, 1937, 118(2): 531-537. |
| [10] |
Shenker M, Oliver I, Helmann M, et al. Utilization by tomatoes of iron mediated by a siderophore produced by Rhizopus arrhizus[J]. Journal of Plant Nutrition, 1992, 15(10): 2173-2182. DOI:10.1080/01904169209364466 |
| [11] |
Stookey LL. Ferrozine — a new spectrophotometric reagent for iron[J]. Analytical Chemistry, 1970, 42(7): 779-781. DOI:10.1021/ac60289a016 |
| [12] |
Machuca A, Milagres AMF. Use of CAS-agar plate modified to study the effect of different variables on the siderophore production by Aspergillus[J]. Letters in Applied Microbiology, 2003, 36(3): 177-181. DOI:10.1046/j.1472-765X.2003.01290.x |
| [13] |
Yu XM. Isolation of siderophore producing bacterium B. saubtilis CAS15 from the rhizosphere soil of rubber tree in Hainan island and cloning, expression and function analysis of the siderophore related gene dhbC[D]. Tai'an: Doctoral Dissertation of Shandong Agricultural University, 2009 (in Chinese) 余贤美.海南岛橡胶根际嗜铁细菌B. subtilis CAS15筛选及嗜铁素基因dhbC克隆、表达与功能分析[D].泰安: 山东农业大学博士学位论文, 2009 |
| [14] |
Han S, Zhang SC, Huang XY, et al. Antagonism of a siderophore-producing entophytic bacteria on Fusarium oxysporum[J]. Acta Botanica Boreali-Occidentalia Sinica, 2011, 31(5): 1039-1044. (in Chinese) 韩松, 张守村, 黄晓艳, 等. 一株产铁载体内生细菌对尖孢镰刀菌的拮抗作用[J]. 西北植物学报, 2011, 31(5): 1039-1044. |
| [15] |
Radzki W, Gutierrez Mañero FJ, Algar E, et al. Bacterial siderophores efficiently provide iron to iron-starved tomato plants in hydroponics culture[J]. Antonie van Leeuwenhoek, 2013, 104(3): 321-330. |
| [16] |
Nagata T, Oobo T, Aozasa O. Efficacy of a bacterial siderophore, pyoverdine, to supply iron to Solanum lycopersicum plants[J]. Journal of Bioscience and Bioengineering, 2013, 115(6): 686-690. DOI:10.1016/j.jbiosc.2012.12.018 |
| [17] |
Yu XM, Zhou GF, Xin L. Study on factors influencing the siderophore production of Bacillus subtilis BS-15 and effects of BS-15 on disease control and growth promotion of sweet pepper[J]. Chinese Journal of Pesticide Science, 2010, 12(2): 135-141. (in Chinese) 余贤美, 周广芳, 辛力. 枯草芽孢杆菌BS-15产嗜铁素条件及其对甜椒的防病促生效应[J]. 农药学学报, 2010, 12(2): 135-141. DOI:10.3969/j.issn.1008-7303.2010.02.04 |
| [18] |
Yang C. The conditions for siderophore producing of CAS19 and cloning and analysis of the siderophore synthesis-related gene cepR[D]. Haikou: Master's Thesis of Hainan University, 2010 (in Chinese) 杨岑.嗜铁菌CAS19产嗜铁素条件及其嗜铁素合成相关基因cepR的克隆与分析[D].海口: 海南大学硕士学位论文, 2010 |
| [19] |
Maindad DV, Kasture VM, Chaudhari H, et al. Characterization and fungal inhibition activity of siderophore from wheat rhizosphere associated Acinetobacter calcoaceticus strain HIRFA32[J]. Indian Journal of Microbiology, 2014, 54(3): 315-322. DOI:10.1007/s12088-014-0446-z |
| [20] |
Liu YP. Purification of siderophore produced by rhizobacteria and its role in plant growth promotion[D]. Jinan: Master's Thesis of Shandong Normal University, 2012 (in Chinese) 刘艳萍.植物根际促生菌嗜铁素的纯化及其促生机制的研究[D].济南: 山东师范大学硕士学位论文, 2012 |
| [21] |
Zhao RY, Zhao SZ, He HL. Factors influencing production of siderophore from Pseudomonas C-12[J]. Guizhou Agricultural Sciences, 2013, 41(1): 112-114. (in Chinese) 赵荣艳, 赵士振, 贺宏露. 嗜铁假单胞杆菌C-12产嗜铁素的影响因素[J]. 贵州农业科学, 2013, 41(1): 112-114. DOI:10.3969/j.issn.1001-3601.2013.01.034 |
| [22] |
Yi YJ, Zhou GZ, Shi Y, et al. Fermentation conditions of siderophore produced by Pseudomonas fluorescens RB5[J]. Journal of Henan University of Technology (Natural Science Edition), 2011, 32(6): 32-35, 39. (in Chinese) 伊艳杰, 周广舟, 时玉, 等. 荧光假单胞菌RB5产嗜铁素的发酵条件[J]. 河南工业大学学报:自然科学版, 2011, 32(6): 32-35, 39. |
| [23] |
Wang S. Plant growth promotion and control of plant disease with Bacillus spp. and lipopeptide[D]. Nanjing: Doctoral Dissertation of Nanjing Agricultural University, 2009 (in Chinese) 王帅.芽孢杆菌及其脂肽类化合物防治植物病害和促进植物生长的研究[D].南京: 南京农业大学博士学位论文, 2009 |
| [24] |
Xie XJ. Analysis of catechol-type iron carrier secreted by soil bacteria and its effect on pathogenic fungi[D]. Beijing: Doctoral Dissertation of China Agricultural University, 2006 (in Chinese) 谢小军.土壤细菌分泌的儿茶酚型铁载体分析及其对病原真菌作用的研究[D].北京: 中国农业大学博士学位论文, 2006 |
| [25] |
Chang Y, Yang XT, Jiang CY, et al. A Trichoderma longibrachiatum strain with antagonistic effects against three soil-borne pathogenic fungi[J]. Pratacultural Science, 2017, 34(2): 246-254. (in Chinese) 常媛, 杨兴堂, 姜传英, 等. 一株能拮抗3种土传病害病原真菌的长枝木霉[J]. 草业科学, 2017, 34(2): 246-254. |
| [26] |
Luo TY, Zheng X, Li B. Inhibition of chitinase-producing Bacillus subtilis against Rhizoctonia solan[J]. Modern Agricultural Science and Technology, 2014(22): 107-108. (in Chinese) 罗同阳, 郑翔, 李宾. 产几丁质酶枯草芽孢杆菌对立枯丝核菌的抑制作用研究[J]. 现代农业科技, 2014(22): 107-108. DOI:10.3969/j.issn.1007-5739.2014.22.063 |
| [27] |
Zhou C, Zhu L, Ma ZY, et al. Improved iron acquisition of Astragalus sinicus under low iron-availability conditions by soil-borne bacteria Burkholderia cepacia[J]. Journal of Plant Interactions, 2018, 13(1): 9-20. DOI:10.1080/17429145.2017.1407000 |
 2019, Vol. 46
2019, Vol. 46