扩展功能
文章信息
- 李飞, 张儒博, 徐雷, 朱玲, 徐志文
- LI Fei, ZHANG Ru-Bo, XU Lei, ZHU Ling, XU Zhi-Wen
- 猪链球菌2型感染仔猪致脑炎模型的建立
- Establishment of a model of encephalitis caused by Streptococcus suis type 2 infection in piglets
- 微生物学通报, 2019, 46(11): 3070-3075, 3083
- Microbiology China, 2019, 46(11): 3070-3075, 3083
- DOI: 10.13344/j.microbiol.china.181035
-
文章历史
- 收稿日期: 2018-12-19
- 接受日期: 2019-02-01
- 网络首发日期: 2019-04-03
2. 动物疫病与人类健康四川省重点实验室 四川 成都 611130
2. Sichuan Key Laboratory of Animal Disease and Human Health, Chengdu, Sichuan 611130, China
猪链球菌(Streptococcus suis)可以引起猪的急性败血症、脑膜炎、关节炎、心内膜炎以及突然死亡,也可以导致人类感染和死亡,是一种重要的人兽共患传染病病原[1],迄今为止,已知基于猪链球菌荚膜抗原有35种血清型,猪链球菌血清型2是最具毒性和最主要的致病血清型[2]。我国《动物防疫法》把该病列为国家二类传染病。1998年在江苏地区[3]部分猪场暴发链球菌感染,经鉴定病原为猪链球菌2型;2005年7月到8月期间在四川地区暴发链球菌感染猪和人的病例,人感染204例,死亡38例[4-5];2013年3月至5月,在江苏省多个大型养猪场暴发了仔猪链球菌病,并在30日龄仔猪中诱发脑膜炎[6];给我国养猪行业造成了巨大的经济损失。自然病例具有随机单一性和不可控的多重感染和继发感染,同时发病程度因个体差异而存在较大不同,导致病理变化不具有代表性。因此,迫切需要构建出一种重复性好,能模拟自然感染情况下猪的临床症状及病理变化的模型。仔猪具有易感染、易操作、易获得等优点,本研究用三元杂交仔猪构建了致病性猪链球菌2型感染模型,通过临床观察、剖检观察、组织切片观察、细菌分离及PCR鉴定,证明该模型能成功模拟自然感染下仔猪的自然状态。
1 材料与方法 1.1 试验动物6头健康状况良好的5周龄三元杂交公猪购自四川农业大学合作猪场,经检测SS、PCV2、PCV3、PRRSV、PPV、PRV、CSFV、JEV、HEV均为阴性。观察7 d后用于试验。
1.2 主要试剂和仪器2×Taq PCR Master Mix、ddH2O、DL2000 DNA Marker、pMD19-T载体、Solution Ι、16S rRNA基因引物以及各规格的培养板和培养基,生工生物工程(上海)股份有限公司;细菌DNA提取试剂盒、胶回收试剂盒、质粒提取试剂盒,TIANGEN公司;DH5α感受态细胞,四川农业大学动物生物技术中心保存;切片制作试剂:苏木素和伊红,Thermo Fisher公司;无水乙醇、95%乙醇、二甲苯、多聚甲醛,成都市科隆化学品有限公司。
PCR仪、Gel DocTM EZ imager凝胶成像系统,Bio-Rad公司;电热恒温培养箱,上海齐欣科学仪器有限公司;电泳仪,北京市六一仪器厂;正置显微镜DM500、石蜡切片机,Leica公司。
1.3 菌株猪链球菌2型为2005年四川分离株SSsc0501,由四川农业大学动物生物技术中心保存。
取保存菌株接种于含5%犊牛血清的TSA平板,37 ℃培养18-24 h后用无菌生理盐水洗下菌落,按OD600=1×109 CFU/mL计算,制备成5×106 CFU/mL细菌悬液,4 ℃保存,4 h之内用于接种试验动物。
1.4 动物分组与接种选取6头5周龄健康仔猪,随机将其分为A、B两组,A组3头,B组3头。A组仔猪经静脉接种预先配置浓度为5×106 CFU/mL的细菌悬液2 mL,B组接种等量生理盐水,为防止交叉感染,A、B两组隔离饲养。
1.5 病理学观察 1.5.1 临床观察从接种猪链球菌开始每天记录仔猪的直肠体温以及观察仔猪的临床症状。
1.5.2 解剖观察在仔猪接种36 h后,采用前腔静脉抽血致死法剖杀仔猪,待猪死后剖开胸腔、腹腔和脑腔,观察下颌淋巴结、心、肝、脾、肺、肾、腹股沟淋巴结、大脑、小脑等器官组织的形态、颜色、质地等病理形态学变化。
1.5.3 组织切片观察无菌采集A组剖杀仔猪的大脑、脊髓、肺脏、下颌淋巴结等组织,经福尔马林溶液固定后,进行常规石蜡包埋、切片以及HE染色。光学显微镜下观察组织的病理学变化,并拍照、记录。
1.6 病原分离及PCR鉴定无菌采集A、B两组的大脑,在含5%犊牛血清的TSA培养基上划线,培养24 h后挑取疑似菌落进行革兰氏染色和镜鉴。
用细菌16S rRNA基因通用引物27F (5′-AGA GTTTGATCCTGGCTCAG-3′)和1492R (5′-GGTTAC CTGTTACGACTT-3′)扩增分离菌的16S rRNA基因,预期扩增长度为1 465 bp。PCR反应体系(30 μL):上、下游引物(20 μmol/L)各0.5 μL,细菌基因组(317 ng/μL) 2 μL,2×Taq PCR Master Mix 15 μL,ddH2O 12 μL。PCR反应条件:95 ℃ 5 min;95 ℃ 30 s,55 ℃ 30 s,72 ℃ 45 s,30个循环;72 ℃ 7 min。
PCR产物经琼脂糖凝胶电泳后用胶回收试剂盒回收片段,并与pMD19-T载体连接过夜(16 ℃),转化大肠杆菌DH5α感受态细胞,用蓝白斑筛选阳性克隆后送至成都擎科生物技术公司测序。将测序的结果在NCBI上进行BLAST比对。
2 结果与分析 2.1 临床观察A组仔猪在接种猪链球菌后12 h开始出现发病,在接种后36 h剖杀仔猪。发病期间体温高达40.5±0.5 ℃,在发病早期表现出精神沉郁、食欲减退、嗜睡,之后出现站立不稳突然倒地等症状,很快发展到严重的神经症状,如后肢瘫痪、角弓反张、四肢呈现划水样等。B组仔猪无发病症状。
2.2 解剖观察剖杀A组仔猪,可见皮下出血,血液凝固不良;肺脏表面有出血点或淤血;下颌淋巴结、腹股沟淋巴结、肠系膜淋巴结出现肿大,呈现暗红色或紫黑色;大脑和小脑出现明显充血出血。B组仔猪内脏器官和脑部均未发现明显病变。
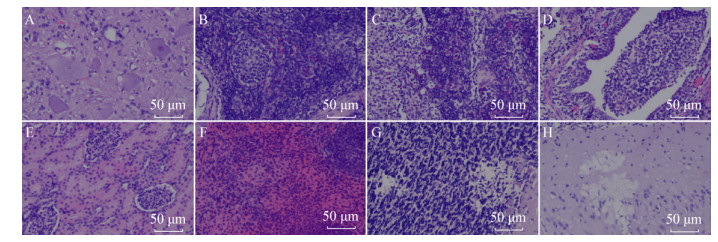
2.3 组织切片观察感染仔猪的组织切片分析如下:(1)脊髓:脊髓的灰质见有神经元细胞的肿胀,核染色质溶解;白质区神经元细胞坏死溶解,胶质细胞增生(图 1A)。(2)下颌淋巴结:下颌淋巴结低倍镜下见有淋巴小结和较多的周围组织,淋巴结组织内见有较多的嗜酸性粒细胞弥漫性浸润(图 1B)。(3)腹股沟淋巴结:腹股沟淋巴结见有较多淋巴小结和副皮质区,淋巴结组织内见有较多的嗜酸性粒细胞弥漫性浸润(图 1C)。(4)肺:肺脏终末细支气管管腔中见有大块的脓性细胞团块聚集(图 1D)。(5)肾:肾小球、肾小囊及各级肾小管组织结构正常,未见有明显病理损伤(图 1E)。(6)脾:脾脏组织红髓区和白髓区分界清楚,未见任何明显的病理学变化(图 1F)。(7)小脑:小脑髓质区结构正常,灰质区浦肯野细胞层和颗粒层见细胞灶状坏死并形成坏死后空腔,腔内见较多的细胞核碎片,以颗粒层较为多见(图 1G)。(8)大脑:大脑皮质区神经元细胞坏死溶解,形成网状空腔,腔内可见有细胞核碎片(图 1H)。
|
| 图 1 感染仔猪组织切片 Figure 1 Infected piglet tissue section 注:A:脊髓,灰质区神经元细胞肿大,胞核轮廓消失;B:下颌淋巴结,组织结构正常,未见明显组织病理损伤;C:腹股沟淋巴结,组织结构正常,未见明显组织病理损伤;D:肺脏,终末细支气管管腔中有脓性细胞团块;E:肾脏,组织结构正常,未见明显病理损伤;F:脾脏,组织结构正常,未见明显病理损伤;G:小脑,浦肯野细胞层核颗粒层见有细胞坏死,坏死灶内较多核碎片;H:大脑,皮质区神经元细胞坏死溶解,形成空腔. Note: A: Spinal cord, gray matter area, neuronal cell enlargement, nuclear contour disappeared; B: Mandibular lymph node, normal tissue structure, no obvious histopathological damage; C: Inguinal lymph node, normal tissue structure, no obvious histopathological damage; D: Lung, there are purulent cell masses in the end of the bronchioles; E: Kidney, normal tissue structure, no obvious pathological damage; F: Spleen, normal tissue structure, no obvious pathological damage; G: Cerebellum, there are cell necrosis in the nuclear layer of Purkinje cell layer, and more nuclear fragments in the necrotic foci; H: Nervous cells in the brain and cortex are necrotic and dissolve, forming a cavity. |
|
|
观察平板可见B组无细菌生长;A组可见划线处均匀长出灰白色、光滑、整齐、半透明、针尖大小的菌落,革兰氏染色为阳性球菌,呈现为双球型和短链状排列。
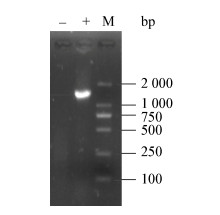
根据16S rRNA基因引物序列扩增相应1 465 bp的片段大小(图 2)。
|
| 图 2 16S rRNA基因的PCR扩增 Figure 2 The PCR amplication of 16S rRNA gene 注:-:阴性对照;+:疑似链球分离菌株;M:DL2000分子标准. Note:-: Negative control; +: Suspected Streptococcus isolated strain; M: DL2000 DNA Marker. |
|
|
将所得测序结果进行BLAST比对,16S rRNA基因与Streptococcus suis strain ATCC 43765 16S ribosomal RNA gene (NR_115737.1)以及Streptococcus suis strain S735 16S ribosomal RNA gene (NR_036918.1)等菌株的16S RNA基因相似性达99%,仅有8个碱基差别,证明该菌株为猪链球菌。
3 讨论与结论随着养猪行业规模化养殖的发展,猪链球菌2型的感染及流行严重影响了我国养猪业的发展。由于不同来源猪链球菌2型的致病性复杂且多变,导致猪链球菌2型动物模型的建立是个难题,虽然国内外关于猪链球菌2型动物模型的报道很多,但看法与结果也各不相同。2005年桂炳东[7]研究发现用猪链球菌2型18 h培养物腹腔注射小白鼠,未出现发病和死亡,由此认为小鼠为非理想模型;2001年王继春等[8]研究发现普通小鼠只引起一过性精神萎顿,6 h后恢复正常,认为普通小鼠对猪链球菌2型不敏感;Vecht等[9]研究发现对猪具有高毒力的猪链球菌菌株在小鼠中引起高发病率和中度死亡率,对猪具有弱毒性的猪链球菌菌株导致小鼠高发病率和低死亡率,但对猪无毒力的猪链球菌菌株导致小鼠高发病率和死亡率,因此认为小鼠不适合作为猪链球菌的动物模型;吴全忠等[10]研究发现用江苏分离株HA9801接种普通小鼠及BALB/c小鼠,均无致病性,家兔虽可感染,但发病死亡极不规律,豚鼠同群感染时间比仔猪晚,证明豚鼠的易感性低于仔猪。目前,国内外也有很多学者用猪作为实验动物,采用不同的感染途径,如鼻腔接种、静脉接种、肌肉接种等[11-12],鼻腔接种未能引起全身性的感染,静脉注射的实验组死亡时间最早;2003年Pallarés等[13]研究发现仔猪静脉接种更易导致仔猪脑膜炎的产生。
本研究之所以采用静脉接种作为接种途径,是因为猪链球菌在没有穿过黏膜上皮细胞毛细血管之前,一般不会引起感染[11],且静脉注射更容易导致仔猪脑膜炎。静脉接种猪链球菌,使病原直接进入血液,在血液循环中进行繁殖,能迅速到达全身各器官组织引起菌血症。2005年Tenenbaum等[14]研究发现猪链球菌分离株在体外模型中诱导血-脑脊液屏障功能的丧失,可以促进细菌和白细胞穿过血-脑脊液屏障。在临床中我们也观察到仔猪静脉接种后迅速出现了嗜睡、精神沉郁、食欲减退等症状,在发病后期出现严重的神经症状,如后肢瘫痪、角弓反张、四肢呈现划水样等;在剖检时也发现大量的脑脊液,大脑和小脑严重充血出血;通过组织病理学分析发现大脑神经元肿胀坏死形成空腔,小脑浦肯野细胞层和颗粒层见有细胞坏死,坏死灶内较多核碎片;空白组没有出现上述的症状;推断猪链球菌2型对猪的中枢神经系统造成了损伤,表明在仔猪上成功模拟了脑炎的症状。通过临床观察、解剖观察及组织学观察发现仔猪血液凝固不良;皮下、浆膜、黏膜不同程度的出血或淤血;淋巴结出现肿胀而呈现暗红色或紫黑色,弥漫性浸润大量的炎性细胞;肺脏终末细支气管管腔中见有大块的脓性细胞团块聚集;表明在仔猪上成功模拟了败血症的症状。
目前为止,已经有了许多猪链球菌2型动物模型建立的报道,如BALB/c小鼠模型[15]、斑马鱼模型[16]、豚鼠模型[10]等,每种模型都有其特点,但是这些动物有很多局限性,难以复制出猪链球菌2型感染的典型脑炎症状,所以还要对动物模型进行深入的研究和改良,以致反应出在自然情况下动物感染猪链球菌最真实的临床症状和病理变化。本次试验的研究结果成功模拟了败血症和脑炎症状,重复性好,表现出来的症状也与自然感染表现出的症状相一致。另外,仔猪具有体型小,易于饲养和操作等优点,给试验带来了极大的便利。因此,本试验的研究结果对于猪链球菌2型动物模型的建立具有重要的意义。
| [1] |
Staats JJ, Feder I, Okwumabus O, et al. Streptococcus suis: past and present[J]. Veterinary Research Communications, 1997, 21(6): 381-407. DOI:10.1023/A:1005870317757 |
| [2] |
Guo CN, Liao XP, Wang MR, et al. In vivo pharmacodynamics of cefquinome in a neutropenic mouse thigh model of Streptococcus suis serotype 2 at varied initial inoculum sizes[J]. Antimicrobial Agents and Chemotherapy, 2015, 60(2): 1114-1120. |
| [3] |
Ou Y, Lu CP. Analysis of virulence-related proteins of Streptococcus suis type 2 from swine Streptococcus isolatrd in China[J]. Acta Microbiologica Sinica, 2002, 42(1): 105-109. (in Chinese) 欧瑜, 陆承平. 猪链球菌2型国内分离株毒力相关蛋白的分析[J]. 微生物学报, 2002, 42(1): 105-109. DOI:10.3321/j.issn:0001-6209.2002.01.017 |
| [4] |
Xu K, Wang W, Wen XT, et al. Epidemiological investigation of swine Streptococcus suis type 2 in Sichuan region[J]. Chinese Journal of Preventive Veterinary Medicine, 2017, 39(5): 370-373. (in Chinese) 徐魁, 王巍, 文心田, 等. 四川主要养猪地区猪2型链球菌血清流行病学调查[J]. 中国预防兽医学报, 2017, 39(5): 370-373. |
| [5] |
Wang ZZ, Yu Y, Cheng J, et al. Epidemiological investigation of porcine streptococcosis in Sichuan Province[J]. Chinese Journal of Veterinary Science, 2006, 36(6): 502-506. (in Chinese) 王泽洲, 余勇, 程江, 等. 四川省猪链球菌病的流行病学调查[J]. 中国兽医科学, 2006, 36(6): 502-506. |
| [6] |
Pan ZH, Ma JL, Dong WY, et al. Novel variant serotype of Streptococcus suis isolated from piglets with meningitis[J]. Applied and Environmental Microbiology, 2015, 81(3): 976-985. DOI:10.1128/AEM.02962-14 |
| [7] |
Gui BD. Laboratory diagnosis of human-swine streptococcosis[J]. Jiangxi Medical Examination, 2005, 23(5): 463-466. (in Chinese) 桂炳东. 人-猪链球菌病的实验室诊断[J]. 江西医学检验, 2005, 23(5): 463-466. DOI:10.3969/j.issn.1674-1129.2005.05.032 |
| [8] |
Wang JC, He KW, He JH, et al. Test on the pathogenicity of Streptococcus suis type 2[J]. Chinese Journal of Veterinary Science and Technology, 2001, 31(12): 23-25. (in Chinese) 王继春, 何孔旺, 何家惠, 等. 2型猪链球菌动物致病性试验[J]. 中国兽医科技, 2001, 31(12): 23-25. DOI:10.3969/j.issn.1673-4696.2001.12.009 |
| [9] |
Vecht U, Stockhofe-Zurwieden N, Tetenburg BJ, et al. Virulence of Streptococcus suis type 2 for mice and pigs appeared host-specific[J]. Veterinary Microbiology, 1997, 58(1): 53-60. DOI:10.1016/S0378-1135(97)00131-4 |
| [10] |
Wu QZ, Tian Y, Lu CP. Guinea-Pig model of Streptococcus suis type 2 induced meningitis and septicaemia[J]. Chinese Journal of Veterinary Science, 2002, 22(3): 228-230. (in Chinese) 吴全忠, 田云, 陆承平. 猪链球菌2型引致脑炎及败血症的豚鼠模型[J]. 中国兽医学报, 2002, 22(3): 228-230. DOI:10.3969/j.issn.1005-4545.2002.03.007 |
| [11] |
Zhou K, Li ZM, Li JH, et al. Comparison of five infection routes of Streptococus suis type 2 in pigs[J]. Chinese Journal of Animal Infectious Diseases, 2016, 24(2): 35-41. (in Chinese) 周康, 李宗明, 李江华, 等. 猪链球菌Ⅱ型五种感染途径感染猪模型的比较[J]. 中国动物传染病学报, 2016, 24(2): 35-41. DOI:10.3969/j.issn.1674-6422.2016.02.007 |
| [12] |
Berthelot-Héraulta F, Gottschalk M, Labbéa A, et al. Experimental airborne transmission of Streptococcus suis capsular type 2 in pigs[J]. Veterinary Microbiology, 2001, 82(1): 69-80. DOI:10.1016/S0378-1135(01)00376-5 |
| [13] |
Pallarés FJ, Halbur PG, Schmitt CS, et al. Comparison of experimental models for Streptococcus suis infection of conventional pigs[J]. Canadian Journal of Veterinary Research, 2003, 67(3): 225-228. |
| [14] |
Tenenbaum T, Adam R, Eggelnpöhler I, et al. Strain-dependent disruption of blood-cerebrospinal fluid barrier by Streptoccocus suis in vitro[J]. FEMS Immunology and Medical Microbiology, 2005, 44(1): 25-34. DOI:10.1016/j.femsim.2004.12.006 |
| [15] |
Zhang YQ, Liu WQ, Liu YS, et al. Experimental animal models of BALB/c mice infected with Streptococcus suis[J]. Chinese Journal of Zoonoses, 2011, 27(5): 418-422. (in Chinese) 张奕强, 刘文倩, 刘永生, 等. 猪链球菌BALB/c小鼠感染模型的初步建立[J]. 中国人兽共患病学报, 2011, 27(5): 418-422. DOI:10.3969/j.issn.1002-2694.2011.05.013 |
| [16] |
Pu JY, Huang XX, Lu CP. Virulence detection of Streptococcus suis type 2 in zebrafish[J]. Chinese Agricultural Science, 2007, 40(11): 2655-2658. (in Chinese) 濮俊毅, 黄新新, 陆承平. 用斑马鱼检测猪链球菌2型的致病力[J]. 中国农业科学, 2007, 40(11): 2655-2658. DOI:10.3321/j.issn:0578-1752.2007.11.036 |
 2019, Vol. 46
2019, Vol. 46