扩展功能
文章信息
- 张中耀, 王爽, 孙策, 魏云林, 林连兵, 张琦, 季秀玲
- ZHANG Zhong-Yao, WANG Shuang, SUN Ce, WEI Yun-Lin, LIN Lian-Bing, ZHANG Qi, JI Xiu-Ling
- 流式细胞仪检测纳帕海高原湿地浮游病毒和浮游细菌丰度
- Determination of virioplankton and panktonic bacteria abundance in the Napahai plateau wetland by flow cytometry
- 微生物学通报, 2018, 45(5): 1007-1015
- Microbiology China, 2018, 45(5): 1007-1015
- DOI: 10.13344/j.microbiol.china.170480
-
文章历史
- 收稿日期: 2017-07-03
- 接受日期: 2017-10-12
- 网络首发日期(www.cnki.net): 2017-11-02
浮游病毒是指浮游于水体中的一切病毒的总称,主要包括噬菌体、噬藻体和浮游植物病毒,由于其能裂解宿主,变有机质为无机质,所以在调节水体中微生物物种多样性、参与地球物质循环和介导微生物之间的基因水平转移等方面具有重要作用[1-10]。因此,浮游病毒是水体微生物群落中重要的组成成分。目前浮游病毒的研究越来越受到国内外学者的重视,关于其研究主要集中在浮游病毒的丰度、分布及其与浮游细菌和环境的相关性研究、浮游病毒的多样性研究这几个方面[11-13]。但大多数研究集中在海洋、河流入海口及近海区域,关于湿地尤其是高原湿地的研究鲜有报道[14-15]。
纳帕海高原湿地地处青藏高原的东南延伸部分,是金沙江流域云南西北高原低纬度高海拔的季节性沼泽湿地,为中国湿地的独特类型。作为我国少有的低纬度高海拔湿地,具有很高的科学研究价值。目前已经有很多学者相继对纳帕海湿地开展了湿地季节性景观格局动态变化及其驱动[16]、湖滨带优势植物生物量及其凋落物分解[17]、土壤有机碳密度及碳储量特征[18],以及气候变化对纳帕海湿地的影响[19]等方面的研究,但关于纳帕海湿地浮游病毒与浮游细菌丰度及其与其他环境因子相关性研究尚未见报道。本研究拟通过流式细胞仪来检测纳帕海湿地不同季节浮游病毒与浮游细菌丰度并分析其与叶绿素a (Chl-a)等环境因子的相关性。
1 材料与方法 1.1 样品采集、固定及保存分别于2013年12月(旱季)和2014年9月(雨季)采集纳帕海高原湿地(E99°37′22″-E99°38′16″,N27°50′01″-N27°53′35″)的7个水样样品。其中,YW代表原水;YNW代表淤泥水;SDW代表湿地水。采集到的水样分别加入DNaseⅠ和RNase A至终浓度为1 g/mL,37 ℃消化30 min,加25%的戊二醛至终浓度为0.5% (体积比),4 ℃避光固定15 min后迅速放入液氮冷冻,于-80 ℃长期保存。
1.2 主要试剂和仪器SYBR Green Ⅰ染料,上海安妍生物有限公司;0.45 μm (硝酸纤维素,16541-K)滤膜、0.22 μm (硝酸纤维素,16553-K)滤膜、0.45 μm (醋酸纤维素,11104-13-N)滤膜,Sartorius公司。流式细胞仪,美国贝克曼库尔特公司;等离子体发射光谱质谱仪,Perkinelmer公司;荧光显微镜,尼康公司。
1.3 分析方法现场测定样品温度和pH。
元素测定由农业部农产品质量监督检测测试中心(昆明)完成。采用等离子体发射光谱质谱仪测定水样中的元素含量:水样经0.45 μm (硝酸纤维素,16541-K)滤膜抽滤后用HNO3酸化,贮存于PET塑料瓶中。将水样分成两份,其中一份加入一定量的标准溶液,分别测定两份水样中各元素的浓度,计算其加标回收率。用Sc、Ge、In、Tb、Bi作内标,浓度为50 ng/L。
采用丙酮提取法测定叶绿素a (Chl-a)的含量[20]:取40 mL水样,经0.45 μm (醋酸纤维素,11104-13-N)滤膜过滤,抽滤浓缩藻类于滤膜上,将滤膜对折装袋,避光保存。先置于-20 ℃冰冻12 h,室温下解冻5 min,直至滤膜变软。然后在-20 ℃冰冻约20 min,室温下解冻,反复冻融3-5次后,放入盛有10 mL 90%丙酮的避光离心管中,上下颠倒1 min混匀,直至滤膜完全溶解。将离心管于4 ℃中浸提20 h,浸提过程中需振摇1-2次。浸提后离心管于4 000 r/min离心15 min。分别在630、645、663和750 nm波长处测定离心管上清液的吸光度,通过公式:Chl-a浓度=12.7A663-2.69A645计算叶绿素a (Chl-a)的浓度(mg/L)。
1.4 流式细胞仪测样品中浮游病毒和浮游细菌丰度将用0.22 μm (硝酸纤维素,16553-K)的滤膜抽滤过的pH 8.0的TE缓冲液作为稀释液,分别将样品和SYBR Green I 10 000×稀释到100×。稀释过的每个样品取400 μL,向其中加100×染液至终浓度为0.5×。常温避光染色5 min,80 ℃水浴孵育10 min后避光冷却至室温,样品从侧向角SSC和通道FL1经流式细胞仪检测浮游病毒和浮游细菌丰度。同一样点样品,用0.22 μm滤膜(硝酸纤维素,16553-K)过滤前后分别上样检测。
1.5 浮游病毒丰度与浮游细菌丰度、Chl-a及环境因子相关性分析采用SPSS 17.0软件用Pearson相关系数分析纳帕海湿地环境因子之间、浮游病毒与环境因子之间的关系。采用R语言1.7分析旱雨两季水样浮游病毒丰度与浮游细菌及环境因素线性回归。
2 结果与分析 2.1 水样旱季和雨季各元素的测定旱季和雨季水样元素由农业部农产品质量监督检验测试中心(昆明)测定。由表 1和表 2可知:在进行元素含量测定过程中,有一些元素未检测出来,可能是水体元素检测要尽可能早地进行测定,否则水体中的生物作用可能会对某些元素的含量造成影响(中华人民共和国国家环境保护标准,HJ 493-2009,《水质采样样品的保存和管理技术规定》)。因此只针对检测出的水样元素进行统计学分析。
| 样品 Samples |
氮 N |
磷 P |
锌 Zn |
铁 Fe |
锰 Mn |
镁 Mg |
钙 Ca |
铜 Cu |
钠 Na |
钾 K |
| SDW-1 | 6.74 | 1.430 | 0.265 | 33.00 | 0.625 | 8.87 | 41.3 | 0.068 0 | 7.73 | 24.80 |
| SDW-2 | 1.35 | 0.158 | 0.033 | 8.31 | 0.238 | 6.92 | 34.1 | 0.008 0 | 3.14 | 3.30 |
| YNW-1 | 4.04 | 0.773 | 0.032 | 7.99 | 0.430 | 6.00 | 22.8 | 0.011 0 | 17.80 | 6.14 |
| YNW-2 | 33.70 | 9.190 | 0.912 | 123.00 | 3.970 | 23.00 | 92.4 | 0.412 0 | 7.20 | 1.83 |
| YW-5 | 0 | - | - | - | - | 5.90 | 45.7 | 0.035 4 | 9.90 | 3.04 |
| YW-6 | 0 | - | - | - | - | 5.00 | 45.6 | 0.004 0 | 9.80 | 3.47 |
| YW-7 | 0 | - | - | - | - | 6.12 | 44.9 | 0.006 0 | 9.85 | 2.88 |
| 注:YW:原水;SDW:湿地水;YNW:淤泥水;-:未检出元素,单位均为mg/L. Note: YW: Raw water; SDW: Wetland water; YNW: Silt water; -: No elements detected, units are mg/L. | ||||||||||
| 样品 Samples |
氮 N |
磷 P |
锌 Zn |
铁 Fe |
锰 Mn |
镁 Mg |
钙 Ca |
铜 Cu |
钠 Na |
钾 K |
| SDW-1 | 1.34 | - | - | 0.838 | - | 3.45 | 29.5 | - | 2.32 | 0.790 |
| SDW-2 | 2.67 | - | - | 0.552 | - | 4.14 | 43.0 | - | 1.41 | 0.592 |
| YNW-1 | 0.00 | - | - | - | - | 4.45 | 34.4 | - | 9.08 | 5.120 |
| YNW-2 | 0.00 | - | - | - | - | 5.20 | 33.2 | - | 7.20 | 1.830 |
| YW-5 | 0.00 | - | - | - | - | 4.86 | 26.0 | - | 4.62 | 2.660 |
| YW-6 | 2.67 | - | - | - | - | 5.04 | 23.1 | - | 4.40 | 2.110 |
| YW-7 | 0.00 | - | - | 0.074 | - | 4.78 | 28.2 | - | 4.56 | 2.660 |
如表 3所示,纳帕海湿地具有典型的高原气候特征,太阳辐射强,气温年较差小(平均16 ℃),而日较差大(平均可达20 ℃,旱季时可达30 ℃),年均温为5.4 ℃。纳帕海湿地雨季和旱季采样样品温度差异较大,雨季温度较高。
| 样品 Samples |
旱季 Dry season |
雨季 Rainy season |
|||
| 酸碱度 pH |
温度 Temperature (℃) |
酸碱度 pH |
温度 Temperature (℃) |
||
| SDW-1 | 5.5 | 9.0 | 7.0 | 27 | |
| SDW-2 | 6.0 | 9.0 | 7.0 | 27 | |
| YNW-1 | 6.6 | 7.5 | 6.0 | 19 | |
| YNW-2 | 5.5 | 6.0 | 6.0 | 19 | |
| YW-5 | 6.0 | 8.0 | 6.0 | 23 | |
| YW-6 | 5.5 | 9.0 | 6.0 | 25 | |
| YW-7 | 6.0 | 5.0 | 6.0 | 22 | |
分别对旱季和雨季的水样中的Chl-a含量进行测定。由表 4可知,样品中雨季Chl-a的含量明显高于旱季。YNW (淤泥水)样品中的Chl-a的含量要远高于YW (原水)和SDW (湿地水)样品。
| 样品 Samples |
Chl-a含量 Chlorophyll a content (mg/L) |
|
| 旱季 Dry season |
雨季 Rainy season |
|
| SDW-1 | 0.098 | 0.121 |
| SDW-2 | 0.010 | 0.075 |
| YNW-1 | 0.768 | 1.056 |
| YNW-2 | 1.732 | 1.875 |
| YW-5 | 0.105 | 0.263 |
| YW-6 | 0.207 | 0.162 |
| YW-7 | 0.144 | 0.190 |
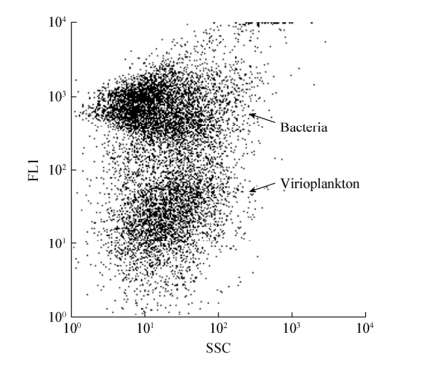
对采集到的样品和经0.22 μm滤膜(硝酸纤维素,16553-K)过滤的浮游病毒的样品分别利用流式细胞仪确定浮游病毒与浮游细菌区域。
由图 1可知,经0.22 μm滤膜(硝酸纤维素,16553-K)过滤后,在FL1 102-103荧光级别上的颗粒物明显减少,因此推断此区域为细菌所在区域;由于浮游病毒颗粒小,核酸量相对也少,所以推测荧光级别FL1 100-102为浮游病毒所在区域。
|
| 图 1 浮游病毒和浮游细菌的定位 Figure 1 Position of virioplankton and planktonic bacteria |
|
|
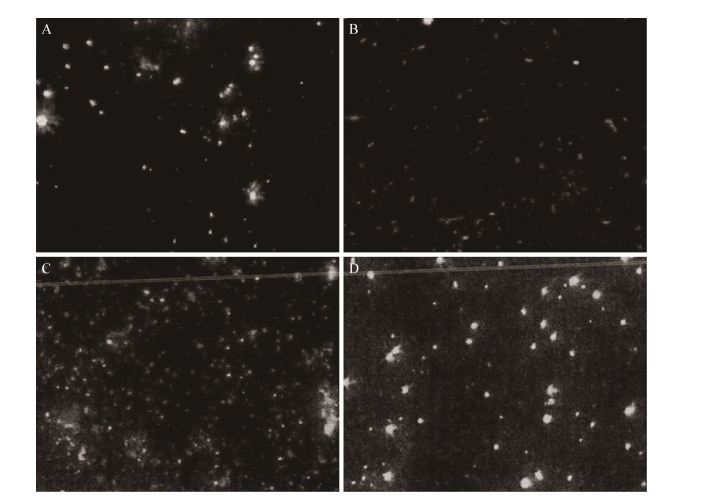
采用SYBR Green Ⅰ染料对纳帕海湿地采集的样品进行染色,用流式细胞仪对旱季和雨季浮游病毒和浮游细菌进行计数(图 1),同时在荧光显微镜下计数浮游细菌和浮游病毒(图 2)。无论在雨季还是旱季,浮游病毒丰度变化趋势和浮游细菌丰度趋于一致,所以初步断定浮游细菌丰度是影响浮游病毒丰度变化的重要因素之一。
|
| 图 2 纳帕海高原湿地浮游病毒与浮游细菌的荧光照片 Figure 2 The fluorescence picture of virioplankton and planktonic bacteria in the Napahai plateau wetland 注:A:旱季SDW-1浮游细菌;B:旱季SDW-1浮游病毒;C:雨季SDW-2浮游病毒;D:雨季SDW-2浮游细菌. Note: A: Planktonic bacteria of SDW-1 in dry season; B: Virioplankton of SDW-1 in dry season; C: Virioplankton of SDW-2 in rainy season; D: Planktonic bacteria of SDW-2 in rainy season. |
|
|
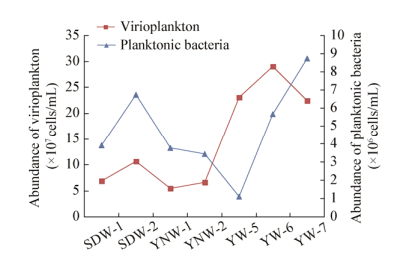
水样浮游病毒与浮游细菌丰度计数结果见表 5。旱季和雨季水样的浮游病毒丰度范围分别为1.35×106-8.46×106个/mL和6.86×107-2.91×108个/mL;浮游细菌丰度范围分别为2.57×105-4.63×105个/mL和1.14×106-8.75×106个/mL。旱季和雨季水样浮游病毒和浮游细菌变化情况如图 3-5所示。在季节分布上,雨季水样的浮游病毒丰度明显高于旱季。旱季淤泥-1水样(YNW-1)与原水-7 (YW-7)之间浮游病毒丰度是呈现增长趋势的,而雨季增加的尤其明显。这可能是由于雨季降水量增多从而导致样品水样温度、pH值等理化性质发生变化。原水-5 (YW-5)、原水-6 (YW-6)和原水-7 (YW-7)旱、雨两季的浮游病毒丰度较高。由图 4和图 5比较可得,雨季测得的浮游病毒和浮游细菌的丰度明显要比旱季的浮游病毒和浮游细菌的丰度高出10倍。其中,原水-5 (YW-5)、原水-6 (YW-6)和原水-7 (YW-7)这3个区域雨季的浮游病毒和浮游细菌丰度要比旱季高得多,可能是由于附近存在着大批水域。
| 样品 Samples |
旱季 Dry season |
雨季 Rainy season |
|||
| 浮游病毒丰度 Abundance of virioplankton (cells/mL) |
浮游细菌丰度 Abundance of planktonic bacteria (cells/mL) |
浮游病毒丰度 Abundance of virioplankton (cells/mL) |
浮游细菌丰度 Abundance of planktonic bacteria (cells/mL) |
||
| YW-5 | 3.54×106 | 2.87×105 | 2.31×108 | 1.14×106 | |
| YW-6 | 5.78×106 | 3.58×105 | 2.91×108 | 5.68×106 | |
| YW-7 | 8.46×106 | 4.63×105 | 2.25×108 | 8.75×106 | |
| SDW-1 | 1.65×106 | 2.57×105 | 6.86×107 | 3.95×106 | |
| SDW-2 | 1.35×106 | 3.06×105 | 1.07×108 | 6.74×106 | |
| YNW-1 | 3.36×106 | 2.82×105 | 5.46×107 | 3.77×106 | |
| YNW-2 | 2.22×106 | 4.55×105 | 6.67×107 | 3.47×106 | |

|
| 图 3 旱季和雨季浮游病毒变化情况 Figure 3 The variation curve of virioplankton abundance in dry and rainy season |
|
|

|
| 图 4 旱季浮游病毒和浮游细菌丰度变化情况 Figure 4 The variation curve of virioplankton and planktonic bacteria abundance in dry season |
|
|
|
| 图 5 雨季浮游病毒和浮游细菌丰度变化情况 Figure 5 The variation curve of virioplankton and planktonic bacteria abundance in rainy season |
|
|
利用SPSS 17.0软件对水样样品pH、温度及元素含量作相关性分析,结果如表 6和表 7所示,旱季各元素之间N与Mg的相关性为正相关0.992;Mg与Cu的相关性达到正相关0.993;Ca与Cu的相关性是正相关0.925;Na、K与其他元素的相关性不是很高;pH与Ca具有较高的负相关性,而与Na有较高的正相关性;温度与其他元素的相关性不高。而针对于雨季而言,N与Na、K、pH及温度具有相关性;Mg与pH、温度负相关,与Na正相关;Ca与pH正相关;Na与K正相关,与pH、温度负相关;K与pH、温度负相关;pH与温度正相关。上述各水样元素及pH、温度的正负相关性可以为后续分析水样中各浮游病毒丰度的影响因子提供一定参考。
| 元素 Element |
氮 N |
镁 Mg |
钙 Ca |
铜 Cu |
钠 Na |
钾 K |
酸碱度 pH |
温度 Temperature |
| N | 1.000 | |||||||
| Mg | 0.992 | 1.000 | ||||||
| Ca | 0.868 | 0.902 | 1.000 | |||||
| Cu | 0.989 | 0.993 | 0.925 | 1.000 | ||||
| Na | -0.176 | -0.279 | -0.371 | -0.233 | 1.000 | |||
| K | -0.066 | -0.086 | -0.234 | -0.118 | -0.036 | 1.000 | ||
| pH | -0.398 | 0.443 | -0.638 | -0.454 | 0.621 | -0.276 | 1.000 | |
| Temperature | -0.383 | -0.401 | -0.445 | -0.400 | -0.207 | 0.413 | -0.160 | 1.000 |
| 元素 Element |
氮 N |
镁 Mg |
钙 Ca |
钠 Na |
钾 K |
酸碱度 pH |
温度 Temperature |
| N | 1.000 | ||||||
| Mg | -0.288 | 1.000 | |||||
| Ca | 0.171 | -0.346 | 1.000 | ||||
| Na | -0.667 | 0.515 | -0.119 | 1.000 | |||
| K | -0.589 | 0.343 | -0.185 | 0.852 | 1.000 | ||
| pH | 0.565 | -0.863 | 0.541 | -0.758 | -0.707 | 1.000 | |
| Temperature | 0.799 | -0.655 | 0.079 | -0.915 | -0.694 | 0.793 | 1.000 |
分别以旱、雨两季浮游病毒丰度为因变量,以其他各元素为自变量的前提下可以得出:旱季Chl-a浓度与浮游病毒丰度有显著性差异性(P=0.036 7 < 0.05,r2=0.808 4),即旱季水样的浮游病毒丰度受到细菌丰度及Chl-a浓度的影响较大;雨季pH值和温度与浮游病毒丰度有显著差异性(P=0.008 394 < 0.01,r2=0.908 4趋于1),由此看出雨季水样的浮游病毒丰度受到水体的pH值和温度的影响较大。
2.7 水样样品浮游病毒丰度与元素相关性分析用SPSS 17.0软件对不同季节浮游病毒丰度与元素的相关性进行分析得出:旱季浮游病毒丰度与N、Ca、Mg相关但不显著(r分别为0.490、0.586和0.442,P均 > 0.05);旱季浮游病毒丰度与Na无统计学意义(r=0.251,P > 0.05);旱季浮游病毒丰度与K呈负相关,但不显著(r=-0.447,P > 0.05)。雨季浮游病毒丰度与Ca无统计学意义(r=0.034,P > 0.05);雨季浮游病毒丰度与Mg、K分别呈正相关但不显著(r分别为0.625,0.573,P均 > 0.05);雨季浮游病毒丰度与N呈负相关但不显著(r=-0.522,P > 0.05);雨季浮游病毒丰度与Na呈显著正相关(r=0.906,P < 0.05)。
3 讨论与结论本研究采用FC技术对纳帕海高原湿地不同季节的浮游病毒和浮游细菌丰度进行了测量,并用SPSS 17.0软件和R语言1.7对影响浮游病毒丰度的浮游细菌丰度、Chl-a浓度等其他环境因子做了相关性分析。
研究结果表明,纳帕海湿地浮游病毒和浮游细菌的活动都比较活跃,但是在雨季会有明显的增强,而这一结果与裴达的研究结果(东湖浮游病毒的丰度在夏季达到峰值,冬季最小;浮游细菌的丰度春夏较高,冬季最小)相一致[21]。雨季水样的浮游病毒丰度最高可达2.91×108个/mL,远高于浮游细菌的丰度106个/mL;旱季水样的浮游病毒丰度最高可达8.46×106个/mL,浮游细菌丰度最高可达4.63×105个/mL。雨季浮游病毒和浮游细菌高于旱季的原因可能是浮游病毒主要包括噬菌体和藻类病毒两大类[22],他们的宿主即异氧细菌、蓝藻和浮游植物的分布要受到pH值、温度、营养和光照等因素的共同影响。夏季光照强、水温高,蓝藻、浮游植物等的生长比较旺盛,导致浮游病毒的裂解量也比较高;冬季光照弱、水温低,浮游植物等的代谢比较弱,导致病毒的裂解量减少。
在浮游病毒的丰度上,纳帕海湿地旱季和雨季的浮游病毒的丰度分别为3.15×107个/mL和1.05×108个/mL,与国内外报道[11, 15, 23]相似。Hara等[23] (1991)首次利用荧光显微计数法检测了日本大阪湾和Otsuchi Bay两个湾域中游离病毒的丰度,病毒直接检测量为1.2×106-3.5×107个/mL。卢龙飞等[11]采用流式细胞仪从水平分布和垂直分布上测得东海、黄海(119.5°-129°E,25°-39°N)浮游病毒的丰度为3.38×105-2.26×107个/mL (平均6.24× 106个/mL)和5.83×103-1.23×106个/mL (平均1.22×105个/mL)。刘晶晶等[15]采用荧光显微镜计数法测得2006年夏季和2007年冬季长江口浮游病毒丰度分别为2.22×106-9.97×107个/mL和1.99×106-2.66×107个/mL。从浮游细菌的丰度来看,纳帕海湿地的旱季和雨季的浮游细菌丰度分别为3.52×105个/mL和2.02×106个/mL,与张喆等[24]的研究结果[南海中北部海域秋季浮游细菌的丰度(39.62±35.35)×104个/mL]相似,但是低于姜发军等[25]的研究结果(大鹏湾全年浮游细菌丰度1.40×108- 24.43×108个/mL)。
叶绿素是浮游植物进行光合作用的主要色素。叶绿素主要包括叶绿素a、b和c。Chl-a广泛存在于藻类和浮游植物中,是衡量其生物量的一个重要指标。而Chl-a含量的变化一定程度上可以表示藻类与浮游植物生物量的动态变化。用R语言分析得出旱季水样浮游病毒丰度与浮游细菌丰度、Chl-a浓度有显著差异性(P=0.036 7 < 0.05),与浮游细菌成正相关性,而与Chl-a呈负相关性,说明在旱季噬菌体而非噬藻体或浮游植物病毒是纳帕海湿地中浮游病毒的优势种群;雨季水样浮游病毒丰度与pH值、温度具有显著差异性(P=0.008 394 < 0.01);表明在样品中Chl-a、浮游细菌、pH值和温度对浮游病毒丰度有较大影响,这可能与纳帕海湿地独特的高原气候有关。据文献报道,大多数情况下浮游病毒丰度与Chl-a含量并无显著相关性,但是王海丽等[12]的研究结果表明Chl-a是象山港海域表层海水中的浮游病毒丰度主要影响因素之一。
在水平分布上,原水水样样品中的浮游病毒要高于湿地水和淤泥水的,尤其是原水-7 (YW-7)的浮游病毒丰度达到了108个/mL,这可能是湿地水和淤泥水附近在雨季和旱季容易受到牲畜和人类活动的影响,影响了水体的pH和水质。具体原因还有待进一步地研究。
本研究初步探讨了纳帕海湿地不同季节、不同样品浮游病毒和浮游细菌的丰度,并对浮游病毒与环境因子的相关性做了分析,对纳帕海湿地微生物资源的开发和保护具有重要的指导意义。
| [1] |
Fuhrman JA. Marine viruses and their biogeochemical and ecological effects[J]. Nature, 1999, 399(6736): 541-548. DOI:10.1038/21119 |
| [2] |
Bratbak G, Heldal M. Viruses rule the waves-the smallest and most abundant members of marine ecosystems[J]. Microbiology Today, 2000, 27: 171-173. |
| [3] |
Wang F, Zheng TL, Hong HS. The important role of marine viruses in microbial loop[J]. Marine Sciences, 1998(4): 41-43. 王斐, 郑天凌, 洪华生. 海洋病毒在微生物食物环中的重要作用[J]. 海洋科学, 1998(4): 41-43. |
| [4] |
Zhang QY. Virioplankton[J]. Acta Hydrobiologica Sinica, 2002, 26(6): 691-696. 张奇亚. 浮游病毒[J]. 水生生物学报, 2002, 26(6): 691-696. |
| [5] |
Bettarel Y, Sime-Ngando T, Amblard C, et al. Viral activity in two contrasting lake ecosystems[J]. Applied and Environmental Microbiology, 2004, 70(5): 2941-2951. DOI:10.1128/AEM.70.5.2941-2951.2004 |
| [6] |
Bergh Ø, Børsheim KY, Bratbak G, et al. High abundance of viruses found in aquatic environments[J]. Nature, 1989, 340(6233): 467-468. DOI:10.1038/340467a0 |
| [7] |
Proctor LM, Fuhrman JA. Viral mortality of marine bacteria and cyanobacteria[J]. Nature, 1990, 343(6253): 60-62. DOI:10.1038/343060a0 |
| [8] |
Fuhrman JA, Noble RT. Viruses and protists cause similar bacterial mortality in coastal seawater[J]. Limnology & Oceanography, 1995, 40(7): 1236-1242. |
| [9] |
Wang H, Bai SJ, Cai WW, et al. Modulating marine ecosystem by marine viruses—a review[J]. Acta Microbiologica Sinica, 2009, 49(5): 551-559. 王慧, 柏仕杰, 蔡雯蔚, 等. 海洋病毒——海洋生态系统结构与功能的重要调控者[J]. 微生物学报, 2009, 49(5): 551-559. |
| [10] |
Breitbart M, Rohwer F. Here a virus, there a virus, everywhere the same virus?[J]. Trends in Microbiology, 2005, 13(6): 278-284. DOI:10.1016/j.tim.2005.04.003 |
| [11] |
Lu LF, Wang M, Liang YT, et al. Distribution of virioplankton, heterotrophic bacteria in the yellow sea and east china sea[J]. Oceanologia et Limnologia Sinica, 2013, 44(5): 1339-1346. 卢龙飞, 汪岷, 梁彦韬, 等. 东海、黄海浮游病毒及异养细菌的分布研究[J]. 海洋与湖沼, 2013, 44(5): 1339-1346. |
| [12] |
Wang HL, Yang JF, Tu XX, et al. Spatiotemporal distribution of marine viruses with related to environmental factors in the Xiangshan Bay[J]. China Environmental Science, 2011, 31(5): 834-844. 王海丽, 杨季芳, 屠霄霞, 等. 象山港海洋病毒时空分布特征及其环境影响因素[J]. 中国环境科学, 2011, 31(5): 834-844. |
| [13] |
Zhang QY. Advances in studies on biodiversity of cyanophages[J]. Microbiology China, 2014, 41(3): 545-559. 张奇亚. 噬藻体生物多样性的研究动态[J]. 微生物学通报, 2014, 41(3): 545-559. |
| [14] |
Bai XG, Wang M, Ma JJ, et al. Virioplankton abundance in winter and spring in Changjiang River estuary by fluorescence microscope counting[J]. Oceanologia et Limnologia Sinica, 2007, 38(4): 367-372. 白晓歌, 汪岷, 马晶晶, 等. 冬季和春季长江口及其近海水域浮游病毒丰度的分析[J]. 海洋与湖沼, 2007, 38(4): 367-372. |
| [15] |
Liu JJ, Zeng JN, Du P, et al. Abundance distribution of virioplankton in Yangtze River estuary and its adjacent East China Sea in summer and winter[J]. Chinese Journal of Applied Ecology, 2011, 22(3): 793-799. 刘晶晶, 曾江宁, 杜萍, 等. 长江口及邻近海域夏、冬季浮游病毒丰度分布[J]. 应用生态学报, 2011, 22(3): 793-799. |
| [16] |
Hu JM, Li J, Yuan H, et al. Easonal landscape pattern change and its driving forces of the Napahai Wetland[J]. Geographical Research, 2010, 29(5): 899-908. 胡金明, 李杰, 袁寒, 等. 纳帕海湿地季节性景观格局动态变化及其驱动[J]. 地理研究, 2010, 29(5): 899-908. |
| [17] |
Guo XH, Xiao DR, Tian K, et al. Biomass production and litter decomposition of lakeshore plants in Napahai wetland, Northwestern Yunnan Plateau, China[J]. Acta Ecologica Sinica, 2013, 33(5): 1425-1432. 郭绪虎, 肖德荣, 田昆, 等. 滇西北高原纳帕海湿地湖滨带优势植物生物量及其凋落物分解[J]. 生态学报, 2013, 33(5): 1425-1432. |
| [18] |
Guo XL, Tian K, Ge XX, et al. Distribution of organic carbon density and carbon storage in plateau wetland soils in Napahai[J]. Journal of Soil and Water Conservation, 2012, 26(4): 159-162. 郭雪莲, 田昆, 葛潇霄, 等. 纳帕海高原湿地土壤有机碳密度及碳储量特征[J]. 水土保持学报, 2012, 26(4): 159-162. |
| [19] |
Liao J, Shen CM, Yu XS. Climate changes and its influence on Napahai wetland[J]. Journal of West China Forestry Science, 2016, 45(4): 136-140, 146. 廖君, 沈才明, 余晓珊. 气候变化及其对纳帕海湿地的影响[J]. 西部林业科学, 2016, 45(4): 136-140, 146. |
| [20] |
Ji XL. Bacteriophage diversity, abundance and its role in the production of disolved organic carbon in Napahai Plateau Wetland[J]. Kunming: Doctoral Dissertation of Kunming University of Science and Technology, 2015 (in Chinese) 季秀玲. 高原湿地纳帕海噬菌体的多样性、丰度及其与DOC关系初步研究[D]. 昆明: 昆明理工大学博士学位论文, 2015 http://cdmd.cnki.com.cn/Article/CDMD-10674-1015638947.htm |
| [21] |
Pei D. Temporal and spatial distribution of virioplankton in Donghu Lake and preliminary study on its genetic diversity[D]. Wuhan: Master's Thesis of Huazhong Normal University, 2007 (in Chinese) 裴达. 东湖浮游病毒的时空分布调查及遗传多样性的初步研究[D]. 武汉: 华中师范大学硕士学位论文, 2007 http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y1122287 |
| [22] |
Contreras-Coll N, Lucena F, Mooijman K, et al. Occurrence and levels of indicator bacteriophages in bathing waters throughout Europe[J]. Water Research, 2002, 36(20): 4963-4974. DOI:10.1016/S0043-1354(02)00229-4 |
| [23] |
Hara S, Terauchi K, Koike I. Abundance of viruses in marine waters: assessment by epifluorescence and transmission electron microscopy[J]. Applied and Environmental Microbiology, 1991, 57(9): 2731-2734. |
| [24] |
Zhang Z, Gong XY, Hu Y, et al. Abundance of bacterioplankton and virioplankton in the central and northern South China Sea in autumn[J]. South China Fisheries Science, 2016, 12(4): 9-16. 张喆, 巩秀玉, 胡莹, 等. 南海中北部海域秋季浮游细菌和病毒丰度及其影响因子[J]. 南方水产科学, 2016, 12(4): 9-16. |
| [25] |
Jiang FJ, Hu ZL, Hu CQ. Correlation between spatial-temporal distribution of bacterioplankton and environmental factors in the Dapeng Bay[J]. Journal of Tropical Oceanography, 2011, 30(1): 96-100. 姜发军, 胡章立, 胡超群. 大鹏湾浮游细菌时空分布与环境因子的关系[J]. 热带海洋学报, 2011, 30(1): 96-100. DOI:10.11978/j.issn.1009-5470.2011.01.096 |
 2018, Vol. 45
2018, Vol. 45




