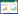扩展功能
文章信息
- 韩晓伟, 张小波, 严玉平, 郑玉光, 冯红, 赵同安
- HAN Xiao-Wei, ZHANG Xiao-Bo, YAN Yu-Ping, ZHENG Yu-Guang, FENG Hong, ZHAO Tong-An
- 16S rRNA基因高通量测序法分析黄河太岁细菌的多样性
- Bacterial diversity of the Yellow River Taisui by 16S rRNA gene sequencing
- 微生物学通报, 2018, 45(4): 866-874
- Microbiology China, 2018, 45(4): 866-874
- DOI: 10.13344/j.microbiol.china.170406
-
文章历史
- 收稿日期: 2017-06-06
- 接受日期: 2017-08-10
- 网络首发日期(www.cnki.net): 2017-08-28
2. 中国中医科学院中药资源中心 北京 100700;
3. 安国数字本草检验中心有限公司 河北 安国 071200
2. China Academy of Chinese Medical Sciences (CACMS), Beijing 100700, China;
3. Anguo Digital Materia Medica Testing Center Co., Ltd., Anguo, Hebei 071200, China
太岁又称肉灵芝,《神农本草经》记载其“无毒、补中、益精气、久服轻身不老”,《本草纲目》将其奉为“本经上品”,认为“久食,轻身不老,延年神仙”。现代的一些研究发现太岁富含多糖、几丁质和硒等数十种营养成分,具有调节体液酸碱平衡、增强机体免疫力、防癌、抗衰老等作用,是一味十分具有开发前途的药食同源中药[1]。我国对太岁的记载和研究由来已久,现代研究从关注其药效逐渐开始探究太岁的生命本质,现代研究表明太岁是一种大型的黏菌、细菌和真菌的复合体[2]。随着生命科学技术的不断发展,对太岁进行系统的生物学研究已成为大势所趋。
戴璐[3]利用玉米琼脂和燕麦琼脂的有饲培养技术初步从太岁中分离纯化出了多种黏菌。化学分析的方法研究发现,太岁是一种聚乙烯醇并含有一些黏细菌、霉菌和芽孢杆菌的“不明物体”[4],而利用简单的分子生物学方法分析发现,其主要由粘质的红酵母菌组成[5]。不同地区、不同来源的太岁,利用不同的分析方法得到不同的结果,因此对于太岁的鉴别仍然是模糊的。
在微生物种类鉴定的技术方面,传统的鉴定方法要对所研究的细菌进行富集、培养,然后根据其形态、生理、生化等实验来确定菌的种类。由于培养条件的限制,许多菌类无法培养,从而无法完全反映样本中的微生物群落情况[6]。随着分子生物学技术的发展,基于DNA测序的高通量技术也越来越广泛地运用到微生物多样性分析中。微生物细胞内特定的遗传物质如原核微生物16S rRNA、真核微生物18S rRNA和rDNA-ITS[7-9],这些区域保守序列之间存在由于进化造成的物种之间序列差异的可变区域,是微生物多样性分析的首选。原核微生物16S rRNA基因序列共有9个可变区(V1–V2区、V2区、V3区、V4区、V5–V6区、V6区、V6–V7区、V8区和V9区)和10个保守区,9个可变区的基因序列主要用来鉴定微生物的物种[10]。Claesson等[11]对16S rRNA基因的9个可变区进行了分析。在能够比对到属水平上的比例及准确率方面V1和V9区的效果最差,V7和V8的效果较差,V3、V4和V5效果较好,而分类效率最好的是V3和V4区[12],因此微生物16S rRNA基因V3–V4区的检测已被广泛地运用到医学[13]、食品[14]、动植物、土壤微生物类群[15]、空气微生物多样性[16]等研究中,并取得了一定的成果。
基于以上原因,本实验利用Illumina平台检测黄河太岁的16S rRNA基因的V4区,分析太岁中所含的细菌种类,从而为研究太岁的构成提供更科学的证据。
1 材料与方法 1.1 样品采集样品出自内蒙古薛家湾电厂(电厂施工期间挖出),由河北省石家庄市太岁收藏家才彦良先生购得后友情提供。
1.2 主要试剂和仪器十六烷基三甲基溴化铵(CTAB),生工生物工程(上海)股份有限公司;Tris平衡酚,索莱宝生物科技有限公司;核酸染料10 000×Gene Green,天根生化科技(北京)有限公司;AL2000 DNA Marker,北京艾德莱生物科技有限公司;Phusion® High-Fidelity PCR Master Mix with GC Buffer,美国纽英伦生物技术公司;QIA Quick Gel Extraction Kit,德国凯杰生物公司;TruSeq® DNA PCR-Free Library Sample Preparation Kit,上海睿铂赛生物科技有限公司;Qubit™ dsDNA HS Assay Kit,赛默飞世尔科技公司。
离心机和荧光计,赛默飞世尔科技公司;PCR仪,美国伯乐公司;琼脂糖凝胶电泳仪,北京六一生物科技有限公司;全自动凝胶成像分析系统,上海培清科技有限公司;高通量测序仪,上海睿铂赛生物科技有限公司。
1.3 太岁样品的处理将样品在超净台用无菌生理盐水冲洗干净,75% (体积比)乙醇浸泡2 min后无菌水清洗3次,再用0.1% (质量体积比)升汞浸泡1 min,最后用无菌水冲洗3次,用无菌的解剖刀切去表面,将剩下的样品切成小块。吸取第3次漂洗消毒材料的无菌水涂平板,培养后若无微生物长出,证明表面消毒彻底。
1.4 DNA的提取与测序太岁样品利用CTAB法提取基因组DNA,提取的总DNA经琼脂糖凝胶电泳和16S rRNA基因V4区PCR扩增,上游引物515F:5′-GTGCCAGCMG CCGCGGTAA-3′;下游引物806R:5′-GGACTACHV GGGTWTCTAAT-3′。PCR反应体系(30 μL):Phusion Master Mix (2×) 15 μL,上、下游引物(2 μmol/L)各1.5 μL,gDNA (1 ng/μL) 10 μL,ddH2O 2 μL。PCR反应条件:98 ℃ 1 min;98 ℃ 10 s,50 ℃ 30 s,72 ℃ 30 s,30个循环;72 ℃ 5 min。检测合格后进行文库构建及利用带有Barcode的引物扩增16S rRNA基因V4区。构建好的文库经过Qubit和Q-PCR定量,文库检测合格后使用Illumina MiSeq 2×250进行上机测序。
1.5 测序结果分析使用FLASH (Version 1.2.7,http://ccb.jhu.edu/software/FLASH/)[17]对原始数据进行处理。利用UPARSE软件(Version 7.0.1001,http://drive5.com/uparse/)[18]对所有样品的全部Effective Tags进行聚类,默认以97%的一致性(Identity)将序列聚类成为OTU (Operational taxonomic unit)。对OTU代表序列进行物种注释,用QIIME软件(Version 1.7.0)中的BLAST方法(http://qiime.org/scripts/assign_taxonomy.html)[19]与Unit数据库(https://unite.ut.ee/)[20]进行物种注释分析,并分别在各个分类水平:界(Kingdom)、门(Phylum)、纲(Class)、目(Order)、科(Family)、属(Genus)、种(Species)统计各样本的群落组成。使用MUSCLE[21] (Version 3.8.31,http://drive5.com/muscle/)软件进行快速多序列比对,得到所有OTU代表序列的系统发生关系。
2 结果与分析 2.1 测序数据统计提取黄河太岁DNA后,对16S rRNA基因V4区进行高通量测序,结果样品共得到有效序列28 118条,序列长度分布在44−388 bp之间;通过过滤去除含有错误引物、序列小于200 bp、模糊碱基大于0的序列的优化过程,共得到序列27 200条,序列平均长度255 bp。经过数据库比对分析,共有26 141条序列与数据库中的序列有相似性,有效序列为92.97%,可用于后续的分析。
对所得到的有效序列进行稀释曲线和等级聚类曲线的分析,稀释曲线可直接反映测序数据量的合理性,当曲线趋向平坦时说明测序数据量渐进合理,更多的数据量只会产生少量新的物种。等级聚类曲线可直观地反映样品中物种的丰富度和均匀度。在水平方向上,物种的丰富度越高曲线在横轴上的跨度越大;在垂直方向上,曲线越平缓表明物种分布越均匀。16S rRNA基因V4区的数据量在30 000左右,从稀释曲线和等级聚类曲线(图 1)可以看出,曲线已较平缓,数据量已达饱和状态,可满足分析需求。

|
| 图 1 16S rRNA基因V4区的稀释曲线(A)和等级聚类曲线(B) Figure 1 The rarefaction curve (A) and rank abundance curve (B) |
|
|
黄河太岁注释到各分类水平界、门、纲、目、科、属上的序列数目分别是590、205、1 227、3 689、4 539、10 515,由此可知黄河太岁的16S rRNA基因V4区的数据以注释到属水平的为最多。根据物种注释结果,选取样品在各分类水平(门、纲、目、科、属)上最大丰度排名前十的物种(图 2),在门水平上Proteobacteria和Firmicutes分别占到了45.3%和40.3%,在纲的水平上居于前两位的是Clostridia和Gammaproteobacteria,二者各占34%,在目水平上Clostridiales和Oceanospirillales二者合计占到了57%,在科的水平上Halomonadaceae和Ruminococcaceae占到了40%,无法确定的科占35%左右,在属的水平上居于前十的菌主要是Bacteroides、Coprococcus、Escherichia、Ruminococcus、Lactobacillus、[Ruminococcus]、Oscillospira、Faecalibacterium、Shewanella和Halomonas。其中Halomonas是优势菌群,大约占24%,而无法确定的属占50%。
|
| 图 2 门、纲、目、科、属水平上的物种相对丰度 Figure 2 Relative abundance of species at the level of phylum, class, order, family and genus |
|
|
从样品的物种分类结果中筛选特别关注的物种(默认选择最大相对丰度前20的种)进行物种分类树统计[22],样品的物种分类树见图 3。从图 3可以看出,太岁所含细菌种类主要分布在Bacteroidetes、Proteobacteria和Firmicutes 3个门,其中Proteobacteria约占65.55%,占绝对优势;从纲的分类水平来看以Gammaproteobacteria为主,占65.55%;在目的水平上以Clostridiales和Oceanospirillales为优势目;在科的水平上以Halomonadaceae为优势科,占比达到50.39%;在属水平上,以盐单胞菌属Halomonas的比例最大,达50.39%;在种的水平上,以H. algae、prausnitzii和colibacillus占比最大,分别达到12.87%、7.38%和2.3%,其中H. algae和colibacillus属于同一个纲(Gammaproteobacteria),prausnitzii属于Clostridia纲。注释到种水平的序列较少,可以确定种名的更少,大部分都无法定种。

|
| 图 3 黄河太岁中特定物种分类树 Figure 3 Specific species classification tree in the Yellow River Taisui |
|
|
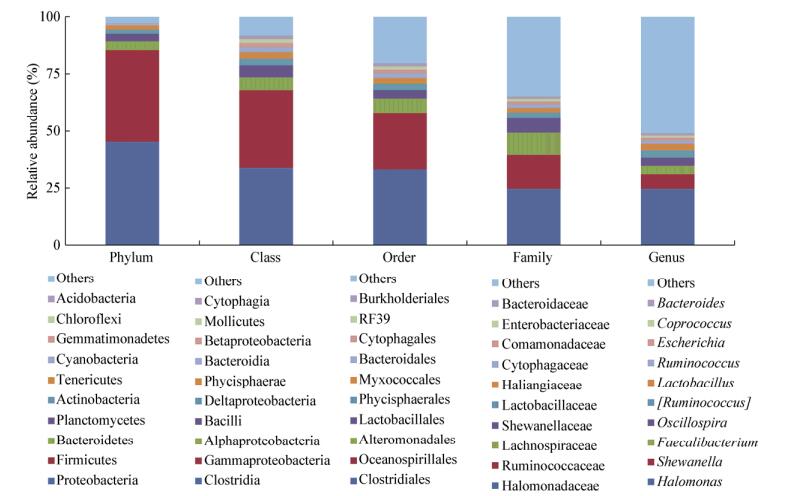
为了进一步研究太岁中所含细菌的系统进化关系,通过多序列比对得到所有OTU代表序列的系统进化关系。选取最大相对丰度排名前十的属所对应OTU的系统进化关系数据,并结合每个OTU的相对丰度及其代表序列的物种注释置信度信息进行整合展示,由此可见这些属中OTU之间的系统进化关系,见图 4。图 4由3层构成,由里向外依次为第一层:OTU代表序列构建的系统发育树,分支的颜色代表其对应的属名;第二层:OTU的相对丰度分布,柱子的高度表示OTU相对丰度的大小;第三层:OTU注释的可信度,柱子的高度代表OTU注释的可信度。从图 4中可以看出Halomonas、Shewanella和Escherichia的相对丰度较高,在系统进化的关系也较为接近,其次为Oscillospira、[Ruminococcus]和Faecalibacterium在系统进化上较为接近,聚为一支。第二层的柱子高度基本一致,说明这些物种的丰度差别不大,在进化上基本趋于一致。
|
| 图 4 黄河太岁的OTU系统进化关系 Figure 4 OTU phylogenetic relationship of the Yellow River Taisui |
|
|
长期以来太岁的分类定位有多种说法。中国科学院的茆晓岚认为太岁是非生命体,而吉林大学的微生物学家认为太岁是介于原生生物和真菌之间的黏细菌,西北大学生物系专家则认为太岁为特大型黏菌复合体[23]。这是由于太岁来源的不同以及检测技术的限制,无法系统地分析太岁中所含的微生物,从而形成了不同的结论。高通量测序技术可以解决由于不同样品、不同培养方式所产生的结果差异,一次性对几十万甚至上百万条DNA分子的序列进行测定,从而成为利用宏基因组学方法研究太岁的重要手段[24]。
依据高通量测序技术检测黄河太岁中细菌,发现细菌种类非常多,有很多细菌无法确定其种属,而已知细菌的功能又多种多样,既有对人体有益的种类,也有一些能够使人体致病的种类。在属的水平上居于前十的菌主要是Bacteroides、Coprococcus、Escherichia、Ruminococcus、Lactobacillus、[Ruminococcus]、Oscillospira、Faecalibacterium、Shewanella和Halomonas,其所占比例见表 1。Halomonas具有很强的适应能力,对温度、盐度和氧气的适应范围广,在污水处理与生物修复方面可能具有重要的应用价值[25]。Shewanella对于环境的生物修复具有一定的作用,但是有一部分希瓦氏菌也是人类和鱼类的致病原,主要通过接触海水或海水鱼类而致病[26]。Faecalibacterium和Oscillospira属于肠道菌群,具有保护肠黏膜等作用[27-28],但研究得并不透彻。Faecalibacterium和Ruminococcus多存在于牛羊的胃和肠道中,其代谢为典型的混合发酵[29]。Lactobacillus是一类能利用可发酵碳水化合物产生大量乳酸的细菌的通称,这类细菌在自然界分布极为广泛,具有丰富的物种多样性,它们不仅是研究分类、生化、遗传、分子生物学和基因工程的理想材料,在理论上具有重要的学术价值,而且在工业、农牧业、食品和医药等与人类生活密切相关的重要领域应用价值也极高[30-32]。此外,这类菌中有些细菌又是人畜的致病菌,因此受到人们的关注和重视。Bacteroides是人类肠道的有益菌群,对于维持人类肠道的菌群平衡有重要作用[33],它是一种优良的碳水化合物降解细菌,能够将许多植物类食品中的大分子碳水化合物降解为葡萄糖和其他易消化的小分子糖类,人体中没有可以合成降解碳水化合物的酶基因,而多形拟杆菌的基因能合成多种消化植物成分的酶,从而帮助人体高效地从橙子、苹果、土豆、小麦胚芽等食物中提取营养素[34]。
| 菌种 Name of bacteria |
属名 Name of genus |
所占比例 Percentage (%) |
| Halomonas | 盐单胞菌属 | 24.71 |
| Shewanella | 希瓦氏菌属 | 6.31 |
| Faecalibacterium | 普式粪杆菌 | 4.04 |
| Oscillospira | 颤螺菌属 | 3.50 |
| [Ruminococcus] | 瘤胃球菌属 | 3.16 |
| Lactobacillus | 乳酸菌 | 2.78 |
| Ruminococcus | 瘤胃球菌 | 1.39 |
| Escherichia | 埃希氏菌属 | 1.13 |
| Coprococcus | 粪球菌属 | 1.05 |
| Bacteroides | 拟杆菌属 | 0.96 |
| Others | 未知 | 50.95 |
表 1所列属的细菌种类繁多,功能各不相同,大多数是容易导致腐败和变质的种类,但实际上太岁不易腐败。太岁在含有如此众多细菌的情况下却不会发生腐败,可能是由于其含有可抑制腐败细菌的黏菌所致,黏菌可通过分泌抑菌酶吞噬细菌[35]而使太岁保持高度不腐的状态。
综上所述,太岁不是一个单一的物种,细菌只是构成太岁的一部分,太岁应该是一个各种细菌协调合作构成的一个生物体。迄今为止,太岁在生物界还没有一个科学的定位,因此,系统地研究太岁的生物学特征对于研究微生物的进化和分类具有重要的意义。
| [1] |
Zhu CY, Bai TT, Jiang QS, et al. Biological components of "Tai Sui"[J]. Journal of Microbiology, 2011, 31(1): 1-5. 朱春玉, 白婷婷, 姜秋实, 等. "太岁"生物学组分的研究[J]. 微生物学杂志, 2011, 31(1): 1-5. |
| [2] |
Li HY, Huang JH, Feng JW, et al. The research progress of Tai sui[J]. Farm Products Processing, 2015(6): 73-75. 李海月, 黄继红, 冯军伟, 等. 太岁的研究进展[J]. 农产品加工, 2015(6): 73-75. |
| [3] |
Dai L. Assessment of myxomycete and fungal diversity of the "myxomycete complex"[D]. Xi'an: Master's Thesis of Northwest University, 2007 (in Chinese) 戴璐. "大型黏菌复合体"黏菌和真菌多样性的初步研究[D]. 西安: 西北大学硕士学位论文, 2007 |
| [4] |
Zheng KY, Dong ZL. Preliminary study result of the unkown objects of "Tai Sui"[J]. Journal of Northwest University (Natural Science Edition), 2010, 40(6): 1012-1016. 郑科研, 董兆麟. 不明物体"太岁"的初步研究[J]. 西北大学学报:自然科学版, 2010, 40(6): 1012-1016. |
| [5] |
Lin J, Xiong XH, Ge X, et al. Isolation and identification of microbial strains in two different Taisui samples[J]. Letters In Biotechnology, 2013, 24(6): 825-827. 林涧, 熊向华, 葛欣, 等. 2种太岁样品中微生物的分离和鉴定[J]. 生物技术通讯, 2013, 24(6): 825-827. |
| [6] |
Cao R, Zhang J, Meng HH, et al. Microbial flora analysis of oyster: a comparison between traditional plate incubation method and High Throughput Sequencing technology[J]. Food Science, 2016, 37(24): 137-141. 曹荣, 张井, 孟辉辉, 等. 高通量测序与传统纯培养方法在牡蛎微生物群落分析中的应用对比[J]. 食品科学, 2016, 37(24): 137-141. DOI:10.7506/spkx1002-6630-201624021 |
| [7] |
Cheung MK, Au CH, Chu KH, et al. Composition and genetic diversity of picoeukaryotes in subtropical coastal waters as revealed by 454 pyrosequencing[J]. The ISME Journal, 2010, 4(8): 1053-1059. DOI:10.1038/ismej.2010.26 |
| [8] |
Oros-Sichler M, Smalla K. Semi-Nested PCR approach to amplify large 18S rRNA gene fragments for PCR-DGGE analysis of soil fungal communities[A]//Gupta VK, Tuohy MG, Ayyachamy M, eds. Laboratory Protocols in Fungal Biology[M]. New York: Springer, 2013
|
| [9] |
Stoeck T, Behnke A, Christen K, et al. Massively parallel tag sequencing reveals the complexity of anaerobic marine protistan communities[J]. BMC Biology, 2009, 7: 72. DOI:10.1186/1741-7007-7-72 |
| [10] |
Yuan S. Analysis of the bacterial diversity in two different Distillers Grains by High Throughput Sequencing of 16S rRNA V4[D]. Guiyang: Master's Thesis of Guizhou Normal University, 2014 (in Chinese) 袁帅. 用16S rRNA V4区高通量测序分析两种酒糟细菌多样性[D]. 贵阳: 贵州师范大学硕士学位论文, 2014 |
| [11] |
Claesson MJ, Wang Q, O'Sullivan O, et al. Comparison of two next-generation sequencing technologies for resolving highly complex microbiota composition using tandem variable 16S rRNA gene regions[J]. Nucleic Acids Research, 2010, 38(22). |
| [12] |
Xia ZK. The comparative analysis and discussion of 16S rRNA sequencing data based on 454 and ion torrent platform[D]. Beijing: Master's Thesis of University of Electronic Science and Technology of China, 2014 (in Chinese) 夏忠奎. 基于454与Ion Torrent平台的16S rRNA测序数据的比较分析与研究[D]. 北京: 电子科技大学硕士学位论文, 2014 |
| [13] |
Zheng H, Xu LX, Wang ZC, et al. Subgingival microbiome in patients with healthy and ailing dental implants[J]. Science Reports, 2015, 5: 10948. DOI:10.1038/srep10948 |
| [14] |
Qiao XM, Zhao JL, Du XW, et al. Analysis of fungal communities of Qingxiang Daqu by Barcoded Pyrosequencing[J]. Liquor-Making Science & Technology, 2015(4): 28-31. 乔晓梅, 赵景龙, 杜小威, 等. 高通量测序法对清香大曲真菌群落结构的分析[J]. 酿酒科技, 2015(4): 28-31. |
| [15] |
Zhang CX. The research of microorganism composition responses to environment conditions with the Next Generation High Throughput DNA Sequencing Technology[D]. Nanjing: Master's Thesis of Nanjing Agricultural University, 2012 (in Chinese) 张彩霞. 新一代高通量测序技术研究土壤微生物群落结构对环境条件的响应[D]. 南京: 南京农业大学硕士学位论文, 2012 |
| [16] |
Li HM, Bai L, Jiang DM, et al. Microbial diversity of piggery air detected by 16S rDNA high-throughput sequencing[J]. Chinese Journal of Animal Science, 2015, 51(3): 81-84. 李红梅, 白林, 姜冬梅, 等. 基于16S rDNA高通量测序方法检测猪舍空气微生物多样性[J]. 中国畜牧杂志, 2015, 51(3): 81-84. |
| [17] |
Lundberg DS, Yourstone S, Mieczkowski P, et al. Practical innovations for high-throughput amplicon sequencing[J]. Nature Methods, 2013, 10(10): 999-1002. DOI:10.1038/nmeth.2634 |
| [18] |
Rivas MN, Burton OT, Wise P, et al. A microbiota signature associated with experimental food allergy promotes allergic sensitization and anaphylaxis[J]. The Journal of Allergy and Clinical Immunology, 2013, 131(1): 201-212. DOI:10.1016/j.jaci.2012.10.026 |
| [19] |
Segata N, Lzard J, Waldron L, et al. Metagenomic biomarker discovery and explanation[J]. Genome Biology, 2011, 12: R60. DOI:10.1186/gb-2011-12-6-r60 |
| [20] |
Magoč T, Salzberg SL. FLASH: fast length adjustment of short reads to improve genome assemblies[J]. Bioinformatics, 2001, 27(21): 2957-2963. |
| [21] |
Bokulich NA, Subramanian S, Faith JJ, et al. Quality-filtering vastly improves diversity estimates from Illumina amplicon sequencing[J]. Nature Methods, 2013, 10(1): 57-59. DOI:10.1038/nmeth.2276 |
| [22] |
Li B, Zhang XX, Guo F, et al. Characterization of tetracycline resistant bacterial community in saline activated sludge using batch stress incubation with high-throughput sequencing analysis[J]. Water Research, 2013, 47(13): 4207-4216. DOI:10.1016/j.watres.2013.04.021 |
| [23] |
Zhou QC. What is the "Taisui" actually[J]. Science and Technology Daily, 2005(5): 1-3. 周青春. 这个"太岁"究竟为何物[J]. 科技日报, 2005(5): 1-3. |
| [24] |
Nie ZQ, Han Y, Zheng Y, et al. Metagenomic analysis of microbial diversity in the traditional vinegar fermentation process[J]. Food Science, 2013, 34(15): 198-203. 聂志强, 韩玥, 郑宇, 等. 宏基因组学技术分析传统食醋发酵过程微生物多样性[J]. 食品科学, 2013, 34(15): 198-203. DOI:10.7506/spkx1002-6630-201315041 |
| [25] |
Qian YX. Study on the removal mechanism of similar Persistent Organic Pollutants from dyeing wastewater bv Pseudomonas sp. Bacteria[J]. Hangzhou: Doctoral Dissertation of Zhejiang University, 2015. |
| [26] |
Shang BD, Yang X, Li ZY, et al. Research progress of Shewanella[J]. Fujian Agricultural, 2015(7): 152-154. 商宝娣, 杨星, 李正友, 等. 希瓦氏菌的研究进展[J]. 福建农业, 2015(7): 152-154. |
| [27] |
Wuri LG, Sun ZH, Mehe BLG. The relation between Faecalibacterium prausnitzii and human diseases: research progress[J]. Chinese Journal of Microecology, 2017, 29(5): 604-609, 614. 乌日拉嘎, 孙志宏, 孟和毕力格. Faecalibacterium prausnitzii与人类疾病关系的研究进展[J]. 中国微生态学杂志, 2017, 29(5): 604-609, 614. |
| [28] |
Liu JP, Zou WL, Chen SJ, et al. Effects of different diets on intestinal microbiota and nonalcoholic fatty liver disease development[J]. World Journal of Gastroenterology, 2016, 22(32): 7353-7364. DOI:10.3748/wjg.v22.i32.7353 |
| [29] |
Gao YF, Ouyang KH, Zhai MR, et al. Analysis of rumen bacterial diversity in Jinjiang cattle using MiSeq sequencing technology[J]. Chinese Journal of Animal Nutrition, 2016, 28(1): 244-248. 高雨飞, 欧阳克蕙, 瞿明仁, 等. 利用MiSeq测序技术分析锦江牛瘤胃细菌多样性[J]. 动物营养学报, 2016, 28(1): 244-248. |
| [30] |
Zhang HP, Yu J. New progress on the genomics of Lactic Acid Bacteria[J]. Journal of Chinese Institute of Food Science and Technology, 2016, 16(2): 1-8. 张和平, 于洁. 乳酸菌基因组学研究新进展[J]. 中国食品学报, 2016, 16(2): 1-8. |
| [31] |
Cui MY, Zhang M, Xu ZW, et al. Research progress of Lactic Acid Bacteria resistance under extreme conditions[J]. China Dairy Industry, 2016, 44(5): 28-31. 崔美岩, 张淼, 许宗为, 等. 乳酸菌在极端条件下抗逆性的研究进展[J]. 中国乳品工业, 2016, 44(5): 28-31. |
| [32] |
Meng X, Jiang LS, Qian Y, et al. Research development on Hypoglycemic activity of Lactic Acid Bacteria[J]. Food Research and Development, 2016, 37(6): 193-196. 孟晓, 蒋丽施, 骞宇, 等. 用于降血糖的乳酸菌研究进展[J]. 食品研究与开发, 2016, 37(6): 193-196. |
| [33] |
Li YD, Ren HW, Wu YB, et al. Bacteroides and gut microbial ecology[J]. Microbiology China, 2008, 35(2): 281-285. 李亚丹, 任宏伟, 吴彦彬, 等. 拟杆菌与肠道微生态[J]. 微生物学通报, 2008, 35(2): 281-285. |
| [34] |
Wu YB, Li YD, Li XJ, et al. The study and application on bacteroides[J]. Biotechnology Bulletin, 2007(1): 66-69. 吴彦斌, 李亚丹, 李晓俊, 等. 拟杆菌的研究及应用[J]. 生物技术通报, 2007(1): 66-69. |
| [35] |
Gu S. Study on culture, biological characteristics and Phagocytosis to bacteria of Plasmodia in major species of myxomycetes[D]. Changchun: Master's Thesis of Jilin Agricultural University, 2011 (in Chinese) 谷硕. 黏菌主要种原质团的培养、生物学特性及其对细菌吞噬作用的研究[D]. 长春: 吉林农业大学硕士学位论文, 2011 |
 2018, Vol. 45
2018, Vol. 45