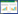扩展功能
文章信息
- 周婧, 黄丽云, 李钢, 徐静
- Zhou Jing, Huang Li-Yun, Li Gang, Xu Jing
- 一株红茄苳内生烟曲霉菌的分离鉴定及其发酵产物抗氧化活性
- Isolation, identification and antioxidant activity Aspergillus fumigatus HQD24 endophytic in Rhizophora mucronata
- 微生物学通报, 2017, 44(8): 1958-1966
- Microbiology China, 2017, 44(8): 1958-1966
- DOI: 10.13344/j.microbiol.china.160834
-
文章历史
- 收稿日期: 2016-11-16
- 接受日期: 2017-02-14
- 优先数字出版日期(www.cnki.net): 2017-02-27
红树林(Mangrove)是一个广泛分布于热带和亚热带特殊潮间带的生态系统,以红树植物为主体的常绿灌木或乔木组成的生物群落。在中国主要分布于海南、广西、广东、福建、浙江、台湾、香港、澳门等沿海地区,其中以海南省分布最广、种类也最多,是我国红树植物的分布中心[1]。植物内生真菌(endophytes)是指在整个生活史或是生活史的某一阶段能够定殖在宿主植物健康细胞之间或者细胞内,却不对其宿主产生明显病害症状的真菌[2]。
在生物系统中氧化过程是产生自由基的重要途径之一[3]。自由基是导致人类衰老的主要因素,在食品中添加适当的抗氧化剂能够防止和延缓机体的衰老和疾病[4-5]。一些人工合成的抗氧化剂,如丁基羟基茴香醚(BHA)、2, 6-二叔丁基-4-甲基苯酚(BHT)、叔丁基对苯二酚(TBHQ)被作为食品添加剂使用,但由于这些人工合成的抗氧化剂会对人体产生副作用,因而被禁止使用[6]。因此,人们希望能从自然界中寻求到高效低毒的天然抗氧剂,自1993年Stierle等[7]首次从短叶红豆杉(Taxus brevifolia)的内生真菌Taxomyces andreanae中分离到紫杉醇,内生真菌作为重要类群被广泛研究。红树林特殊的生境必然带来红树林内生真菌资源的丰富和种类的多样性,目前超过280种的红树林内生真菌已被分离鉴定[8-9]。红树林内生真菌与红树林中其他类群的相互作用再加上环境因子的胁迫,使得红树林内生真菌在不断地进化下形成特殊的群落,能够代谢出陆源真菌无法比拟的新颖结构和具有特殊功能的生物活性物质,成为发现新的活性化合物和先导化合物的重要来源[10]。越来越多的研究工作者将目光投向红树林内生真菌的研究,为了寻找到有价值的生物活性成分,并应用于环境、农业和医药等领域。目前从红树林内生真菌中得到的代谢产物有耐盐、溶磷、抗氧化、抗菌、抗肿瘤等作用[11]。本实验室一直从事红树林内生真菌和生物活性相关研究,课题组Xu等[12-15]从红茄苳一株拟盘多毛孢菌种分离出40个新化合物。本研究从海南岛东寨港红树林国家自然保护区药用植物红茄苳(R. mucronata)中分离获得一株能产生较高抗氧化活性的内生真菌,对其进行生物学鉴定和发酵产物抗氧化活性的评价,以期为开发利用提供理论依据。
1 材料与方法 1.1 材料 1.1.1 主要试剂和仪器: Taq DNA聚合酶、dNTPs、10×Taq buffer、D2000 DNA ladder均购自中科瑞泰(北京)生物科技有限公司;2-2′二苯基-1-三硝基苯肼(DPPH)和2′-联氨-双-3-乙基苯并噻唑啉-6-磺酸(ABTS)购自Sigma公司;氯仿、乙醇、异戊醇、琼脂糖、β-巯基乙醇、葡萄糖均为分析纯试剂。灭菌锅HVE-50,日本HIRAYAMA公司;超净工作台BCM-1300,苏州苏洁净设备有限公司;恒温箱MP-160,上海福马实验设备有限公司;PCR扩增仪,德国Biometra公司;DYY-Ⅱ型电泳仪,北京市六一仪器厂;冷冻离心机5415,德国Eppendorf公司;酶标仪XMARK,美国Bio-Rad公司。 1.1.2 样品采集: 样品采自海南岛东寨港红树林国家自然保护区,属于热带海洋性气候区域,年平均气温23.8℃,年平均降雨量1 676 mm。得天独厚的地理条件造就了东寨港红树林物种的多样性,世界上红树林植物一共有23科81种,而海南岛红树林的种类有23科41种。因此该红树林也成为国内外研究者研究湿地物种多样性的重要样地。健康红茄苳(R. mucronata)植物的花采集后置于塑料袋中,存放于4 ℃备用。 1.1.3 培养基: 内生真菌分离PDA培养基(g/L):马铃薯(去皮) 200.0,葡萄糖20.0,人工海水1 000 mL,pH 7.0–7.2,琼脂15.0–20.0。内生真菌麦麸发酵培养基[16]:小米7.5 g、麸皮7.5 g作为基础天然基质加入容量200 mL口径6 cm的圆形玻璃罐头瓶中,再加入由0.5 g酵母膏和0.5 g琥珀酸溶于10 mL水的液体基质,搅拌均匀,1×105 Pa灭菌30 min后,加入5 mL水充分搅拌,同条件灭菌30 min,备用。 1.2 内生真菌的分离与鉴定 1.2.1 内生真菌的分离: 将采集的样品用自来水清洗干净,备用。参考Schulz等方法进行内生真菌的分离[17],在超净工作台中依次用75%乙醇浸泡60 s,2%次氯酸钠浸泡30 s,无菌水清洗3次。以上操作重复3次,最后一次的无菌水作为空白对照。用刀片切除材料的边缘,并用刀片将植物切成5 mm×5 mm的小组织块。将这些组织块接入PDA平板培养基上,置于28 ℃恒温培养箱中倒置培养3-7 d。 1.2.2 内生真菌的鉴定: 将分离纯化的菌株接种至新的PDA培养基上,生长7 d,用盖玻片从培养皿中刮取菌丝,采用CTAB法提取DNA[18],以总DNA为模板,采用引物ITS1F (5′-CTTGGTCATTTAGAG GAAGTAA-3′)和ITS4 (5′-TCCTCCGCTTATTGATA TGC-3′)对ITS内转录间隔区进行PCR扩增[19-20]。PCR反应体系:DNA模板1.0 μL,正向引物(10 μmol/L) 1.0 μl,反相引物(10 μmol/L) 1.0 μL,dNTP mixture (2.5 mmol/L) 1.0 μL,Taq DNA聚合酶(2 U/μL) 1.0 μL,10×Taq buffer 5.0 μL,ddH2O 40 μL。PCR反应条件:94 ℃ 5 min;94 ℃ 40 s,55 ℃ 40 s,72 ℃ 55 s,30个循环;72 ℃ 10 min。PCR产物经处理后送至上海英潍捷基公司进行测序。测序获得的ITS序列在GenBank中进行BLAST比对分析[21]。 1.3 菌株抗氧化活性筛选采用ABTS法进行内生真菌发酵产物抗氧化活性筛选[22],在96孔板中取195 μL ABTS自由基溶液(120 μmol/L)加入10 μl待测液,反应30 min后用全波长酶标仪在734 nm处测得吸光值,清除率=[(A空白-A样品)/A空白]×100%。
1.4 内生真菌发酵培养和产物提取参考Juan-Badaturuge等研究方法[23],对活化后的活性菌株HQD24接种至麦麸固体培养基上,进行28 d的发酵培养[24],发酵产物用乙酸乙酯浸泡提取,回收浓缩。用水溶解浸膏,依次用石油醚、二氯甲烷、乙酸乙酯、正丁醇进行1:3体积比的萃取,重复3次,反萃取一次,回收浓缩有机溶剂,制得不同有机溶剂萃取浸膏。
1.5 内生真菌发酵提取物的抗氧化活性 1.5.1 DPPH自由基的测定: 菌株发酵提取物清除DPPH自由基能力的测定参考Jing等的研究方法,在实验过程中待测物提供氢原子与DPPH自由基结合,使其颜色发生改变,进而推测出待测物的抗氧化活性[25]。用60%的乙醇溶解不同有机溶剂萃取浸膏,并配制成0.5、1.0、1.5 g/L三个梯度浓度,分别取0.1 mL待测样品到试管中再加入3.9 mL的DPPH自由基,反应30 min在517 nm处测其吸光值,同时做空白处理,以维生素C (VC)和BHT为阳性对照,重复3次。 1.5.2 ABTS自由基的测定: 通过参考Li等研究方法测定菌株发酵提取物清除ABTS自由基能力[22],在准确称取0.192 15 g ABTS于50 mL的容量瓶中,用无水乙醇定容,摇匀,浓度7 mmol/L;7 mmol/L ABTS与2.45 mmol/L的高硫酸钾等体积混合,在室温、避光黑暗的条件下,静置反应12-16 h形成ABTS自由基储备液。用无水乙醇稀释成工作液,于波长734 nm处测得其吸光度为0.70±0.02,再装入棕色试剂瓶中,4℃冷藏以备用。分别取0.1 mL不同浓度的待测样品置于试管中,再加入3.9 mL的ABTS自由基,反应30 min,在734 nm测出吸光值,同时做空白处理,以VC和BHT为阳性对照,重复3次,计算清除率。 1.5.3 超氧自由基的测定: 在菌株发酵提取物超氧自由基能力测定中,分别取1 mL 150 μmol/L的四唑硝基兰(NBT)和468 μmol/L的烟酰胺腺嘌呤二核苷二钠(NADH)溶液到试管中,再加入不同浓度的待测液1 mL,此反应在加入1 mL 60 μmol/L的5-甲基吩嗪硫酸甲酯(PMS)溶液后开始反应,25 ℃反应5 min后在560 nm下测其吸光值,同时做空白处理[26],以BHT和VC为阳性对照,计算清除率。 1.5.4 还原Fe3+的测定: 根据Guo等研究方法并适当调整,测定菌株发酵提取物Fe3+的还原能力[27],取1 mL不同浓度的待测液于试管中,依次加入pH 6.6的磷酸盐缓冲溶液(0.2 mol/L) 2.5 mL和1% K3Fe(CN)6溶液2.5 mL后混合均匀,混合液于50 ℃水浴20 min,再加入10%的三氯乙酸2.5mL。于3 000 r/min离心10 min,取2.5 mL的上清液再依次加2.5 mL蒸馏水和0.5 mL 0.1%的FeCl3混合均匀,静置10 min在700 nm处测定吸光值,以没食子酸为阳性对照,在700 nm下测得吸光值,吸光值越高表明还原力越强。 1.5.5 Fe2+螯合反应测定: 菌株提取物Fe2+螯合能力测定参考Decker等[28]的研究方法,分别取1 mL不同浓度待测液于试管中,加入100μl的2 mmol/L FeCl2·4H2O和3.7 mL的蒸馏水,再加入200 μL 5 mmol/L的Ferrozine,在室温下反应20 min,在562 nm下测得吸光值,并做空白处理,以EDTA为阳性对照,计算出清除率。 2 结果与分析 2.1 内生真菌HQD24的分离从东寨港红树林国家自然保护区植物红茄苳花中分离出内生真菌。通过清除ABTS自由基法,筛选出菌株HQD24发酵产物对ABTS自由基有很强的作用。
HQD24菌落在PDA培养基上生长迅速,在25-28℃培养生长5-7 d可达50 mm,菌落边缘均匀、平滑,质地呈丝绒状或发絮状,分生孢子结构大量或较少,中部多边缘少,近于百合绿,带灰的橄榄色或海狸灰;菌落反面黄褐色、淡黄色或带绿的淡黄色(图 1A、B)。大量分生孢子梗发生于基质,不分枝,无色,无隔,光滑,直立,丛生,(50.0-650.0)μm×(4.0-9.5)μm,分生孢子梗顶端膨大形成顶囊,顶囊烧瓶状,直径20 μm-30μm,产孢结构瓶梗以放射状分布于顶囊表面,单层,分生孢子球形或近球形(图 1C),参考中国真菌志曲霉属(Aspergillus)中的烟曲霉其形态特征相似,初步判定为烟曲霉(Aspergillus fumigatus)[29]。

|
| 图 1 菌株HQD24的形态特征和产孢结构 Figure 1 Colony morphology and conidiogenous structure of strain HQD24 注:A、B:菌落形态特征;C:菌株产孢结构. Note: A, B: The colony morphology of strain HQD24; C: The conidiogenous structure of strain HQD24. |
|
|
将内生真菌HQD24的总DNA提取后作为模板,使用引物ITS1F和ITS4进行PCR扩增,回收产物后测序,获得的ITS序列通过BioEdit 7.1.9软件编辑,并将序列提交到NCBI获取登录号为KX618209。
将HQD24的ITS序列结果与GenBank数据库进行比对分析,下载相似度较高的参比序列,采用MEGA 6.0软件对其构建系统发育树(图 2)。
|
| 图 2 菌株HQD24与GenBank中参考菌株ITS rDNA构建的系统发育树 Figure 2 Phylogenetic tree based on the ITS rDNA sequences of HQD24 and its GenBank allies 注:从GenBank中下载相关参考序列,并与HQD24构建系统发育树,在分支点上显示了重复1 000次大于60%的自展支持率,Peziza vesiculosa作为外源菌. Note: HQD24 was used in the construction of the clustering together with a reference sequence retrieved from GenBank. The bootstrap numbers shown on the left (≥60%) were obtained using 1 000 replicates. The fungus Peziza vesiculosa was used as outgroup for the construction of the tree. |
|
|
通过HQD24 ITS序列与参比序列比对分析,发现菌株HQD24与烟曲霉(Aspergillus fumigatus)的参比序列KT972124、KP724998、KF494830形成稳定分支,其支持率为87%,并与这3条参比序列的鉴别率和覆盖率均为100%,再结合菌株形态特征鉴定菌株HQD24为曲霉属(Aspergillus)的烟曲霉(Aspergillus fumigatus)。
2.3 内生真菌发酵提取物抗氧活性 2.3.1 DPPH自由基测定: 烟曲霉在麦麸培养基上发酵培养28 d后,经乙酸乙酯粗提,浓缩回收得浸膏。用石油醚、二氯甲烷、乙酸乙酯、正丁醇依次萃取,得各段浸膏。采用清除DPPH自由基法测定各萃取物抗氧化活性的能力。清除DPPH自由基能力随着浓度的增加而增强,当不同有机溶剂萃取浸膏质量浓度为1.5 g/L时,清除DPPH自由基的能力为:BHT (99.87%)>VC (99.80%)>正丁醇萃取物(20.81%)>乙酸乙酯萃取物[18.68%>二氯甲烷萃取物(18.61%)]>石油醚萃取物(5.51%),这表明烟曲霉发酵产物中具有生物活性的物质极性差异较大,主要分布于正丁醇、乙酸乙酯和二氯甲烷有机溶剂中,而石油醚萃取物中的抗氧化活性能力最低(图 3)。

|
| 图 3 菌株HQD24乙酸乙酯提取物的不同极性段浸膏对DPPH自由基清除率 Figure 3 The scavenging capacity on DPPH radical of different fractions of crude extraction from strain HQD24 |
|
|
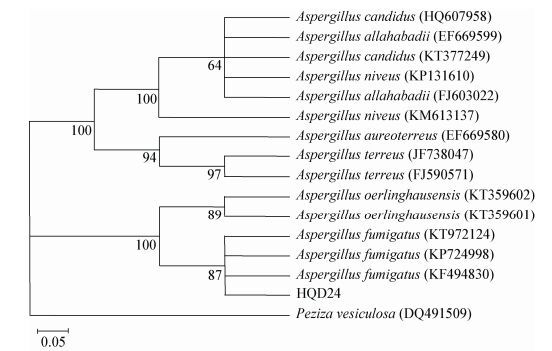
|
| 图 4 菌株乙酸乙酯段提取物的不同极性段浸膏对ABTS自由基清除率 Figure 4 The scavenging capacity on ABTS radical of different fractions of crude extraction from strain HQD24 |
|
|
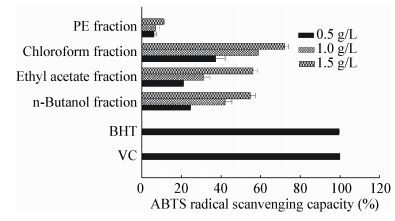
|
| 图 5 菌株乙酸乙酯段提取物的不同极性段浸膏对超氧自由基清除率 Figure 5 The scavenging capacity on superoxide radical of different fractions of crude extraction from strain HQD24 |
|
|
|
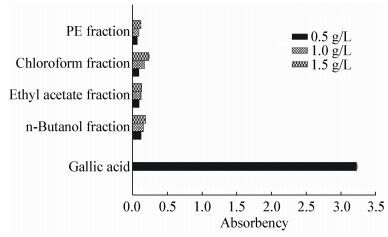
| 图 6 菌株乙酸乙酯段提取物的不同极性段浸膏还原能力的测定 Figure 6 The Fe3+ reducing capacity of different fractions of crude extraction from strain HQD24 |
|
|

|
| 图 7 菌株乙酸乙酯段提取物的不同极性段浸膏螯合Fe2+的测定 Figure 7 The ferrous ion chelating capacity of different fractions of crude extraction from strain HQD24 |
|
|
红树林内生真菌资源的多样性必定带来代谢产物的多样性,同样代谢产物的应用也呈现多样性。红树林内生真菌代谢物质应用涉及多方面,如提高红树林植物耐盐、抗逆性、病虫害防治、促进植物生长、抗氧化、抗肿瘤、抗菌抗炎等作用,红树林内生真菌是人类的天然资源宝库[11]。。
赵云涛等[34]研究红树林内生真菌的抗氧化作用发现,大部分内生真菌具有清除羟自由基、超氧阴离子自由基的作用。刘伟等[35]筛选红树植物无瓣海桑、海马齿和秋茄中具有抗氧化活性的内生真菌,结果显示,分离得到25株内生真菌发酵产物对DPPH自由基、ABTS自由基和羟基自由基具有较强清除作用(0<EC50<1 g/L)的菌株分别有3、8、12株。孙彬秩等[36]研究18株海洋内生真菌发酵产物生物活性,结果表明,样品150103乙酸乙酯提取液在浓度10 g/L时对DPPH自由基的清除率大于90%。本研究从药用植物红茄苳花中分离筛选出一株抗氧化活性强的内生真菌HQD24,采用分子生物学手段结合形态学鉴定,确定为曲霉属(Aspergillus)的烟曲霉(Aspergillus fumigatus)。抗氧化活性研究发现菌株麦麸发酵物的乙酸乙酯提取物具有清除DPPH自由基、ABTS自由基、超氧自由基和还原Fe3+、螯合Fe2+的能力,当浓度为1.5 g/L时,二氯甲烷部位ABTS自由基清除率为71.92%,正丁醇部位超氧自由基清除率为62.36%。这说明烟曲霉发酵乙酸乙酯提取物中,具有抗氧化活性的物质主要分布于二氯甲烷和正丁醇部位,其次是分布于乙酸乙酯部位,石油醚部位中抗氧化活性物质含量最少。从本研究结果来看,红茄冬内生烟曲霉是具有抗氧化活性的生物资源,其抗氧化活性物质方面值得进一步深入研究。
| [1] |
Lin P. A review on the mangrove research in China[J]. Journal of Xiamen University (Natural Science Edition), 2001, 40(2): 592-603. (in Chinese) 林鹏. 中国红树林研究进展[J]. 厦门大学学报:自然科学版, 2001, 40(2): 592-603. |
| [2] |
Petrini O. Fungal endophytes of tree leaves[A]//Andrews JH, Hirano SS. Microbial Ecology of Leaves[M]. New York: Springer, 1991: 179-197
|
| [3] |
Nikolić M, Glamočlija J, Ferreira ICFR, et al. Chemical composition, antimicrobial, antioxidant and antitumor activity of Thymus serpyllum L. Thymus algeriensis Boiss. and Reut. and Thymus vulgaris L. essential oils[J]. Industrial Crops and Products, 2013, 52: 183-190. |
| [4] |
Saad A, Fadli M, Bouaziz M, et al. Anticandidal activity of the essential oils of Thymus maroccanus and Thymus broussonetii and their synergism with amphotericin B and fluconazol[J]. Phytomedicine, 2010, 17(13): 1057-1060. DOI:10.1016/j.phymed.2010.03.020 |
| [5] |
Ali IBEH, Guetat A, Boussaid M. Genetic diversity, population structure and relationships of Tunisian Thymus algeriensis Boiss. et Reut. and Thymus capitatus Hoffm. et Link. assessed by isozymes[J]. Industrial Crops and Products, 2012, 36(1): 149-163. DOI:10.1016/j.indcrop.2011.08.021 |
| [6] |
Amarowicz R, Pegg RB, Rahimi-Moghaddam P, et al. Free-radical scavenging capacity and antioxidant activity of selected plant species from the Canadian prairies[J]. Food Chemistry, 2004, 84(4): 551-562. DOI:10.1016/S0308-8146(03)00278-4 |
| [7] |
Stierle A, Strobel G, Stierle D. Taxol and taxane production by Taxomyces andreanae, an endophytic fungus of Pacific yew[J]. Science, 1993, 260(5105): 214-216. DOI:10.1126/science.8097061 |
| [8] |
Liu AR, Wu XP, Xu T. Research advances in endophytic fungi of mangrove[J]. Chinese Journal of Applied Ecology, 2007, 18(4): 912-918. (in Chinese) 刘爱荣, 吴晓鹏, 徐同. 红树林内生真菌研究进展[J]. 应用生态学报, 2007, 18(4): 912-918. |
| [9] |
Gao J. Diversity and ecological distribution of endophytic fungi associated with mangroves[D]. Guangzhou: Master's Thesis of Guangdong Ocean University, 2013(in Chinese) 高剑. 红树林内生真菌多样性及其生态分布[D]. 广州: 广东海洋大学硕士学位论文, 2013 http://cdmd.cnki.com.cn/Article/CDMD-10566-1013225108.htm |
| [10] |
Liu F, Hong K. Microbial diversity of mangrove and its diversity[J]. Journal of Hainan Madical, 2006, 17(5): 171-173. (in Chinese) 刘峰, 洪葵. 红树林微生物及其代谢产物多样性[J]. 海南医学, 2006, 17(5): 171-173. |
| [11] |
Xu J. The Study on Natural Products of Mangrove Microorganism[M]. Beijing: Science Press, 2015, 7-8. (in Chinese) 徐静. 红树林微生物天然产物化学研究[M]. 北京: 科学出版社, 2015, 7-8.
|
| [12] |
Xu J, Kjer J, Sendker J, et al. Cytosporones, coumarins, and an alkaloid from the endophytic fungus Pestalotiopsis sp. isolated from the Chinese mangrove plant Rhizophora mucronata[J]. Bioorganic & Medicinal Chemistry, 2009, 17(20): 7362-7367. |
| [13] |
Xu J, Kjer J, Sendker J, et al. Chromones from the endophytic fungus Pestalotiopsis sp. isolated from the Chinese mangrove plant rhizophora mucronata[J]. Journal of Natural Products, 2011, 72(4): 662-665. |
| [14] |
Xu J, Aly AH, Wray V, et al. Polyketide derivatives of endophytic fungus Pestalotiopsis sp. isolated from the Chinese mangrove plant Rhizophora mucronata[J]. Tetrahedron Letters, 2011, 52(1): 21-25. DOI:10.1016/j.tetlet.2010.10.131 |
| [15] |
Xu J, Lin Q, Wang B, et al. Pestalotiopamide E, a new amide from the endophytic fungus Pestalotiopsis sp.[J]. Journal of Asian Natural Products Research, 2011, 13(4): 373-376. DOI:10.1080/10286020.2011.554829 |
| [16] |
Wang WL, Wang LP, Wang C, et al. Alkaloids from Aspergillus sp. OUCMDZ-3658 associated with soft coral[J]. Chinese Journal of Marine Drugs, 2015, 34(6): 1-11. (in Chinese) 王文玲, 王立平, 王聪, 等. 珊瑚真菌Aspergillus sp. OUCMDZ-3658产生的生物碱[J]. 中国海洋药物, 2015, 34(6): 1-11. |
| [17] |
Schulz B, Wanke U, Draeger S, et al. Endophytes from herbaceous plants and shrubs: effectiveness of surface sterilization methods[J]. Mycological Research, 1993, 97(12): 1447-1450. DOI:10.1016/S0953-7562(09)80215-3 |
| [18] |
Fredlund E, Gidlund A, Olsen M, et al. Method evaluation of Fusarium DNA extraction from mycelia and wheat for down-stream real-time PCR quantification and correlation to mycotoxin levels[J]. Journal of Microbiological Methods, 2008, 73(1): 33-40. DOI:10.1016/j.mimet.2008.01.007 |
| [19] |
White TJ, Bruns T, Lee S, et al. Amplification and direct sequencing of fungal ribosomal RNA genes for phylogenetics[A]//Innis MA, Gelfand DH, Sninsky JJ, eds. PCR Protocols: A Guide to Methods and Applications[M]. San Diego: Academic Press, 1990: 315-322
|
| [20] |
Gardes M, Bruns TD. ITS primers with enhanced specificity for Basidiomycetes-application to the identification of mycorrhizae and rusts[J]. Molecular Ecology, 1993, 2(2): 113-118. DOI:10.1111/j.1365-294X.1993.tb00005.x |
| [21] |
Fernandes EG, Pereira OL, Silva CCD, et al. Diversity of endophytic fungi in Glycine max[J]. Microbiological Research, 2015, 181: 84-92. DOI:10.1016/j.micres.2015.05.010 |
| [22] |
Li D, Zhou J, Xia J, et al. Antioxidant activities of extract and fractions from Clerodendrum inerme[J]. Journal of Chemical and Pharmaceutical Research, 2015, 7(8): 875-879. |
| [23] |
Juan-Badaturuge M, Habtemariam S, Thomas MJK. Antioxidant compounds from a South Asian beverage and medicinal plant, Cassia auriculata[J]. Food Chemistry, 2011, 125(1): 221-225. DOI:10.1016/j.foodchem.2010.08.065 |
| [24] |
Narendran R, Kathiresan K. Antimicrobial activity of crude extracts from Mangrove-derived Trichoderma, species against human and fish pathogens[J]. Biocatalysis and Agricultural Biotechnology, 2016, 6: 189-194. DOI:10.1016/j.bcab.2016.03.003 |
| [25] |
Jing Z, Zheng XX, Qi Y, et al. Optimization of ultrasonic-assisted extraction and radical-scavenging capacity of phenols and flavonoids from Clerodendrum cyrtophyllum turcz leaves[J]. PLoS One, 2013, 8(7): e68392. DOI:10.1371/journal.pone.0068392 |
| [26] |
Nagai T, Inoue R, Inoue H, et al. Scavenging capacities of pollen extracts from Cistus ladaniferus, on autoxidation, superoxide radicals, hydroxyl radicals, and DPPH radicals[J]. Nutrition Research, 2002, 22(4): 519-526. DOI:10.1016/S0271-5317(01)00400-6 |
| [27] |
Guo T, Wei L, Sun J, et al. Antioxidant activities of extract and fractions from Tuber indicum Cooke & Massee[J]. Food Chemistry, 2011, 127(4): 1634-1640. DOI:10.1016/j.foodchem.2011.02.030 |
| [28] |
Decker EA, Welch B. Role of ferritin as a lipid oxidation catalyst in muscle food[J]. Journal of Agricultural and Food Chemistry, 1990, 38(3): 674-677. DOI:10.1021/jf00093a019 |
| [29] |
Qi ZT. Chinese Journal of Fungi[M]. Beijing: Science Press, 1997, 18-20. (in Chinese) 齐祖同. 中国真菌志第五卷:曲霉属及其相关有性型[M]. 北京: 科学出版社, 1997, 18-20.
|
| [30] |
Zhu YC, Jiao BN. Research progress on ABTS assay in determination of TAA in fruits and vegetables in vitro[J]. Food and Fermentation Industries, 2005, 31(8): 77-80. (in Chinese) 朱玉昌, 焦必宁. ABTS法体外测定果蔬类总抗氧化能力的研究进展[J]. 食品与发酵工业, 2005, 31(8): 77-80. |
| [31] |
Korycka-Dahl M, Richardson T. Photogeneration of superoxide anion in serum of bovine milk and in model systems containing riboflavin and amino acids[J]. Journal of Dairy Science, 1978, 61(4): 400-407. DOI:10.3168/jds.S0022-0302(78)83613-3 |
| [32] |
Meir S, Kanner J, Akiri B, et al. Determination and involvement of aqueous reducing compounds in oxidative defense systems of various senescing leaves[J]. Journal of Agricultural and Food Chemistry, 1994, 43(7): 1813-1819. |
| [33] |
Halliwell B, Murcia MA, Chirico S, et al. Free radicals and antioxidants in food and in vivo: what they do and how they work[J]. Critical Reviews in Food Science and Nutrition, 1995, 35(1/2): 7-20. |
| [34] |
Zhao YT, Li QR, Chen SH, et al. Antioxidant activity of mangrove endophytic fungi[J]. Journal of Zhanjiang Ocean University, 2005, 25(6): 93-96. (in Chinese) 赵云涛, 李倩茹, 陈绍红, 等. 红树林内生真菌的抗氧化作用[J]. 湛江海洋大学学报, 2005, 25(6): 93-96. |
| [35] |
Liu W, Ni H, Huang GL, et al. Screening of endophytic fungi with antibacterial, antioxidant and antitumor activities from mangrove plants[J]. Acta Laser Biology Sinica, 2012, 21(6): 569-574. (in Chinese) 刘伟, 倪辉, 黄高凌, 等. 从红树植物中筛选具有抗菌、抗氧化和抗肿瘤活性的内生真菌[J]. 激光生物学报, 2012, 21(6): 569-574. |
| [36] |
Sun BZ, Tian ZH, Liu X. Preliminary screening and biological activity of fermentation products of 18 marine endophytic fungi strains[J]. Food & Machinery, 2016(2): 41-43. (in Chinese) 孙彬秩, 田振华, 刘旭. 18株海洋内生真菌发酵产物初步筛选及活性研究[J]. 食品与机械, 2016(2): 41-43. |
 2017, Vol. 44
2017, Vol. 44