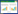扩展功能
文章信息
- 杨移斌, 胥宁, 董靖, 杨秋红, 刘永涛, 艾晓辉
- YANG Yi-Bin, XU Ning, DONG Jing, YANG Qiu-Hong, LIU Yong-Tao, AI Xiao-Hui
- 台湾泥鳅源维氏气单胞菌Zy01株的分离鉴定及药敏特性研究
- Isolation and identification of Aeromonas veronii strain Zy01 from Taiwan Loach and its antibiotic sensitivity
- 微生物学通报, 2017, 44(4): 852-858
- Microbiology China, 2017, 44(4): 852-858
- DOI: 10.13344/j.microbiol.china.160390
-
文章历史
- 收稿日期: 2016-05-15
- 接受日期: 2016-09-09
- 优先数字出版日期(www.cnki.net): 2016-09-29
2. 淡水水产健康养殖湖北省协同创新中心 湖北 武汉 430223
2. Hubei Freshwater Aquaculture Collaborative Innovation Center, Wuhan, Hubei 430223, China
台湾泥鳅又名台湾龙鳅、台湾鳗鳅、台湾大黄鳅等[1],是中国台湾改良的泥鳅养殖新品种,分类地位不明确。2012年,台湾泥鳅开始被内地少数养殖单位养殖,因个体大、雌雄生长无差异、产量高而引起业界轰动,养殖发展势头迅猛[2]。台湾泥鳅养殖适宜水温为15−30 ℃,食物来源广泛,几乎可以摄食各种天然饵料,同时也喜食各种性状的人工配合饵料,是一种比较理想的养殖新品种。随着台湾泥鳅在内地养殖的发展,病害也日渐增多,对养殖生产效益产生了一定的影响[3]。
维氏气单胞菌 (Aeromonas veronii) 在养殖水体中普遍存在,属条件致病菌[4]。目前关于维氏气单胞菌引发水产养殖动物疾病的报道日益增多,给水产养殖业带来了较大的经济损失。鱼类感染维氏气单胞菌后主要出现皮下点状溃烂、皮肤隆起等症状[5]。
2015年11月辽宁某台湾泥鳅养殖场出现死亡病例,发病较快,死亡率较高。笔者现场取样后分离得到一株优势菌,通过回归感染、生理生化特征测定、16S rRNA基因序列分析对该病原进行确诊和鉴定,并研究了其药敏特性,以期为台湾泥鳅维氏气单胞菌病的防控提供参考依据。
1 材料与方法 1.1 材料 1.1.1 试验用鱼: 10尾发病的台湾泥鳅购自辽宁某养殖场,具备该病的典型症状;健康台湾泥鳅 (15±5 g) 购自武汉某水产市场,体格健壮,无伤病,暂养7 d无异常后用于试验。 1.1.2 主要试剂和仪器: 普通营养琼脂、水解酪蛋白琼脂 (MH)、脑心浸出液肉汤 (BHI)、革兰氏染色液及药敏纸片、细菌微量生化鉴定管购自杭州滨和微生物试剂有限公司;细菌基因组DNA提取试剂盒、PCR扩增细菌16S rRNA基因试剂盒均购自生工生物工程 (上海) 股份有限公司。无菌操作台、摇床及高压灭菌锅购自上海博讯实业有限公司;离心机及恒温培养箱购自上海恒一科学仪器有限公司;PCR仪购自赛飞 (中国) 有限公司。 1.2 方法 1.2.1 病害临床诊断: 对养殖场台湾泥鳅发病死亡情况进行评估,实地查看养殖水环境,了解发病台湾泥鳅规格大小。对多个死亡病例进行观察以确定该疾病的典型特征,并取具有典型症状的样品进行病原的分离与纯化。 1.2.2 细菌分离纯化: 取具有典型皮下肌肉溃烂症状的濒死的台湾泥鳅10尾,用70%的酒精进行体表消毒,在无菌环境下取其肝、肾脏、溃烂肌肉及血水用于细菌分离,划线接种于普通营养琼脂平板上,置于28 ℃培养24 h后挑取形态、大小、颜色等特征基本一致的优势菌落进一步纯化,纯化后的菌株用含25%甘油的脑心浸出液培养基保存于–80 ℃备用。 1.2.3 回归感染: 将分离纯化后的细菌接种于普通营养琼脂平板上28 ℃培养24 h,用无菌生理盐水洗下菌苔,参照麦氏比浊法调整菌悬液浓度为4.0×107 CFU/mL[6]。选取健康台湾泥鳅用于回归感染试验,分为攻毒组和对照组,每组鱼的数量均为10尾,攻毒组和对照组均设2个重复。试验期间,水体溶氧保持在6.0−7.5 mg/L,水温25−28 ℃,保持水质良好,不投喂饵料。攻毒组每尾台湾泥鳅在其胸鳍基部注射浓度4.0×107 CFU/mL菌悬液,注射量为0.1 mL/尾,对照组在相同部位注射同等剂量的无菌生理盐水。每隔12 h观察台湾泥鳅的发病情况,记录死亡尾数,并对濒死的台湾泥鳅进行解剖,观察器官病理变化,同时进行细菌的再分离。
1.2.4 细菌LC50测定: 将细菌悬液分别稀释至以下5个浓度:4.2×104、4.2×105、4.2×106、4.2×107、4.2×108 CFU/mL,然后分别从胸鳍基部注射到健康的台湾泥鳅体内进行感染,每尾注射剂量为0.1 mL。对照组的台湾泥鳅注射等量的无菌生理盐水,攻毒组及对照组均设置2个重复。水温保持在25−28 ℃,试验周期为15 d,连续观察台湾泥鳅表现,并记录试验鱼的死亡数,并用概率单位图解法[7]计算半数致死浓度 (LC50)。 1.2.5 细菌生理生化特征测定: 将分离菌接种于普通营养琼脂平板上,28 ℃培养24 h后观察菌落的大小、形态及颜色,同时进行革兰氏染色,采用光学显微镜观察细菌形态,其他各项生理生化指标的测定参照文献[8],采用细菌微量生化鉴定管进行测定。 1.2.6 细菌16S rRNA基因序列分析: 按照细菌DNA提取试剂盒说明书提取分离菌的DNA。细菌16S rRNA基因扩增通用引物由生工生物工程 (上海) 股份有限公司合成,引物序列为:正向27F:5′-AGAGTTTGATC (C/A) TGGCTCAG-3′;反向1492R:5′-GGTTACCTTGTTACGACTT-3′。PCR反应体系 (50 μL):无菌蒸馏水36.5 μL,10×PCR缓冲液 (含Mg2+) 5 μL,10 mmol/L dNTPs 1 μL,10 μmol/L正向和反向引物各1 μL,rTaq DNA聚合酶 (5 U/μL) 0.5 μL,菌液5 μL。PCR反应条件:95 ℃ 3 min;94 ℃ 35 s,55 ℃ 35 s,72 ℃ 1 min,35个循环;72 ℃ 10 min。PCR扩增后的产物经1.0%琼脂糖凝胶电泳检测目的条带,后将PCR产物送生工生物工程 (上海) 股份有限公司进行纯化和序列测定。将得到的16S rRNA基因序列通过NCBI进行BLAST,根据比对结果检索出同源性较高的序列采用ClustalX软件进行多序列匹配分析,用MEGA 5.0软件包中的Neighbor-Joining法构建系统进化树,通过1 000次Bootstrap检验置信度。
1.2.7 药物敏感性测定: 采用纸片扩散法 (K-B法),将分离菌接种于营养肉汤,28 ℃、200 r/min培养18 h后,稀释菌液浓度至107 CFU/mL,取200 μL均匀涂布于MH琼脂平板上,贴上不同的药敏纸片,置于28 ℃培养箱中培养24 h后测量抑菌圈直径 (mm),根据杭州滨和微生物试剂有限公司药敏纸片抑菌圈标准确定该菌株对药物的敏感程度。 2 结果与分析 2.1 临床主要症状发病台湾泥鳅的养殖场水质较差,水色发黑,氨氮偏高,最高达到0.4 mg/L。发病率在40%左右,死亡率70%左右,规格主要集中在可以上市的商品台湾泥鳅 (100 g左右)。发病的典型症状表现为体表两侧呈隆起状,皮肤下面有溃烂点,肌肉溃烂成脓状物,溃烂处有脓状物流出;解剖后发现其肝脏及胰脏发黑,肾脏充血,心脏肿大,腹腔内有腹水。
|
| 图 1 台湾泥鳅死亡率与菌液浓度对数的关系曲线 Figure 1 The relation curve of Taiwan loach mortality with logarithm of bacterial concentration |
|
|
从自然发病的台湾泥鳅肌肉溃烂处分离到一株优势菌,命名为Zy01,经过人工回归感染试验,Zy01对台湾泥鳅具有致病性,死亡率达到80%,感染后发病的台湾泥鳅也出现与自然发病的鱼相似的症状,并从感染后濒死的鱼体内又分离到与菌株Zy01形态特征及理化特性一致的菌株。根据试验鱼死亡率 (%) (表 1) 与菌液浓度对数[lg (CFU/mL)]建立的关系曲线:y=0.25x−1.075 (图 1),分离菌株Zy01对台湾泥鳅的半数致死浓度LC50=2.0×106 CFU/mL,根据Devesa对鱼类致病菌毒力的划分标准[9],可判定菌株Zy01对台湾泥鳅具有很强的毒力。
| 组别 Group |
数量 Amount |
细菌浓度 Bacteria concentration (CFU/mL) |
细菌浓度 对数 Logarithm of bacteria concentration lg(CFU/mL) |
死亡量 Amount of death |
死亡率 Mortality (%) |
| A | 10 | 4.2×104 | 4.62 | 0 | 0 |
| B | 10 | 4.2×105 | 5.62 | 4 | 40 |
| C | 10 | 4.2×106 | 6.62 | 6 | 60 |
| D | 10 | 4.2×107 | 7.62 | 9 | 90 |
| E | 10 | 4.2×108 | 8.62 | 10 | 100 |
菌株Zy01为革兰氏阴性杆菌,具有运动性。如表 2所示,菌株Zy01生理生化特征与维氏气单胞菌 (Aeromonas veronii) 基本一致。分离菌株16S rRNA基因序列与已知基因序列比对,发现与菌株Zy01的16S rRNA基因序列同源性高的菌株均属于气单胞菌属,构建的系统发育树 (图 2) 显示菌株Zy01与维氏气单胞菌聚为一支,相似性达到99%,综合生理生化特征测定结果,菌株Zy01可判定为维氏气单胞菌。
| 测定项目 Test item |
Zy01 | A.veronii |
| 革兰氏染色 | − | − |
| Gram stain | ||
| 运动性 | + | + |
| Mobility | ||
| 氧化酶 | + | + |
| Oxidase | ||
| V-P反应 | + | + |
| V-P reaction | ||
| 产生吲哚 | + | + |
| Indole | ||
| 鸟氨酸脱羧酶 | − | − |
| Ornithine decarboxylase | ||
| 苯丙氨酸脱氨酶 | + | + |
| Phenylalanine deaminase | ||
| 赖氨酸脱羧酶 | + | + |
| Lysine decarboxylase | ||
| 精氨酸双水解酶 | − | − |
| Arginine dihydrolase | ||
| 麦芽糖 | + | + |
| Maltose | ||
| 木糖 | − | − |
| Xylose | ||
| 柠檬酸盐 | + | + |
| Citrate | ||
| D-甘露醇 | + | + |
| D-mannitol | ||
| D-甘露糖 | + | + |
| D-mannose | ||
| 硫化氢 | − | − |
| H2S | ||
| 丙二酸盐 | − | − |
| Malonate | ||
| 七叶灵水解 | + | + |
| Esculine hydrolysis | ||
| 棉子糖 | − | − |
| Raffinose | ||
| 鼠李糖 | − | − |
| Rhamnose | ||
| 海藻糖 | + | + |
| Trehalose | ||
| 尿素 | − | − |
| Urea | ||
| 山梨醇 | − | − |
| Sorbitol | ||
| 阿拉伯糖 | − | − |
| Arabinose | ||
| 纤维二糖 | + | + |
| Cellobiose | ||
| 明胶液化 | + | + |
| Gelatin liquefaction | ||
| D-葡萄糖产酸 | − | − |
| D-glucose to produce acid | ||
| D-葡萄糖产气 | − | − |
| D-glucose gas | ||
| 蜜二糖 | + | + |
| Melibiose | ||
| 注:+:阳性;−:阴性. | ||
| Note: +: Positive; −: Negative. | ||

|
| 图 2 基于菌株Zy01的16S rRNA基因序列同源性构建的系统发育树 Figure 2 Phylogenetic tree based on 16S rRNA gene sequence homolog of strain Zy01 注:括号内的数字为GenBank序列号;节点处的数字为bootstrap值. Note: Numbers in parenthesis represented GenBank accession number; Numbers at the branch points indicated the Bootstrap values. |
|
|
如表 3所示,菌株Zy01对环丙沙星、头孢拉定、诺氟沙星、阿奇霉素、头孢噻肟、新霉素、左氧氟沙星、妥布霉素、庆大霉素及丁胺卡那霉素高度敏感;对头孢唑林、痢特灵、红霉素、卡那霉素及链霉素中度敏感;对苯唑西林、青霉素、阿莫西林、磺胺异噁唑、氯霉素、氟苯尼考、克林霉素、利福平及多西环素不敏感。
| 药物 Drug |
抑菌圈直径判断标准 The judgment standard of inhibition zone diameter (mm) |
药物含量 Dose (μg/disc) |
抑菌圈直径 Inhibition zone diameter (mm) |
敏感性 Sensitivity |
||
| 耐药 Resistant |
中度敏感 Medium sensitivity |
高度敏感 Highly sensitive |
||||
| 环丙沙星Ciflox | ≤15 | 16−20 | ≥21 | 5 | 23±0.21 | S |
| 苯唑西林Oxacillin | ≤10 | 11−12 | ≥13 | 1 | 0 | R |
| 头孢唑林Cefazolin | ≤14 | 15−17 | ≥18 | 30 | 15±0.11 | I |
| 青霉素Penicillin | ≤19 | 20−27 | ≥28 | 10 | 0 | R |
| 头孢拉定Cefadroxil | ≤14 | 15−17 | ≥18 | 30 | 19±0.12 | S |
| 阿莫西林Amoxicillin | ≤13 | 14−17 | ≥18 | 20 | 0 | R |
| 痢特灵Furazolidone | ≤14 | 15−16 | ≥17 | 300 | 16±0.12 | I |
| 磺胺异噁唑Sulfisoxazole | ≤12 | 13−16 | ≥17 | 300 | 0 | R |
| 氯霉素Chloramphenicol | ≤12 | 13−17 | ≥18 | 300 | 10±0.13 | R |
| 氟苯尼考Florfenicol | ≤12 | 13−17 | ≥18 | 75 | 0 | R |
| 克林霉素Clindamycin | ≤14 | 15−20 | ≥21 | 2 | 0 | R |
| 利福平Rifampicin | ≤16 | 17−19 | ≥20 | 5 | 12±0.22 | R |
| 诺氟沙星Norfloxacin | ≤12 | 13−16 | ≥17 | 10 | 20±0.23 | S |
| 阿奇霉素Azithromycin | ≤13 | 14−17 | ≥18 | 15 | 21±0.14 | S |
| 头孢噻肟Cefotaxime | ≤14 | 15−22 | ≥23 | 30 | 30±0.25 | S |
| 红霉素Erythrocin | ≤13 | 14−22 | ≥23 | 15 | 14±0.02 | I |
| 新霉素Neomycin | ≤12 | 13−16 | ≥17 | 30 | 23±0.09 | S |
| 卡那霉素Kanamycin | ≤13 | 14−17 | ≥18 | 30 | 14±0.04 | I |
| 多西环素Doxycycline | ≤12 | 13−15 | ≥16 | 30 | 10±0.08 | R |
| 左氧氟沙星Levofloxacin | ≤13 | 14−16 | ≥17 | 5 | 24±0.08 | S |
| 链霉素Streptomycin | ≤11 | 12−14 | ≥15 | 10 | 13±0.02 | I |
| 妥布霉素Tobramycin | ≤12 | 13−14 | ≥15 | 10 | 17±0.07 | S |
| 庆大霉素Gentamicin | ≤12 | 13−14 | ≥15 | 10 | 16±0.09 | S |
| 丁胺卡那霉素Amikacin | ≤14 | 15−16 | ≥17 | 30 | 18±0.02 | S |
| 注:S:高度敏感;I:中度敏感;R:耐药. | ||||||
| Note: S: Highly sensitive; I: Medium sensitivity; R: Resistant. | ||||||
本研究从发病台湾泥鳅体内分离到的菌株Zy01被鉴定为维氏气单胞菌,该菌又名维罗纳气单胞菌、凡隆气单胞菌和维隆气单胞菌。根据新的分类,维氏气单胞菌隶属于气单胞菌科[10],是近些年来发现的一个新种。据报道该菌对水产动物具有很强的毒性,常对水产养殖造成较大的经济损失。如沈文英等[11]报道维氏气单胞菌引起中华鳖 (Trionyx sinensis) 病四肢、颈部和裙边等处均有溃烂等症状;黄文明等[12]报道了胭脂鱼 (Myxocyprinus asiaticus) 感染维氏气单胞菌引起出血死亡的病例;马英等[13]报道了维氏气单胞菌是鳗鲡病害的病原菌;黎炯等[14]报道了维氏气单胞菌可感染罗非鱼 (Oreochromis niloticus),导致罗非鱼肠道肿大、有积液、肌肉轻微出血并且大量死亡;马志宏等[15]和杨移斌等[5]也先后报道关于维氏气单胞菌对鲟 (Acipenser baerii Brandt) 的致病性。然而关于维氏气单胞菌感染台湾泥鳅的病例尚未有报道。本研究不仅证实台湾泥鳅是该菌的一种新的宿主,还测定了菌株Zy01对台湾泥鳅的半致死浓度,显示对台湾泥鳅具有很强的致病性。也可由此得出,维氏气单胞菌危害的水产养殖品种日益增多,需加强其防控技术研究,为养殖生产提供必要的技术支持,减少经济损失。
3.2 台湾泥鳅维氏气单胞菌病的药物防治本研究发现,菌株Zy01对环丙沙星、头孢拉定、诺氟沙星及阿奇霉素等10种抗生素高度敏感;对头孢唑林、痢特灵及红霉素等5种抗生素中度敏感;对苯唑西林、青霉素及阿莫西林等9种抗生素不敏感。本结果与以往研究结果不尽相同[12, 14-15],如维氏气单胞菌对相同的抗生素敏感情况不尽相同,出现这样结果的可能原因在于养殖环境、养殖模式及药物使用等的差异,病原菌产生了不同程度的耐药性。本结果与其他研究最大不同在于一些水产常用药物出现了耐药,如氟苯尼考及多西环素等,可能原因是养殖户在台湾泥鳅养殖过程中高剂量多次使用这两种抗生素导致的。为此在防控细菌性病害时应当进行药物敏感试验,筛选出有效药物,准确用量进行防控。本研究分离菌株Zy01对庆大霉素等多种抗生素高度敏感,为防控台湾泥鳅发生该病提供了充足依据,在实际防控中做到选择高度敏感抗生素轮换使用,按照说明书提示准确把握用量,用足疗程,使之发挥最大疗效。本文研究了分离菌株对环丙沙星、氯霉素、红霉素及诺氟沙星等数种禁药的敏感性,在此仅是用作研究菌株耐药性,生产上不能选择这些药物用于病害防控。
| [1] | Xu RW, Yu QL, Yang FS, et al. Key technique for pond culture of Misgurnus anguillicaudatus (Taiwan)[J]. Hebei Fisheries, 2015(2) : 30–31, 63. (in Chinese) 徐如卫, 俞奇力, 杨福生, 等. 台湾大泥鳅池塘养殖技术要点[J]. 河北渔业, 2015(2) : 30–31, 63. |
| [2] | Qiu CW, Wang HX, Chen DH, et al. Artificial reproduction and early development research of Taiwan Loach[J]. Fisheries Science & Technology Information, 2014, 41(6) : 284–289. (in Chinese) 邱楚雯, 王韩信, 陈迪虎, 等. 台湾泥鳅人工繁殖及早期发育的研究[J]. 水产科技情报, 2014, 41(6) : 284–289. |
| [3] | Zhao CC, Peng YA, Gong H, et al. Identification pathogen from Taiwan loach surface bleeding canker and its prevention measures[J]. Scientific Fish Farming, 2015(2) : 63–64. (in Chinese) 赵长臣, 彭勇鳌, 巩华, 等. 台湾泥鳅体表出血溃疡病的病原鉴定及防治措施[J]. 科学养鱼, 2015(2) : 63–64. |
| [4] | Zhao M, Wang KY, Wang J, et al. Tetracycline antibiotics resistance and its genetic determinants in Aeromonas veronii isolated from channel catfish (Ictalurus punctatus)[J]. Acta Hydrobiologica Sinica, 2014, 38(2) : 386–392. (in Chinese) 赵敏, 汪开毓, 王均, 等. 斑点叉尾源维氏气单胞菌对四环素类抗生素的耐药性及耐药基因的检测[J]. 水生生物学报, 2014, 38(2) : 386–392. DOI:10.7541/2014.55 |
| [5] | Yang YB, Xia YT, Qiu JQ, et al. Isolation and identification of Aeromonas veronii from sturgeon and its antibiotic sensitivity[J]. Sichuan Journal of Zoology, 2014, 33(3) : 414–418. (in Chinese) 杨移斌, 夏永涛, 邱军强, 等. 鲟源维氏气单胞菌分离鉴定及药敏特性研究[J]. 四川动物, 2014, 33(3) : 414–418. |
| [6] | Wang KY, Lu Y, Geng Y, et al. Ulcer disease pathology observed of Aeromonas veronii from the loach[J]. Reservoir Fisheries, 2008, 28(4) : 117–120. (in Chinese) 汪开毓, 陆艳, 耿毅, 等. 维里纳气单胞菌致泥鳅溃疡病的病理学观察[J]. 水利渔业, 2008, 28(4) : 117–120. |
| [7] | Xu SY, Bian RL, Chen X. Experimental Methodology of Pharmacology.3rd Edition[M]. Beijing: People's Medical Publishing House, 2002 . (in Chinese) 徐叔云, 卞如濂, 陈修. 药理实验方法学.第3版[M]. 北京: 人民卫生出版社, 2002 . |
| [8] | Dong XZ, Cai MY. Identification system manual of common bacteria[M]. Beijing: Science Press, 2001 . (in Chinese) 东秀珠, 蔡妙英. 常见细菌系统鉴定手册[M]. 北京: 科学出版社, 2001 . |
| [9] | Devesa S. First Report of Vibriosis in Turbot (Scophthalmus maximus) Cultured in Northwestern Spain: Fish and Shellfish Pathology[M]. New York: Academic Press, 1985 . |
| [10] | Li M, You ZL, Chen F, et al. Isolation and characterization of Aeromonas caviae from Penaeus vannamei Boone (Litopenaeus vannamei) in Guangdong Province[J]. Journal of Shanghai Ocean University, 2015, 24(4) : 579–586. (in Chinese) 李梅, 游卓霖, 陈锋, 等. 广东省南美白对虾豚鼠气单胞菌的分离鉴定[J]. 上海海洋大学学报, 2015, 24(4) : 579–586. |
| [11] | Shen WY, Li WF, Gao Y. Isolation and drug sensitivity study of pathogenic bacteria Aeromonas veronii from soft-shelled turtle, Trionyx sinensis[J]. Acta Hydrobiologica Sinica, 2010, 34(5) : 1060–1064. (in Chinese) 沈文英, 李卫芬, 高研. 中华鳖病原性维隆气单胞菌的分离及药敏试验[J]. 水生生物学报, 2010, 34(5) : 1060–1064. |
| [12] | Huang WM, Wang L, Ji GZ, et al. Identification and drug sensitivity of bacteria Aeromonas veronii and A.media isolated from Chinese sucker Myxocyprinus asiaticus[J]. Fisheries Science, 2013, 32(4) : 210–214. (in Chinese) 黄文明, 王利, 冀国桢, 等. 胭脂鱼维氏气单胞菌和中间气单胞菌的鉴定及药物敏感性[J]. 水产科学, 2013, 32(4) : 210–214. |
| [13] | Ma Y, Guan RZ, Guo SL, et al. Sequencing and phylogenetic analysis of 16S rRNA genes of pathogenic bacteria isolated from cultivated eels[J]. Journal of Huazhong Agricultural University, 2010, 29(6) : 758–763. (in Chinese) 马英, 关瑞章, 郭松林, 等. 鳗鲡病原菌16S rRNA基因序列测定及系统进化分析[J]. 华中农业大学学报, 2010, 29(6) : 758–763. |
| [14] | Li Q, Ye X, Lu MX, et al. Isolation and identification of Aeromonas veronii from Infected tilapia fry and analysis of its drug sensitivity[J]. Journal of Hydroecology, 2011, 32(3) : 132–136. (in Chinese) 黎炯, 叶星, 卢迈新, 等. 罗非鱼维氏气单胞菌的分离鉴定和药敏试验[J]. 水生态学杂志, 2011, 32(3) : 132–136. |
| [15] | Ma ZH, Yang H, Li TL, et al. Isolation and identification of pathogenic Aeromonas veronii isolated from infected Siberian sturgeon (Acipenser baerii)[J]. Acta Microbiologica Sinica, 2009, 49(10) : 1289–1294. (in Chinese) 马志宏, 杨慧, 李铁梁, 等. 西伯利亚鲟 (Acipenser baerii) 致病性维氏气单胞菌的分离鉴定[J]. 微生物学报, 2009, 49(10) : 1289–1294. DOI:10.3321/j.issn:0001-6209.2009.10.017 |
 2017, Vol. 44
2017, Vol. 44