扩展功能
文章信息
- 杨友联, 李树江, 刘作易
- YANG You-Lian, LI Shu-Jiang, LIU Zuo-Yi
- 虎耳草炭疽病病原菌鉴定
- Identification of Colletotrichum species associated with Saxifraga stolonifera anthracnose
- 微生物学通报, 2017, 44(4): 818-824
- Microbiology China, 2017, 44(4): 818-824
- DOI: 10.13344/j.microbiol.china.160285
-
文章历史
- 收稿日期: 2016-04-05
- 接受日期: 2016-06-12
- 优先数字出版日期(www.cnki.net): 2016-06-21
2. 六盘水师范学院生物研究所 贵州 水城 553004;
3. 贵州省农业科学院 贵州农业生物技术重点实验室 贵州 贵阳 550006
2. Institute of Biology, Liupanshui Normal University, Shuicheng, Guizhou 553004, China;
3. Guizhou Key Laboratory of Agricultural Biotechnology, Guizhou Academy of Agricultural Sciences, Guiyang, Guizhou 550006, China
虎耳草 (Saxifraga stolonifera Curt) 为虎耳草科虎耳草属多年生常绿植物,别名金丝荷叶、耳朵红、老虎耳等。虎耳草全草入药,具有清热解毒、祛湿消肿、凉血止血的功效,我国民间常用于治疗中耳炎、外伤出血、牙痛、湿疹、吐血、前列腺增生等多种疾病,疗效显著[1-3]。为满足制药企业原材料需求,在贵州六盘水、安顺等地进行了虎耳草人工栽培。在虎耳草栽培中炭疽病时有发生,造成了一定损失。鉴于目前尚未有虎耳草炭疽病病原学相关研究报道,本研究对虎耳草炭疽病病原菌进行分离鉴定,旨在为该病的防治奠定病原学基础。
1 材料与方法 1.1 主要试剂和仪器2×PCR Taq MasterMix,天根生化科技 (北京) 有限公司;GOLDVIEWⅠ型核酸染色剂,北京索莱宝科技有限公司;引物由上海捷瑞生物技术公司合成。
9700型PCR仪,美国Applied Biosystems公司;BX51显微镜,奥林巴斯株式会社。
1.2 标本采集、分离2012年8月从六盘水六枝虎耳草种植基地采集具有炭疽病病症的叶片,分别装入信封带回实验室,采用病斑组织块分离法对病原菌进行分离,分离菌株在马铃薯葡萄糖培养基 (potato dextrose agar,PDA)[4]斜面培养7-10 d后于4 ℃保存。
1.3 病原菌确认根据柯赫氏法则,采用活体接种进行致病性测试。将种植基地采挖回的虎耳草,去除老叶片及疑似有病斑的叶片,盆栽培养15 d后用于实验。选取无病斑、生长一致的健康叶片,蒸馏水清洗1次后无菌水清洗2次,再用75%的酒精棉球擦拭,自然晾干。采用刺伤和无刺伤两种方法接种。刺伤接种时用无菌接种针刺伤表皮,将活化的菌株用无菌打孔器 (直径5 mm) 打取菌饼接种到刺伤部位。以无菌PDA培养基接种作为对照,每个处理设5个重复。接种后用透明度较好的塑料袋罩住花盆保湿培养48 h后取弃。逐日观察虎耳草叶片表面的发病症状。发病后采用病斑组织块分离法分离,镜检,确认病原菌。
1.4 病原菌的鉴定 1.4.1 形态学观察: 将4 ℃斜面保存的菌株转接至PDA平板活化5 d后,用灭菌的5 mm直径打孔器从菌落边缘打取PDA菌块,接入PDA平板中央。每株菌株5个重复,于25 ℃、12 h黑光灯照射/12 h黑暗交替培养[5],第7天时记录菌落特征和孢子等显微特征。菌丝体附着胞的诱导参照Sutton的方法[5],采用马铃薯胡萝卜琼脂培养基载片培养法;分生孢子附着胞诱导参照Yang等的方法[6]。
1.4.2 分子系统学分析: 将供试菌株分别接种于PDA平板上,7 d时收集菌丝,采用改良的CTAB法提取基因组DNA[7]。扩增的目的基因分别为核糖体转录间隔区序列 (internal transcribed spaces,ITS)、肌动蛋白基因 (Actin gene,ACT)、几丁质合成酶A基因 (chitin synthase A gene,CHS-1)、3-磷酸甘油醛脱氢酶基因 (glyceraldehydes-3-phosphate dehydrogenase gene,GAPDH)、钙调蛋白基因 (Calmodulin gene,CAL) 和β-微管蛋白基因 (β-tubulin gene,TUB2)。相应的PCR扩增引物、反应体系及条件参照Yang等的方法进行[6]。目的基因测序由成都栢晖生物科技有限公司完成。采用ClustalX 2.0.10[8]对自测的各个基因序列以及在GenBank比对并参考相偶联的文献后下载相关的序列 (表 1) 进行比对[6, 9-12],比对后利用Bioedit 5.0.6软件手工校正,以达到排序匹配的最优化。校正后的各个基因分别首尾相连,采用Paup 4.0 beta 10软件以最大简约法 (Maximum parsimony,MP) 进行分析,以启发式搜索法 (Heuristic search) 获取多基因系统发育树。其中,启发式搜索采用二等分再连接法 (Tree-bisection-reconnection,TBR) 作为获取聚类树的方法。系统发育树的各个分支的支持强度通过1 000次重复的自展检验数值进行评估。
| 种 Species |
菌株 Strain No. |
寄主 Host |
国家 Country |
基因登录号 GenBank accession number |
|||||
| ITS | GAPDH | CAL | ACT | CHS-1 | TUB2 | ||||
| C. annellatum | CBS 129826 | Hevea indica, leaf | Colombia | JQ005222 | JQ005309 | JQ005743 | JQ005570 | JQ005396 | JQ005656 |
| C. camelliae | LF 367 | Camellia sinensis | China | KJ955144 | KJ954845 | KJ954697 | KJ954423 | - | KJ955292 |
| LF 577 | Camellia sinensis | China | KJ955168 | KJ954869 | KJ954720 | KJ954442 | - | KJ955315 | |
| C. cliviae | CBS 125375a | Clivia miniata | China | GQ485607 | GQ856756 | GQ849464 | GQ856777 | GQ856722 | GQ849440 |
| C. gloeosporioides | IMI 18695 | Citrus sp. | USA | JX010153 | JX009979 | JX009735 | JX009494 | JX009779 | - |
| IMI 356878b | Citrus sinensis | Italy | JX010152 | JX010056 | JX009731 | JX009531 | - | JX010445 | |
| C.jiangxiense | LF 488 | Camellia sinensis | China | KJ955149 | KJ954850 | KJ954701 | KJ954427 | - | - |
| LF 687b | Camellia sinensis | China | KJ955201 | KJ954902 | KJ954752 | KJ954471 | - | KJ955348 | |
| LPSU 20120251c | Saxifraga stolonifera | China | KX009037 | KX009035 | KX009040 | KX009031 | KX009033 | KX009039 | |
| C. karstii | CGMCC 3.14194b | Vanda sp. | China | HM585409 | HM585391 | HM582013 | HM581995 | HM582023 | HM585428 |
| CBS 125468 | Coffea sp. | Vietman | JQ005197 | JQ005284 | JQ005718 | JQ005545 | JQ005371 | JQ005631 | |
| LPSU 20120244c | Saxifraga stolonifera | China | KX009036 | KX009034 | - | KX009030 | KX009032 | KX009038 | |
| C. nupharicola | CBS 469.96 | Nuphar lutea subsp. polysepala | USA | JX010189 | JX009936 | JX009661 | JX009486 | JX009834 | JX010397 |
| CBS 470.96b | Nuphar lutea subsp. polysepala | USA | JX010187 | JX009972 | JX009663 | JX009437 | JX009835 | JX010398 | |
| C. novae-zelandiae | CBS 128505b | Capsicum annuum | New Zealand | JQ005228 | JQ005315 | JQ005749 | JQ005576 | JQ005402 | JQ005662 |
| CBS 130240 | Citrus sp. | New Zealand | JQ005229 | JQ005316 | JQ005750 | JQ005577 | JQ005403 | JQ005663 | |
| C. petchii | CBS 387.94b | Dracaena marginata | Italy | JQ005223 | JQ005310 | JQ005744 | JQ005571 | JQ005397 | JQ005657 |
| CBS 118774 | Dracaena sanderana | China | JQ005225 | JQ005312 | JQ005746 | JQ005573 | JQ005399 | JQ005659 | |
| C. phyllanthi | CBS 175.67 | Phyllanthus acidus | India | JQ005221 | JQ005308 | JQ005742 | JQ005569 | JQ005395 | JQ005655 |
| C. salsolae | ICMP 19051b | Salsola tragus | Hungary | JX010242 | JX009916 | JX009696 | JX009562 | JX009863 | JX009863 |
| ICMP 18693 | Glycine max | Hungary | JX010241 | JX009917 | JX009695 | JX009559 | JX009791 | - | |
| C. theobromicola | CBS 124945b | Theobroma cacao | Panama | JX010294 | JX010006 | JX009591 | JX009444 | JX009869 | JX010447 |
| IMI 348152 | Fragaria vesca | USA | JX010288 | JX010003 | JX009589 | JX009448 | JX009819 | JX010379 | |
| C. tropicale | ICMP 18651 | Annona muricata | Panama | JX010277 | JX010014 | JX009720 | JX009570 | JX009868 | - |
| ICMP 18653b | Theobroma cacao | Panama | JX010264 | JX010007 | JX009719 | JX009489 | JX009870 | - | |
| 注:a:作为外类群;b:模式菌株或诠释模式菌株;c:本研究分离的菌株;粗体显示的序列号为本研究所测的序列. Note:a: outgroup; b: Ex-type or ex-epitype; c: Isolated in this study; sequenced in this study show in bold. | |||||||||
在叶上引起的病斑多为圆形或近圆形,初期水渍状棕褐色,零星分布在叶片上,后期病斑逐渐扩大,病斑变为深褐色至黑色 (图 1A)。通过组织块分离法分离到2株菌株 (LPSU 20120244和LPSU 20120251),菌株保存于六盘水师范学院,各菌株的DNA序列GenBank登录号为KX009030-KX009040 (表 1)。

|
| 图 1 虎耳草炭疽病病症及病原菌喀斯特炭疽菌形态特征 (菌株号:LPSU 20120244) Figure 1 Anthracnose symptoms on Saxifraga stolonifera and morphology of the Colletotrichum karstii (strain: LPSU 20120244) 注:A:自然条件下感染产生的病斑;B:致病性测试回接感染21 d形成的病斑 (箭头所示);C:病原菌喀斯特炭疽菌产孢细胞;D:分生孢子;E:分生孢子附着胞 (芽管如箭头所示);F、G:菌丝体附着胞.标尺为10 μm. Note: A: Symptom on leaf in the wild; B: Symptom of pathogenicity test on leaf in vivo after 21 d (indicated by an arrow); C: Conidiogenous cells; D: Conidia; E: Conidial appressoria (germ tube was indicated by an arrow); F-G: Mycelial appressoria. Bars=10 μm. |
|
|
对照及无刺伤接种未能感染虎耳草叶片形成病斑,刺伤接种8-10 d时开始形成病斑。病斑呈圆形或椭圆形,与自然发病病斑相似,褐色至浅黑色 (图 1B)。再分离培养物菌落、显微特征均与接种菌株相同。根据柯赫氏法则,分离菌株为虎耳草炭疽病病原菌。
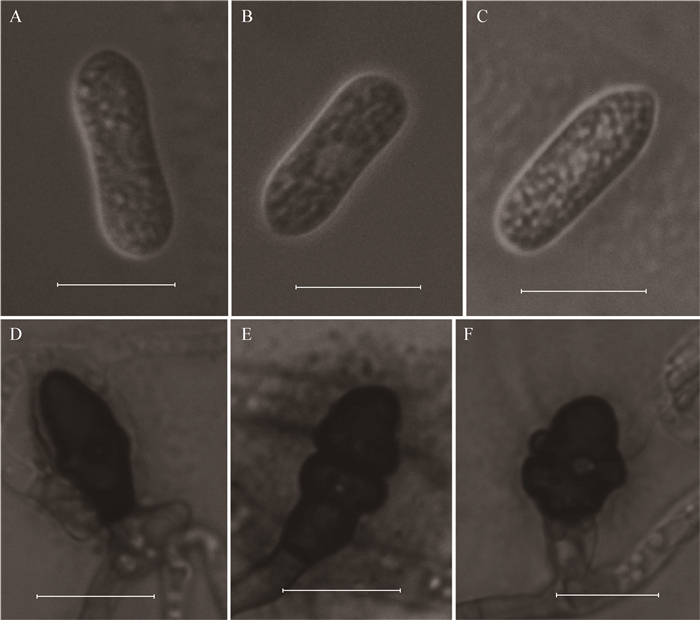
2.3 虎耳草炭疽病病原菌鉴定 2.3.1 病原菌形态学特征: 菌株LPSU 20120244在PDA上,生长速度4.3-5.0 mm/d,x±s=4.5±0.1 mm/d,气生菌丝致密,绒毛状,扁平,深灰色至黑色,边缘白色,分生孢子堆黄色;背面中央黑色,边缘白色。分生孢子梗多分枝,无色或稍浅棕色;产孢细胞圆柱状或长安培瓶状,无色,(9.5-23.5) µm×(3.5-6.0) µm (图 1C)。分生孢子无色,单孢,直,圆柱状,顶端钝圆,基部平截,(11-25) µm×(5-9) µm,x±s=(16.1±1.6) µm×(7.0±0.5) µm (图 1D)。分生孢子附着胞褐色,球形,边缘完整,(4-9) µm×(4-8) µm,x±s=(7.0±0.9) µm×(6.0±0.6) µm (图 1E);菌丝体附着胞浅棕色,舟状至棍棒状,边缘完整或波浪状,部分菌丝体附着胞从稍膨大的菌丝一侧形成,基部直接与菌丝相连,(6.5-14.0) µm×(5.0-7.0) µm,x±s=(8.5±1.9) µm×(5.8±0.5) µm (图 1F-G)。菌株LPSU 20120251在PDA上,生长速度4.7-6.1 mm/d,x±s=5.5±0.1 mm/d,气生菌丝发达,致密,扁平,中央浅灰色,边缘白色,完整,未见分生孢子堆形成;背面中央褐色,边缘白色到橄榄色。分生孢子单孢,直,圆柱状,两端钝圆或一端钝圆一端平截,无色,(15-25) µm× (5-7) µm,x±s=(16.0±1.6) µm×(6.0±0.6) µm (图 2 A-E)。菌丝体附着胞棍棒状,边缘粗锯齿状,偶有深裂,褐色到深褐色,(4-7) µm×(8-15) µm,x±s=(12.3±1.7) µm×(7.6±2.6) µm (图 2D-F)。
|
| 图 2 江西炭疽菌形态特征 (菌株号:LPSU 20120251) Figure 2 Morphology of the Colletotrichum jiangxiense (strain: LPSU 20120251) 注:A-C:分生孢子;D-F:菌丝体附着胞.标尺为10 μm. Note: A-C: Conidia; D-F: mycelial appressoria. Bars=10 μm. |
|
|

|
| 图 3 基于ACT、CAL、CHS-1、TUB2、ITS和GAPDH基因序列构建的多基因MP分子系统树 Figure 3 Maximum parsimony phylograms inferred from combined partial ACT, CAL, CHS-1, TUB2, ITS, and GAPDH sequences data 注:分支上的数值为1 000次重复后高于50%以上的Bootstrap值;君子兰炭疽菌 (菌株号CBS 125375) 为外类群;菌株号粗体显示的为本研究分离的菌株;▲:模式菌株或诠释模式菌株;比例尺代表该长度有10个碱基变化. Note: Values above the branches are parsimony bootstrap (equal or above 50%); The tree is rooted with Colletotrichum cliviae (CBS 125375); Isolated in this study show in bold; ▲: ex-type or ex-epitype; The scale bar defines 10 substitutions nucleotide positions. |
|
|
通过与已知种形态比较[9-10, 12]及多基因分子系统学分析,2株分离菌株分别代表了喀斯特炭疽菌 (菌株号LPSU 20120244) 和江西炭疽菌 (菌株号LPSU 20120251)。
3 讨论据报道引起虎耳草叶部病害的真菌有葡萄孢属灰葡萄孢菌 (Botrytis cinerea Pers.)、尾孢属某一种 (Cercospora sp.)、小帚梗孢属山茶小帚梗孢[Cylindrocladiella camelliae (Venkataram. & C.S.V. Ram) Boesew.]、普生白粉菌[Erysiphe communis (Wallr.) Schltdl.]、假粉孢属某一种 (Pseudoidium sp.) 和立枯丝核菌 (Rhizoctonia solani J.G. Kühn) 6种真菌[13]。其中仅灰葡萄孢菌在中国发现引起虎耳草病害,喀斯特炭疽菌和江西炭疽菌为首次发现引起虎耳草病害。
喀斯特炭疽菌为全球性分布、寄主广泛的炭疽菌属病原真菌,可引起山茶属、万代兰属等多种植物炭疽病[9-10, 12, 14-15],同时也是植物内生真菌[15]。分离自虎耳草的喀斯特炭疽菌菌落颜色与分离自其他寄主的该种真菌存在一定差异。分离自其他寄主的该病原菌菌落颜色较浅,多为白色至浅灰色,自虎耳草分离的菌株菌落深灰色至黑色,但分生孢子及附着胞等显微特征与模式菌株的大小及形态与其他寄主分离的菌株相同;此外,在菌丝体附着胞形成部位而言,一般仅从菌丝顶端形成,本研究观察到部分菌丝从一侧形成,附着胞基部直接与稍膨大的菌丝侧面相连 (图 1F)。多基因分子系统学分析表明与喀斯特炭疽菌模式菌株形成同一进化支,支内支长差异极小。江西炭疽菌为炭疽菌属近年发现的新分类单元,主要在茶叶上引起炭疽病,同时也作为内生真菌从茶叶上分离出[12]。分离自虎耳草的江西炭疽菌菌株分生孢子形态、大小及菌落与分离自茶的菌株极为相似,大小重叠。在基于多基因构建的系统树中与模式菌株 (LF 687) 的支长相同,但与非模式菌株 (LF 488) 存在一定差异。
炭疽病为一类危害严重的植物病害,常导致局部暴发,甚至大面积流行,造成严重经济损失[16-17]。对本研究发现的虎耳草炭疽病病原菌,建议加强其生物学特性及药效筛选等研究,以进一步为该病的防治奠定坚实的基础。
致谢: 六盘水师范学院生物科学专业2009级学生代方君、2010级王腾荣参与了部分实验,特此感谢。| [1] | Xian C, Gong XJ, Zhao C, et al. Chemical constituents of Saxifraga stolonifera[J]. Chinese Journal of Experimental Traditional Medical Formulae, 2012, 18(10) : 124–126. (in Chinese) 先春, 龚小见, 赵超, 等. 虎耳草的化学成分研究[J]. 中国实验方剂学杂志, 2012, 18(10) : 124–126. DOI:10.3969/j.issn.1005-9903.2012.10.035 |
| [2] | Ju LT. Treatment of prostatic hyperplasia using Saxifraga stolonifera preparation[J]. Chinese Journal of Basic Medicine in Traditional Chinese Medicine, 2007, 13(1) : 79. (in Chinese) 居龙涛. 虎耳草制剂治疗前列腺增生症[J]. 中国中医基础医学杂志, 2007, 13(1) : 79. |
| [3] | Pu X, Song LK. Research advance on Saxifraga stolonifera[J]. Journal of Anhui Agricultural Sciences, 2009, 37(31) : 15224–15226. (in Chinese) 蒲祥, 宋良科. 虎耳草的研究进展[J]. 安徽农业科学杂志, 2009, 37(31) : 15224–15226. |
| [4] | Fang ZD. Plant Pathology Research Methods[M].3rd Edition. Beijing: China Agriculture Press, 1998 . (in Chinese) 方中达. 植病研究方法[M].第3版. 北京: 中国农业出版社, 1998 . |
| [5] | Sutton BC. The Coelomycetes: Fungi imperfecti with pycnidia acervuli and stromata[M]. Kew, UK: Commonwealth Mycological Institute, 1980 . |
| [6] | Yang YL, Liu ZY, Cai L, et al. Colletotrichum anthracnose of Amaryllidaceae[J]. Fungal Diversity, 2009, 39(2) : 123–146. |
| [7] | Chen J, Xu LL, Liu B, et al. Taxonomy of Dactylella complex and Vermispora. I. generic concepts based on morphology and ITS sequences data[J]. Fungal Diversity, 2007, 26(1) : 73–83. |
| [8] | Larkin MA, Blackshields G, Brown NP, et al. ClustalW and ClustalX. version 2.0[J]. Bioinformatics, 2007, 23(21) : 2947–2948. DOI:10.1093/bioinformatics/btm404 |
| [9] | Yang YL, Cai L, Yu ZN, et al. Colletotrichum species on Orchidaceae in southwest China[J]. Cryptogamie, Mycologie, 2011, 32(3) : 229–253. DOI:10.7872/crym.v32.iss3.2011.229 |
| [10] | Damm U, Cannon PF, Woudenberg JHC, et al. The Colletotrichum boninense species complex[J]. Studies in Mycology, 2012, 73 : 1–36. DOI:10.3114/sim0002 |
| [11] | Weir BS, Johnston PR, Damm U. The Colletotrichum gloeosporioides species complex[J]. Studies in Mycology, 2012, 73 : 115–180. DOI:10.3114/sim0011 |
| [12] | Liu F, Weir BS, Damm U, et al. Unravelling Colletotrichum species associated with Camellia: employing ApMat and GS loci to resolve species in the C. gloeosporioides complex[J]. Persoonia, 2015, 35(1) : 62–86. |
| [13] | Farr DF, Rossman AY. Fungal databases, systematic mycology and microbiology laboratory, ARS, USDA[EB/OL]. [2016-03-22]. http://nt.ars-grin.gov/fungaldatabases/ |
| [14] | Wang J, Ai CX, Yu XM, et al. First report of Colletotrichum karstii causing anthracnose on persimmon leaves in China[J]. Plant Disease, 2016, 100(2) : 532. |
| [15] | Velho AC, Alaniz S, Casanova L, et al. New insights into the characterization of Colletotrichum species associated with apple diseases in southern Brazil and Uruguay[J]. Fungal Biology, 2015, 119(4) : 229–244. DOI:10.1016/j.funbio.2014.12.009 |
| [16] | Wu LQ, Zhu LW, Heng W, et al. Identification of Dangshan pear anthracnose pathogen and screening fungicides against it[J]. Scientia Agricultura Sinica, 2010, 43(18) : 3750–3758. (in Chinese) 吴良庆, 朱立武, 衡伟, 等. 砀山梨炭疽病病原鉴定及其抑菌药剂筛选[J]. 中国农业科学, 2010, 43(18) : 3750–3758. DOI:10.3864/j.issn.0578-1752.2010.18.008 |
| [17] | Hyde KD, Cai L, Cannon PF, et al. Colletotrichum-names in current use[J]. Fungal Diversity, 2009, 39(2) : 147–183. |
 2017, Vol. 44
2017, Vol. 44