扩展功能
文章信息
- 商君阳, 周霜艳, 王中华, 李正斌, 谢宁栋, 马文猛, 张永丰, 张建乐, 汪光义
- Shang Jun-yang, Zhou Shuang-yan, Wang Zhong-hua, Li Zheng-bin, Xie Ning-dong, Ma Wen-meng, Zhang Yong-Feng, Zhang Jian-le, Wang Guang-yi
- 降雨对秦皇岛西浴场细菌总数和可培养菌群组成的影响
- Effects of rainfall on the total number of bacteria and the composition of culturable bacteria in Qinhuangdao West Beach
- 微生物学通报, 2016, 43(6): 1227-1234
- Microbiology China, 2016, 43(6): 1227-1234
- DOI: 10.13344/j.microbiol.china.150491
-
文章历史
- 收稿日期: 2015-06-28
- 接受日期: 2015-10-16
- 优先数字出版日期(www.cnki.net): 2016-01-22
2. 国家海洋局秦皇岛海洋环境监测中心站 河北 秦皇岛 066002
2. Qinhuangdao Marine Environmental Monitoring Central Station, SOA, Qinhuangdao, Hebei 066002, China
随着海洋开发力度的逐步加大,海洋旅游业得到了蓬勃发展,海水浴场旅游人数逐年增加,微生物污染问题成为了公众关心的主要方面之一[1]。目前,微生物是浴场环境评价的一个重要方面,其中病原微生物是其中一个重要的指标,根据世界卫生组织(World Health Organization,WHO)的研究报道浴场主要病原菌包括:大肠杆菌O157 (Escherichia coli O157)、沙门氏菌(Salmonella spp.)、钩端螺旋体(Leptospira spp.)、创伤弧菌(Vibrio vulnificus)、军团菌(Legionella spp.)、弯曲杆菌(Campylobacter sp.)、幽门螺杆菌(Helicobacter pylori)、志贺氏菌(Shigella spp.)、鸟分枝杆菌复合体(Mycobacterium avium complex),这些病原菌可以引起人的肠胃疾病、上呼吸道感染等[2-3]。对浴场微生物群落结构及其组成的研究,可以科学地反映浴场的细菌现状,更好地了解浴场环境,从微生物角度对浴场健康环境进行科学的评价。
细菌与环境之间在一定的条件下是相互依存、相互制约的。当环境因子改变时,细菌总数和种类也会随之发生变化,进而引起海洋水质的变化[4]。浴场是人为因素影响极大的小型生态系统,其中的各种理化因子、生物因子关系十分复杂,且处于不断波动变化中。由于海水浴场一般靠近城市,随着城市污水的排放,一些病原微生物也随之流入海洋[5],陆源污染是浴场病原菌的重要来源之一;此外河流、游客以及天气情况等都会对其种类和分布产生影响[6]。李铭巾等在对大连市棒棰岛海水浴场夏季水质状况进行分析及建议中提到:降雨时期海水明显浑浊,各项水质指标恶化[7];潘静芬在对舟山朱家尖海水浴场夏季水质状况进行分析与评价时提到:天气因素是导致粪大肠菌群增高的原因之一,降雨过程中雨水的冲刷使得陆源污染直接进入海域的机率大大增加[8]。然而,降雨对浴场的影响的相关研究报道侧重点一般都在水质方面,关于细菌群落分布的研究却较少。胡晓娟等研究了降雨对水产养殖群落分布的影响[9];Teira、Bolhuis等研究了降雨对海湾微生物群落分布的影响[10-11],这些研究结果表明不同海域的降水对微生物种群的分布及数量的影响存在差异。
目前,海水浴场病原菌的检测方面研究常见的方法有:发酵法、滤膜法、平板涂布法、免疫法、PCR法以及近年来兴起的高通量法等,每种方法都各有利弊[6],随着检测手段的发展,目前已初步实现采用定量PCR方法对肠球菌的测定[12]。由于海水浴场微生物群落结构复杂,检测标准也有所不同,粪大肠菌群(fecal coliforms)和肠球菌(Enterococcus)为澳大利亚所确定的海水浴场的指示菌[13],美国环保部(US Environmental Protection Agency,USEPA)所确定的标准微生物指标为肠球菌[14],欧盟(European Union,EU)将大肠杆菌(Escherichia coli)和肠球菌作为检测的标准[15],这方面我国的指标为粪大肠菌群[16]。
细菌总数可以反映环境中异样细菌的污染程度以及有机污染程度[17],平板计数法可以显示水样中可培养细菌总数的情况,但不能真实地反映细菌总数情况,荧光显微镜计数法可以直接对环境样品进行染色和观察分析,能够更加精确地反映环境中细菌总数情况[18],然而该方法无法分辨出可培养细菌的数量。两种方法结合,既可以对可培养细菌总数进行分析,又可以对细菌总数进行计数统计,能够更直接、更全面地反映浴场的微生物情况。
本研究采用改良的荧光显微镜计数法对降雨前后秦皇岛西浴场站位的细菌总数进行计数统计,采用平板培养法对可培养菌群进行研究,分析了降雨对细菌总数以及可培养菌群的影响,发现降水前后的可培养菌群中,作为优势菌的变形菌门(Proteobacteria)数目降水后有所下降(雨前占80%,雨后占73%),而拟杆菌门(Bacteroides)和厚壁菌门(Firmicutes)的数目降水后有所增加(拟杆菌门雨前占12%,雨后占13%;厚壁菌门雨前占7%,雨后占11%)。我们希望这一研究成果能够为浴场水质监控和环境管理提供依据。
1 材料与方法 1.1 主要试剂和仪器SYBR Gold荧光染料,英潍捷基(上海)贸易有限公司;Taq DNA聚合酶、DNA胶回收试剂盒,天根生化科技(北京)有限公司;化学试剂购于国药集团化学试剂有限公司;引物合成与测序华大基因科技有限公司。
研究级正置荧光显微镜,尼康Nikon ECLIPSE Ni;S1000 Thermal Cycler PCR仪,Bio-Rad。
1.2 样品的采集2014年8月份雨前和雨后分别用无菌玻璃瓶采集秦皇岛西浴场3个不同区域水体表面以下水样1 L,分别命名为S1、S2、S3,每个站位之间相距200 m,每个站位与岸边均相距10 m,3个站位平行于海岸呈直线排布。每站位取3个平行样,取样后立即用无菌无颗粒甲醛现场固定,其中雨后取样时间为降雨后1 h内。此外各站点另取新鲜未固定海水1 L,4 °C保温箱运到实验室,做可培养细菌计数分析。3个站位中S1位于排污口附近约5 m。
1.3 细菌总数的统计细菌总数采用改进的荧光显微镜直接计数法[19-20]:取1 mL固定后的海水样品,真空抽滤到黑色微孔滤膜(Nuclepore filter,0.22 μm,25 mm diameter)上,加入SYBR Gold染色液避光染色15 min取下滤膜置于干净载玻片上,有菌一面向上,加入荧光保护剂。荧光显微镜蓝色激发光、油镜条件下对亮绿色的细菌进行观察,随机均匀选取16个视野对被染色的细菌个体进行计数统计。细菌丰度计算公式[21-22]为:细菌丰度=A×S1/(S2×V)。
1.4 浴场可培养细菌优势菌群的研究无菌水将水样稀释5个梯度(10-1-10-5),每个梯度3个平行,涂布于培养基(g/L,牛肉膏3,蛋白胨5,KCl 0.7,CaCl2·6H2O 1.5,MgSO4·7H2O 5.4,MgCl2·6H2O 10.8,NaCl 30)平板,28 °C连续培养1-2 d,对细菌总数进行计数分析,同时,在3个平行培养基平板中挑取数量和生长状况较好的1个培养基平板挑单菌落进行分子生物学鉴定。16S rRNA基因扩增引物采用常规引物27F (5′-AGAGTTTGATCCTGGCTCAG-3′)和1492R(5′-GGTTACCTTGTTACGACTT-3′)[23]。PCR扩增[23]后测序,结果输入NCBI数据库进行比对。
采用R (gplots) (v 2.14.2,http://www.r-project.org/)软件对所有结果进行多样性(Shannon-Wiener index,Simpson’s diversity index and Evenness index)统计。
2 结果与分析 2.1 细菌总数统计结果雨前,排污口处于干涸状态;雨后,排污口中有污水排水,水体发黑,无异味。分别采用荧光显微镜和平板对降雨前后的细菌总数、可培养细菌总数结果进行计数统计,从统计结果(表 1)可以看出,降雨后不同站位细菌总数不同,降雨前3个站位细菌总数差别不显著,最高的为S2,为7.7×109 CFU/L;对于可培养细菌而言,各站位也不存在显著的差异,最高为S3,可培养细菌总数为8.6×107 CFU/L。降雨后各站位细菌总数和可培养细菌数均有明显的增加,其中S1站位细菌总数增加约2倍,可培养细菌数增加约5倍;对于站位S2而言,雨后细菌总数增加了10%,可培养细菌数增加了约2倍;对于站位S3而言,也具有相同的变化趋势,细菌总数在雨后约为雨前的2倍多,可培养细菌数约增加了12%。细菌总数和可培养细菌数雨后均有所增加。
| 样品 Sample | 雨前 Before rainfall (CFU/L) | 雨后 After rainfall (CFU/L) | ||||||
| 平行样Duplicate sample | 细菌总数平均值 Total bacteria | 平行样Duplicate sample | 可培养菌总数平均值 Culturable bacteria | 平行样Duplicate sample | 细菌总数平均值 Total bacteria | 平行样Duplicate sample | 可培养菌总数平均值 Culturable bacteria | |
| S1 | 4.8×109 5.3×109 4.9×109 | 5.0×109 | 8.1×107 8.6×107 8.8×107 | 8.5×107 | 9.5×109 9.4×109 10.2×109 | 9.7×109 | 4.6×108 3.7×108 3.4×108 | 3.9×108 |
| S2 | 7.8×109 7.5×109 7.8×109 | 7.7×109 | 7.9×107 7.8×107 7.7×107 | 7.8×107 | 9.7×109 8.0×109 7.8×109 | 8.5×109 | 1.3×108 1.7×108 1.5×108 | 1.5×108 |
| S3 | 4.8×109 3.9×109 3.6×109 | 4.1×109 | 8.5×107 8.9×107 8.4×107 | 8.6×107 | 9.7×109 9.1×109 9.4×109 | 9.4×109 | 9.2×107 9.3×107 10.3×107 | 9.6×107 |
| Average | 5.6×109 | 8.3×107 | 9.2×109 | 2.1×108 | ||||
在海洋细菌的计数分析方面,目前我国国家海洋监测规范所规定的细菌总数计数方法主要为平板计数和荧光显微镜直接计数法。两种方法各有利弊,对于平板计数法而言,它可以直接显示水样中可培养细菌总数的情况,而荧光显微镜计数法可以直接对环境样品进行染色和观察分析,能够更加精确地反映环境中异养细菌的数量。在对2004年8月份和10月份渤海湾细菌总数的研究[24]中发现,8月份和10月份的平均值分别为49.4×106 CFU/L和34.4×106 CFU/L,而在2005年对渤海湾不同站位的调查研究[20]发现,不同季节浮游细菌总数也有较大差异,夏季的海洋浮游细菌平均值为12.8×108 CFU/L,秋季为7.4×108 CFU/L。本研究中细菌总数和可培养细菌总数平均值分别为5.6×109 CFU/L和8.3×107 CFU/L,雨后分别为9.2×109 CFU/L和2.1×108 CFU/L,与之前结果相比均有所增加,细菌污染问题需引起重视。
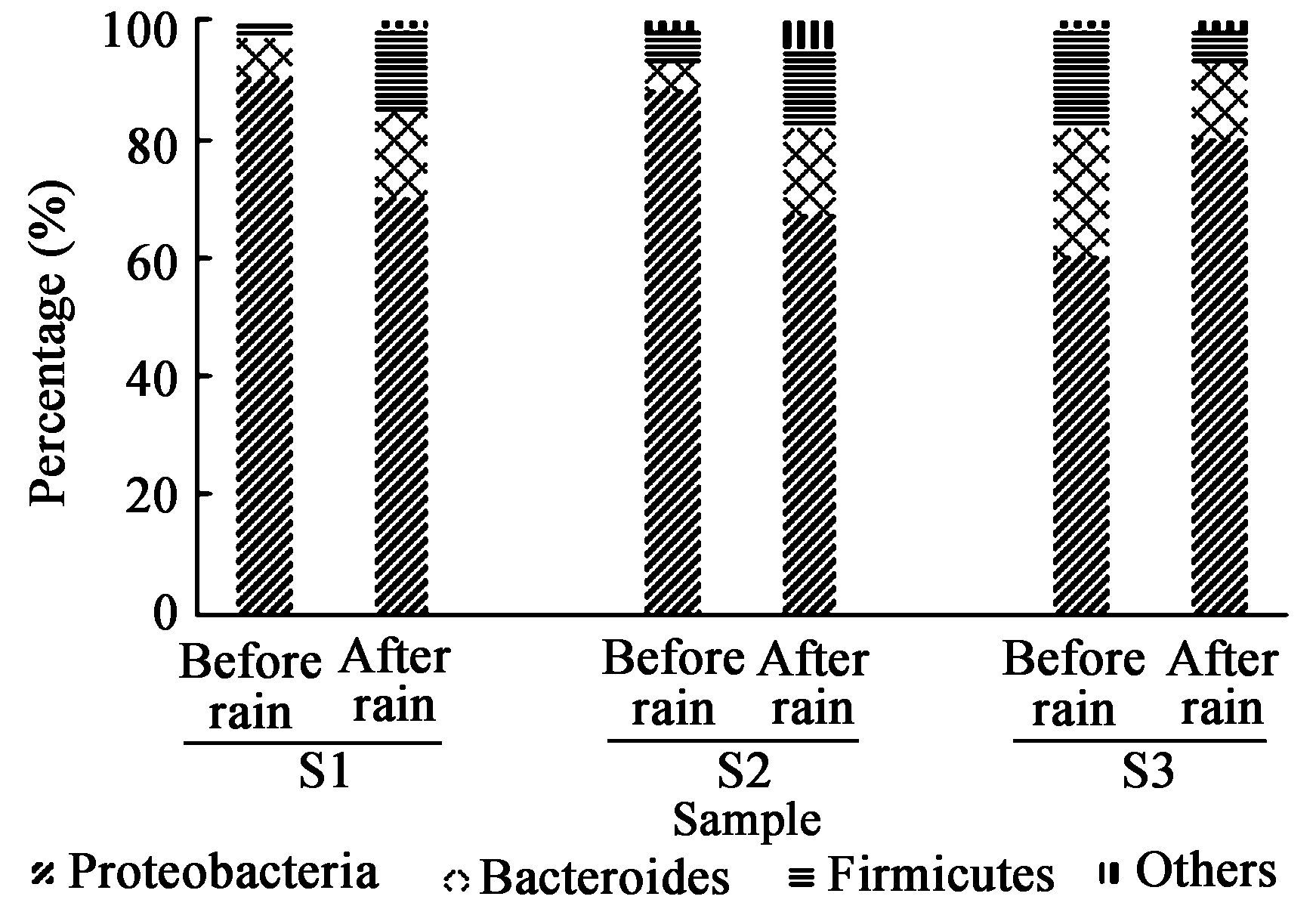
2.2 可培养细菌群落结构的变化为获得水样中微生物群落结构和组成,分析降雨对浴场水质的影响,将水样采用梯度稀释的方法涂平板后,根据菌落的颜色、大小、形状、表面是否光滑、边缘是否整齐等形态学特征对菌落进行了预先分类,挑取典型的200个菌落进行PCR扩增测序。结果表明(图 1):雨后细菌微生物群落结构更为复杂。变形菌门是3个站位的主要微生物类群,其中S1、S2降雨前所占比例较高,约占90%,S3约占60%;雨后S1、S2变形菌门的数量有所下降,约为70%,而S3有所增加,约占细菌总数的80%。对于厚壁菌门而言,站位S1雨后该类群微生物有明显的增加,与之相反的站位S3显著下降。对于拟杆菌门微生物类群而言,S1、S2两个站位雨后其数量均有明显的增加,站位S3其数量有所下降。此外在研究中还发现数量较少的、未鉴定出的微生物类群,以及所占百分比低于1%的微生物类群,将其命名为Others。
|
| 图 1 降雨前后浴场水样可培养细菌结构的变化 Figure 1 Change in bacterial community structure before and after rainfalls |
|
|
雨前3个站位的优势菌为弧菌属、肠杆菌属、海杆菌属、假单胞菌属和芽孢杆菌属。雨后,对于站位S1而言,优势菌为肠杆菌属、假单胞菌属和弓形菌属。通过16S rRNA基因序列分析得到了200个克隆子的测序结果,其在各个样品中的分布情况如表 2所示。从优势菌的分析可以看出,降雨对浴场微生物群落结构的组成产生了显著的影响。
| 样品名称 Sample name | 时间 Time | 名称 Name | 数量 Quantity |
| S1 | 雨前 | Bacillus Enterobacter Marinobacter | 10 8 5 |
| Arthrobacter Alphaproteobacteria Betaproeobacteria | 4 3 3 | ||
| 雨后 | Enterobacter Pseudomonas Bacillus | 11 9 7 | |
| Flavobacteria Spirochaetes Vibrio Gammaproteobacteria | 2 2 2 1 | ||
| S2 | 雨前 | Arcobacter Marinobacter Enterobacter | 13 8 5 |
| Synergistia Opitutae Clostridia | 3 2 2 | ||
| 雨后 | Enterobacter Marinobacter Bacillus | 11 9 7 | |
| Gemmatimonadetes Opitutae Synechococcophycideae Chloroplaet | 2 2 1 1 | ||
| S3 | 雨前 | Pseudomonas Enterobacter Vibrio | 10 8 6 |
| Fusobacteria Epsilonproteobacteria Oscillatoriophycideae | 4 3 2 | ||
| 雨后 | Marinobacter Acinetobacter Arcobacter | 12 11 5 | |
| Erysipelotrichi Sphingobacteria Deltaproteobacteria Opitutae | 2 2 1 1 |
PCR扩增测序后将相同的测序结果归为一个操作分类单元(operational taxonomic unit,OTU),通过R软件进行多样性分析,结果(表 3)表明与降雨之前相比雨后生物多样性指数较高,群落结构更为复杂。结果也进一步表明降雨对近岸海域的微生物群落结构及其组成会产生显著的影响。
| 样品名称 Sample name | 时间 Time | Shannon-Wiener | Simpson’s diversity | Evenness |
| S1 | 雨前 | 1.24 | 0.52 | 0.49 |
| 雨后 | 4.12 | 0.66 | 0.66 | |
| S2 | 雨前 | 2.21 | 0.77 | 0.64 |
| 雨后 | 4.06 | 0.83 | 0.79 | |
| S3 | 雨前 | 2.82 | 0.71 | 0.56 |
| 雨后 | 3.42 | 0.79 | 0.69 |
另外,对降雨前后可培养细菌的微生物群落结构及其组成的研究发现,降雨对于浴场微生物群落结构的组成会产生显著的影响。与其余浴场微生物的研究[25]不同,本研究中占绝大多数的微生物类群为变形菌门,雨后两个站位中其所占比例有了显著的增加,S3中其所占比例有所下降,此外后壁菌门、拟杆菌门所占比例也有明显的变化。在部分研究中发现厚壁菌门微生物占有较大的比例[25-27],而在本研究中该类群所占比例较少,这也进一步说明了环境对微生物类群的影响,不同的区域、不同的海域其微生物类群有很大的不同。
研究表明,浮霉菌门和拟杆菌门细菌在降解环境中的有机质方面具有重要作用,此外,拟杆菌门细菌也是赤潮藻类的共生细菌,与赤潮的发生有一定的联系[28]。在海岸带沉积物的检测中发现γ-变形细菌亚门细菌为优势类群[29-31],研究中检测到较多为肠杆菌目,该类群微生物是典型的异养厌氧型微生物。研究中发现了大肠埃希氏菌和志贺氏菌属均为致病菌,可引起肠胃疾病,在研究中发现其含量在所研究浴场水体中所占比例较低,其它所规定的浴场致病菌未检测到。红细菌目是α-变形细菌亚门中的主要微生物类群,广泛分布于海岸带区域,是赤潮发生后期构成微生物群落的主要菌群。在本研究取样中发现西浴场水体中存在大量浮游藻类,对于藻类与浴场微生物群落结构的关系有待进一步分析。研究还发现多条测序结果与数据库中不可培养的细菌具有高度相似性,这表明海岸带微生物存在大量的未知资源,有待进一步的研究。
3 讨论由于微生物新陈代谢速度较快,其群落结构和组成受到多种环境因素如温度、pH、COD、营养盐等因素的影响[32]。微生物群落结构及其组成与生态系统以及环境密切相关,一方面群落结构及其复杂程度决定了生态系统的特征和强弱,另一方面环境因素的改变也会引起微生物群落结构及其组成的变化[28, 33]。因此,通过研究不同环境条件下的微生物群落结构,对于揭示微生物与环境之间的关系、环境的综合评价分析具有重要的作用[34]。
降雨过程中,一方面雨水携带一些陆源微生物随城市雨水管道直接或间接流入浴场,另一方面部分地区由于浴场附近排泄系统能力的不足,生活污水溢出、甚至发生雨污混排现象,这些都可能会对浴场微生物群落造成影响。胡晓娟等在强降雨对粤西凡纳滨对虾养殖池塘微生物群落影响的研究中发现:未施用微生态制剂的虾池在强降雨后,水体的弧菌数升高,Simpson指数和McIntosh指数显著降低(P<0.05),水体和底泥微生物群落对碳源的利用率变化明显,水体及沉积物环境波动变化明显,强降雨对其水域环境产生很大的影响[9]。由于陆源污染对浴场和养殖区的影响能力不同,所以对比研究成果存在差异,但共同点是降雨会影响细菌群落结构。Teira等在研究降雨对近海富营养化海湾影响中发现,雨后细菌丰度会显著增加,而且变形菌门在雨前、雨后均为主要微生物类群,这与本文结果一致[10];不同的是,本文同时考虑了细菌总数的变化,另外研究了雨前后不同站位的优势菌属。
针对本研究发现,雨后数量增加的肠杆菌属广泛存在于污水中,它们侵入受外伤或缺血的皮下组织会导致患部皮肤组织水肿、缺血,常波及较深的肌肉层。根据中国环境监测总站检测结果,在降雨后部分浴场中粪大肠菌群的含量发生了明显的变化。然而对于整个微生物群落结构的变化情况,以及主要病原菌的变化情况并没有明确的调查结果,对该部分的研究就显得尤为重要。所以本文研究强降雨条件对浴场细菌总数以及细菌群落结构的影响是对区域浴场生态的一个重要补充,为区域浴场微生物检测提供数据支持。
4 结论(1) 雨后细菌总数、可培养细菌总数均有显著增加,微生物群落结构更为复杂,其构成发生了明显改变,降雨影响了浴场微生物群落结构组成。建议相关部门对恶劣天气采取有效措施。
(2) 浴场主要的微生物类群为变形菌门、厚壁菌门和拟杆菌门;芽孢杆菌属、肠杆菌属、海杆菌属、弓形菌属、假单胞菌属为雨前可培养细菌优势属,而雨后可培养细菌优势属为肠杆菌属、假单胞菌属、弧菌属、弓形菌属、不动杆菌属、海杆菌属等。
(3) 通过16S rRNA 基因分析方法研究了浴场微生物组成,发现个别致病菌虽然其数量相对较低,但仍需引起重视,可进一步采取qPCR技术对其含量进行研究证明。
| [1] | Efstratiou MA. Managing coastal bathing water quality: the contribution of microbiology and epidemiology[J]. Marine Pollution Bulletin, 2001, 42 (6): 425–432. |
| [2] | Kathy P. Water Recreation and Disease. Plausibility of Associated Infections: Acute Effects, Sequelae andMortality[M]. London: IWA Publishing, 2005: 59 . |
| [3] | Abouzaid H, Almodovar L, Andelman J, et al. Guidelines for safe recreational water environments: Volume 1: Coastal and fresh waters[R]. Geneva, Switzerland: The World Health Organization, 2003 |
| [4] | Xiao H. Studies on bacteriology of costal waters in Bohai bay and the application of bacteria on assessment of quality of coastal environment[D]. Qingdao: Doctoral Dissertation of Ocean University of China, 2005 (in Chinese) 肖慧. 渤海湾近岸海域的细菌学研究及其在海岸带环境质量评价中的应用[D]. 青岛: 中国海洋大学博士学位论文, 2005 |
| [5] | Prieto MD, Lopez B, Juanes JA, et al. Recreation in coastal waters: health risks associated with bathing in sea water[J]. Journal of Epidemiology & Community Health, 2001, 55 (6): 442–447. |
| [6] | Mu GQ, Li JY, Fan JF. Research progress on microbial indicators and hygienical water quality assessment in marine beach[J]. Marine Environment Science, 2012, 31 (6): 939–944. (in chinese) 穆贵强, 李江宇, 樊景凤. 海水浴场微生物指标与卫生学水质评价研究进展[J]. 海洋环境科学, 2012, 31 (6):939–944. |
| [7] | Li MJ, Li ZM. Analysis and suggestion of the Bangchuidao bathing beach water quality of Dalian in summer[J]. Environment and Sustainable Development, 2014, 39 (6): 181–183. (in chinese) 李铭巾, 李哲民. 大连市棒棰岛海水浴场夏季水质状况分析及建议[J]. 环境与可持续发展, 2014, 39 (6):181–183. |
| [8] | Pan JF. Monitoring and assessment of Zhoushan Zhujiajian bathing beach in summer[J]. Journal of Zhejiang Ocean University (Natural Science), 2012, 31 (4): 365–370. (in chinese) 潘静芬. 舟山朱家尖海水浴场夏季水质状况分析与评价[J]. 浙江海洋学院学报: 自然科学版, 2012, 31 (4):365–370. |
| [9] | Hu XJ, Li ZJ, Cao YC, et al. Influence of heavy rain on microbial community in Litopenaeus vannamei culture ponds in western Guangdong Province[J]. Journal of Fishery Sciences of China, 2010, 17 (5): 987–995. (in chinese) 胡晓娟, 李卓佳, 曹煜成, 等. 强降雨对粤西凡纳滨对虾养殖池塘微生物群落的影响[J]. 中国水产科学, 2010, 17 (5):987–995. |
| [10] | Teira E, Hernando-Morales V, Martínez-García S, et al. Response of bacterial community structure and function to experimental rainwater additions in a coastal eutrophic embayment[J]. Estuarine, Coastal & Shelf Science, 2013, 119 : 44–53. |
| [11] | Bolhuis H, Fillinger L, Stal LJ. Coastal microbial mat diversity along a natural salinity gradient[J]. PLoS One, 2013, 8 (5): e63166. |
| [12] | Wade TJ, Calderon RL, Sams E, et al. Rapidly measured indicators of recreational water quality are predictive of swimming-associated gastrointestinal illness[J]. Environmental Health Perspectives, 2006, 114 (1): 24–28. |
| [13] | National Health and Medical Research Council. Australian guidelines for recreational use of water[R]. Canberra: Australian Government Publishing Service, 1990 |
| [14] | Bartram J, Rees G. Monitoring bathing waters: a practical guide to the design and implementation of assessments and monitoring programmes[R]. New York: E & FN SPON, 2000 |
| [15] | Wang ZW, Li ZM. Comparison of microbial items for drinking water quality standards between China and some other countries[J]. The Administration and Technique of Environmental Monitoring, 2012, 24 (1): 70–74. (in chinese) 王中卫, 李哲民. 中外饮用水水质标准的微生物指标比较[J]. 环境监测管理与技术, 2012, 24 (1):70–74. |
| [16] | The ministry of environmental protection. HJ438-2008 People’s Republic of China National Environmental Standards[S] (in Chinese) 环境保护部. HJ438-2008中华人民共和国国家环境保护标准[S] |
| [17] | Li HY, Chen MX, Li G, et al. Occurrence of total and culturable bacteria in Shenzhen coastal waters and their application in the environment assessment[J]. Marine Environment Science, 2011, 30 (4): 487–491. (in chinese) 李和阳, 陈明霞, 李刚, 等. 深圳海域细菌总数及可培养细菌总数的分布及其在环境评价中的应用研究[J]. 海洋环境科学, 2011, 30 (4):487–491. |
| [18] | GB 17378.1-1998, The specification for marine monitoring[S]. Beijing: China Standard Publishing House, 1998 (in Chinese) GB 17378.1-1998, 海洋监测规范[S]. 北京: 中国标准出版社, 1998 |
| [19] | State Oceanic Administration. Technical Specification of Marine Biological and Ecological Investigations[M]. Beijing: Ocean Press, 2006 . (in chinese) 国家海洋局. 海洋生物生态调查技术规程[M]. 北京: 海洋出版社, 2006 . |
| [20] | Zhao HP, Li QX, Tao JH. Methods of fluorescence enumeration of marine bacteria and application[J]. Journal of Hebei University of Engineering (Natural Science Edition), 2007, 24 (1): 57–60. (in chinese) 赵海萍, 李清雪, 陶建华. 海洋细菌荧光显微计数法及其应用[J]. 河北工程大学学报: 自然科学版, 2007, 24 (1):57–60. |
| [21] | Zheng TL, Wang F, Xu MZ, et al. Bacterial production biomass and role in microbial loop in Taiwan Strait[J]. Oceanologia et Limnologia Sinica, 2002, 33 (4): 415–423. (in chinese) 郑天凌, 王斐, 徐美珠, 等. 台湾海峡海域细菌产量、生物量及其在微食物环中的作用[J]. 海洋与湖沼, 2002, 33 (4):415–423. |
| [22] | Zhou WH, Wang HK, Dong JD, et al. Phytoplankton and bacterial biomass and their relationship with the environmental factors in autumn and winter in the Sanya Bay, China[J]. Acta Ecologica Sinica, 2006, 26 (8): 2634–2639. (in chinese) 周伟华, 王汉奎, 董俊德, 等. 三亚湾秋、冬季浮游植物和细菌的生物量分布特征及其与环境因子的关系[J]. 生态学报, 2006, 26 (8):2634–2639. |
| [23] | Suzuki MT, Giovannoni SJ. Bias caused by template annealing in the amplification of mixtures of 16S rRNA genes by PCR[J]. Applied and Environmental Microbiology, 1996, 62 (2): 625–630. |
| [24] | Li QX, Zhao HP, Tao JH. Ecological research of heterotrophic bacterioplankton in the Bohai Bay waters[J]. Ocean Technology, 2005, 24 (4): 50–53. (in chinese) 李清雪, 赵海萍, 陶建华. 渤海湾海域浮游细菌的生态研究[J]. 海洋技术, 2005, 24 (4):50–53. |
| [25] | Li JY, Fan JF, Mu GQ, et al. Analysis of bacterial community diversity of marine bathing beach water by PCR-DGGE[J]. Marine Environment Science, 2013, 32 (4): 523–528. (in chinese) 李江宇, 樊景凤, 穆贵强, 等. 利用PCR-DGGE分析海水浴场细菌多样性[J]. 海洋环境科学, 2013, 32 (4):523–528. |
| [26] | Kwon S, Kim TS, Yu GH, et al. Bacterial community composition and diversity of a full-scale integrated fixed-film activated sludge system as investigated by pyrosequencing[J]. Journal of Microbiology and Biotechnology, 2010, 20 (12): 1717–1723. |
| [27] | Xia SQ, Duan L, Song YH, et al. Bacterial community structure in geographically distributed biological wastewater treatment reactors[J]. Environmental Science & Technology, 2010, 44 (19): 7391–7396. |
| [28] | Chen J, Xie P. Tissue distributions and seasonal dynamics of the hepatotoxic microcystins-LR and -RR in two freshwater shrimps, Palaemon modestus and Macrobrachium nipponensis, from a large shallow, eutrophic lake of the subtropical China[J]. Toxicon, 2005, 45 (5): 615–625. |
| [29] | Li JL, Wang ZH, Qing S, et al. Microbial diversity of sediments from the coasts of Dalian Changshan Islands[J]. Acta Microbiologica Sinica, 2011, 51 (5): 656–666. (in chinese) 李佳霖, 王中华, 秦松, 等. 大连长山群岛海岸带沉积物微生物群落结构特征[J]. 微生物学报, 2011, 51 (5):656–666. |
| [30] | Bai J, Li HY, Zhao YG. Bacterial distribution at different stations in the Northern Yellow Sea[J]. Acta Microbiologica Sinica, 2009, 49 (3): 343–350. (in chinese) 白洁, 李海艳, 赵阳国. 黄海北部不同站位海洋细菌群落分布特征[J]. 微生物学报, 2009, 49 (3):343–350. |
| [31] | Feng BW, Li XR, Wang JH, et al. Bacterial diversity of water and sediment in the Changjiang estuary and coastal area of the East China Sea[J]. FEMS Microbiology Ecology, 2009, 70 (2): 236–248. |
| [32] | Wang ZH, Yang JQ, Zhang DJ, et al. Composition of microbial communities in industrial drain outlets[J]. Journal of Pure and Applied Microbiology, 2014, 8 (1): 807–815. |
| [33] | Dong GF, Xie SQ, Zhu XM, et al. Nutri-toxicological effects of cyanobacteria on fish[J]. Acta Ecologica Sinica, 2012, 32 (19): 6233–6241. |
| [34] | Wang ZH, Yang JQ, Zhang DJ, et al. Composition and structure of bacterial communities in waste water of aquatic products processing factories[J]. Research Journal of Biotechnology, 2014, 9 (2): 65–70. |
 2016, Vol. 43
2016, Vol. 43




