扩展功能
文章信息
- 陆洪省, 刘文君, 张瑶, 王建燕, 张庆莹, 于梦梦
- LU Hong-Sheng, LIU Wen-Jun, ZHANG Yao, WANG Jian-Yan, ZHANG Qing-Ying, YU Meng-Meng
- 溶藻菌R1的分离鉴定以及对栅藻共处代谢的影响
- Identification of algicidal bacterium R1 and its influence on the metabolism of scenedesmus in a co-culture
- 微生物学通报, 2016, 43(3): 495-503
- Microbiology China, 2016, 43(3): 495-503
- 10.13344/j.microbiol.china.150498
-
文章历史
- 收稿日期: 2015-07-01
- 接受日期: 2015-09-02
- 优先数字出版日期(www.cnki.net): 2015-11-05
部分细菌具有溶解藻细胞、降解藻毒素的作用,被统称为溶藻细菌[1]。20世纪70年代,Daft等研究发现[2],富营养化水体中藻类叶绿素的含量与溶藻菌的数量之间存在着较好的相关性。在之后的几十年中,很多能溶解藻的细菌被分离出来[3],国外报道的主要溶藻菌有假单胞菌属Alteromonas sp.[4]、粘细菌属Myxobacter sp.[5]、芽孢杆菌属、黄杆菌属等。国内学者彭超等[6]分离获得3株溶藻细菌,生理生化鉴定为葡萄球菌属(Staphylococcus sp.)、芽孢杆菌属(Bacillus sp.)和节杆菌属(Arthrobacter sp.)。近些年来,国内外溶藻细菌大多分离自发生水华或赤潮的海洋及湖泊[4, 5, 7],大多为革兰氏阴性菌[1]。
生物除藻技术,尤其是利用溶藻菌来控制水华和赤潮的研究,越来越引起人们的关注[8, 9]。李云晖等研究了氧化铁纳米固定对溶藻菌除藻的影响[10],郭吉等对太湖中分离到的溶藻菌的降解藻毒素的效果进行了分析[11]。但到目前为止,溶藻菌除藻能力低、细菌有效抑制藻的生物量很低等仍然是制约生物除藻的关键因素[12]。另外,对溶藻菌抑制藻类生长机理的研究仍然非常有限,所作研究侧重于溶藻现象和溶藻方式,对溶藻细菌与藻共处培养过程中溶藻物质的鉴定、对藻类蛋白质表达以及光合作用的影响等涉及甚少。
本研究从微富营养化水体中分离到几株溶藻菌,并对其溶藻能力、溶藻机理进行初步分析,所用藻为微富营养化水样中的优势藻(栅藻),研究内容包括:抑藻物质的分离和鉴定(HPLC方法);溶藻菌对藻代谢(如光合作用)的影响;溶藻菌对藻蛋白表达的影响等。不仅对溶藻菌与藻共处培养中的动态变化进行分析,还从分子生物学水平上对溶藻菌抑制藻生长的机理进行初步分析,为溶藻菌抑制藻类的研究提供一定的理论和实践基础。
1 材料与方法 1.1 溶藻菌分离与培养溶藻菌富集:采用高氏一号培养基,培养基组成(g/L):可溶性淀粉20.0,NaCl 0.5,KNO3 1.0,K2HPO4·3H2O 0.5,MgSO4·7H2O 0.5,FeSO4·7H2O 0.01,pH调整至7.4-7.6,1×105 Pa灭菌20 min,待用。将10 mL微富营养化水样接种到含有150 mL高氏一号液体培养基的三角瓶中,30 ℃、150 r/min培养7 d。
溶藻菌的分离:采用牛肉膏蛋白胨固体培养基 (g/L):牛肉膏3.0,蛋白胨10.0,NaCl 5.0,琼脂20.0,pH调整为7.2。将上述富集培养液划线培养到牛肉膏蛋白胨固体平板培养基上,30 ℃静置培养,待长出菌落后,选取不同生长特征的单个菌落,经过多次划线分离纯化得到的多株纯种菌保存4 ℃,待用[13, 14]。
溶藻细菌的筛选:分别将上述分离到的溶藻菌接种到藻液中进行共培养,培养条件28 ℃,光照4.8±0.2 klx (日光灯源)。用肉眼观察藻的绿色深浅,从藻颜色由绿色变黄最快,共选出4株溶藻菌,暂命名为R1、R2、R3和R4,并保存在4 ℃,待用。
1.2 栅藻的分离和筛选藻分离培养基组成(g/L):硝酸钾1.25,磷酸二氢钾1.25,硫酸镁0.49,乙二胺四乙酸二钠0.5,硼酸0.1,微量元素0.21 ml,3% (质量体积比)的三氯化铁溶液,固体平板培养基配制时加入15 g/L的琼脂,pH调整为7.1,1×105 Pa灭菌20 min备用。藻的分离采用平板法,具体过程为:将含有藻的水样装入消毒过的小型喷雾器中,打开培养皿盖,把藻液喷射到固体平板培养基上,盖好盖,培养温度为28 ℃,光照4.8±0.2 klx (日光灯源)条件下培养,待长出藻菌落后,借助镜检用消毒过的接种环挑选栅藻,作为实验藻。水样取自山东科技大学砚湖,为轻度富营养化水体,栅藻形态观察依据《中国常见淡水浮游藻类图谱》[15]。
1.3 溶藻菌发酵上清液对栅藻生长的影响测定将分离纯化的溶藻菌在高氏一号液体培养基中28 ℃ (150 r/min)培养4 d,取发酵液4 ℃离心15 min (1 000 r/min),上清液用0.22 µm的无菌纤维素酯微孔滤膜过滤除菌,无菌滤液对栅藻培养液按体积比0、5%、10%和15%添加进行抑藻实验,培养温度为28 ℃,光照4.8±0.2 klx (日光灯源),每隔24 h取培养液,用作叶绿素a测定。在培养过程中,每隔12 h用溶氧仪(DO-6800,上海诺博环保科技有限公司)测定栅藻单独培养液以及溶藻菌抑菌物质条件下培养液中溶解氧含量。叶绿素a测定方法采用丙酮提取法,叶绿素a以及溶解氧测定时均采用3个平行实验。
1.4 溶藻菌生理生化性质测定溶藻菌生理生化性质测定按照《常见细菌系统鉴定手册》方法进行。溶藻菌生长曲线制作:将溶藻菌培养到牛肉膏蛋白胨液体培养基中,30 ℃、150 r/min培养。每隔24 h取样一次,在600 nm处测定吸光度,制作生长曲线。
1.5 溶藻菌对藻细胞生长影响测定藻细胞计数:将藻培养液用力振荡混匀,然后于无菌操作台取1 ml加入到2.5 ml EP管中,再加入1滴KI-I2溶液,染色15 min。每个样品设3个平行,将染色后液体滴入藻细胞计数板,于光学显微镜(100×)观察并计数,每样计数10次,计算平均数。
将生长对数期的溶藻菌(菌细胞浓度大约为4×106 cells/mL)培养液,按体积比1:4加入到藻培养液中进行共培养,溶藻菌及藻所用培养基分别同1.1和1.2中所述。菌藻共培养条件为28 ℃,光照4.8±0.2 klx (日光灯源),每隔24 h取藻菌培养液,对细胞进行计数,计数方法同上。以藻单独培养液做对照(未加溶藻菌培养),培养条件及计数方法同上,分别对藻细胞数目做生长曲线。
1.6 HPLC法测定溶藻菌活性物质每隔12 h取5 ml藻单独培养液以及藻菌共培养液(1.5),离心后取上清液,放入液氮中彻底冷却10 min,然后放入-80 ℃保存,等样品收集齐全后一起用高效液相色谱仪(Agilent1200,安捷伦科技公司)测定代谢产物甲酸或乙酸。高效液相色谱HPLC选用交换柱(HPX-87C,Bio-Rad),流动相为0.05 mmol/L H2SO4,柱温50 ℃,流速0.6 mL/min,每次进样量为20 μL,所用检测器为紫外检测器。
1.7 溶藻菌对藻蛋白表达影响测定将藻单独培养以及溶藻菌与藻类共培养两组实验进行对照,分析溶藻菌对藻蛋白表达的影响。培养条件同1.5,培养4 d后,分别取培养液2 000 r/min离心10 min,用无菌水进行洗涤,重复上述操作8次,最终获得藻泥,然后用细胞破碎仪对藻泥进行细胞破碎,破碎液在4 ℃下10 000 r/min离心15 min,收集上清液,采用紫外线测定其中蛋白质浓度,测定波长为280 nm和260 nm,蛋白质含量(g/L)计算公式:
蛋白质含量(g/L)=1.55×OD280- 0.76×OD260。
1.8 相差显微镜观察溶藻菌-藻共培养在藻单独培养和溶藻菌-藻共培养过程中,分别定时取培养液在相差显微镜(BM-PH,上海光学仪器厂)下观察,放大倍数为400×,分析溶藻菌对藻生长的动态影响。
1.9 溶藻菌对藻细胞结构的影响测定溶藻菌培养液10 000 r/min离心15 min,再用0.22 μm微孔滤膜对离心上清液过滤除菌得20 mL溶藻菌发酵液,将此发酵液与藻进行共培养作为实验组,对照组中以20 ml藻液体培养基代替溶藻菌发酵液,两者培养条件同1.5所述,分别培养7 d后10 000 r/min离心15 min收集藻,利用低温冷冻干燥机制得藻干粉,取藻干燥粉用KBr固定后于傅里叶红外光谱仪(FTIR-8900,天津市拓普仪器有限公司)测定。
2 结果与分析 2.1 溶藻菌的分离及生理生化测定结果根据溶藻菌与栅藻共处培养时栅藻颜色变化情况,挑选4株抑藻能力强的溶藻菌进行生理生化等性质测定,并把这4株溶藻菌暂分别命名为R1、R2、R3和R4。按照《常见细菌系统鉴定手册》判断溶藻菌R1、R2、R3和R4均为革兰氏阴性,且在固体平板培养基上形成的菌落均为白色、圆形。氧化酶、尿素反应、蔗糖利用、葡萄糖利用均为阳性(表 1),因此,溶藻菌R1、R2、R3和R4可初步判定属于芽孢杆菌属Bacillus sp.。
| Items | R1 | R2 | R3 | R4 |
| Shape Gram staining | Long rod - | Long rod - | Long rod - | Long rod - |
| Nitrate reduction | + | + | + | + |
| Nitrite reduction | + | + | + | + |
| Catalase | - | - | + | + |
| Oxidase | + | + | + | + |
| Arginine | - | - | - | - |
| Ornithine | - | + | - | + |
| Lysine | + | - | - | - |
| Urea | + | + | + | + |
| Sucrose | + | + | + | + |
| Maltose | + | - | - | + |
| Glucose | + | + | + | + |
| Xylose | - | - | - | - |
| Peptone | + | + | - | - |
藻类能够利用光进行光合作用,产生氧气。从表 2可以看出,分离得到的4株溶藻菌对栅藻的光合作用都具有一定的抑制作用,其中溶藻菌R1对栅藻的抑制效果最明显。另外,将上述分离到的4株溶藻菌分别与栅藻共处培养,培养4 d后,发现藻类均有不同程度的变白或颜色变浅变黄的现象,其中与溶藻菌R1共处培养的栅藻变化最明显,由此初步判定溶藻菌R1对栅藻的抑制能力最强。
| 时间 Time (d) | 清水 Rinsing | 藻液Solution of algae | R1+藻 R1+Solution of algae | R2+藻 R2+Solution of algae | R3+藻 R3+Solution of algae | R4+藻 R4+Solution of algae |
| 1 | 8.3 | 10.3 | 9.9 | 10.8 | 11.1 | 10.4 |
| 2 | 8.4 | 11.7 | 9.4 | 10.1 | 10.7 | 9.6 |
| 3 | 8.4 | 12.7 | 7.4 | 8.5 | 7.3 | 9.1 |
| 4 | 8.6 | 13.1 | 7.1 | 8.2 | 7.1 | 8.7 |
| 5 | 8.4 | 12.1 | 6.6 | 7.1 | 6.7 | 7.3 |
| 6 | 8.5 | 10.4 | 6.5 | 6.8 | 6.7 | 7.4 |
将4株溶藻细菌(R1、R2、R3和R4)在30 ℃、150 r/min振荡培养至菌悬液OD600值为0.4,然后离心,再对上清液过滤除菌,分别取无菌滤液50 mL加入到200 ml栅藻培养液中,同时设空白对照,培养1 d后分别测定叶绿素a浓度,计算溶藻菌对叶绿素a的抑制率,结果如图 1所示。从图 1可以看出,R1对藻叶绿素a的抑制效果最明显,高达65%,R3对叶绿素a的去除率最低,为21%。结合上述溶藻菌对藻类释放氧的抑制结果,选择溶藻菌R1作为代表菌株来研究其生长曲线,以及对栅藻蛋白等的抑制机理。
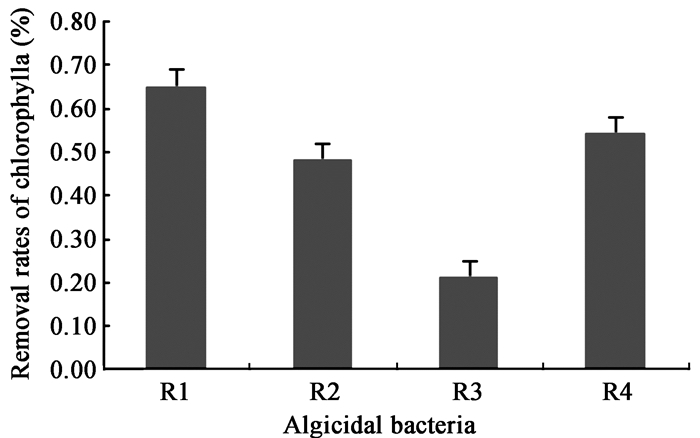 |
| 图 1 各溶藻菌对藻叶绿素a的去除率 Figure 1 The removal of chlorophyll a by algicidal bacteria |
| |
将溶藻菌R1单独在高氏一号液体培养基中培养,每隔1 d取培养液测定其600 nm处吸光度(OD600),做成如图 2所示生长曲线。从图 2可以看出,溶藻菌R1迟缓期较短,而对数增长期较长,在培养5 d左右时,溶藻菌R1生长量达到最大,以后随培养时间延长生物量减小。
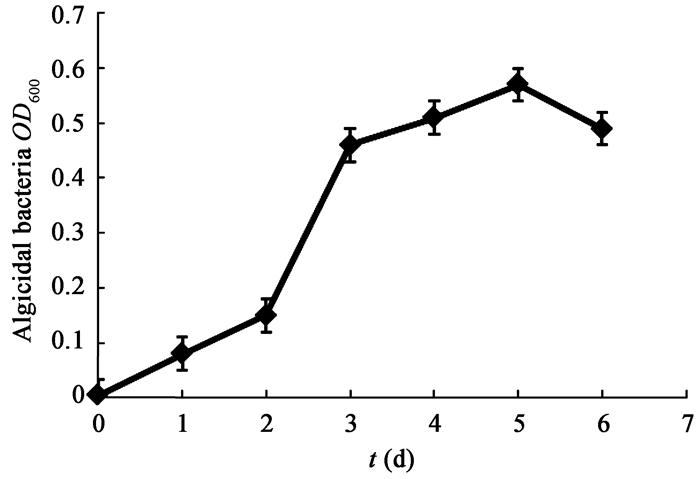 |
| 图 2 溶藻菌R1的生长曲线 Figure 2 The growth curve of algicidal bacteria R1 |
| |
利用染色方法对藻细胞数目进行计数,分别做溶藻菌R1与栅藻共培养以及栅藻单独培养两种情况下的栅藻细胞数目随时间变化曲线(图 3)。从图 3可以看出,溶藻菌R1与栅藻共处培养过程中,随培养时间的延长,栅藻细胞数目持续减少,经过6 d的培养,栅藻从最初的1.6×106 cells/mL下降到0.1×106 cells/mL。而栅藻单独培养条件下,藻细胞数目随培养时间延长而增加,从最初的1.6×106 cells/mL增加到8.7×106 cells/mL。
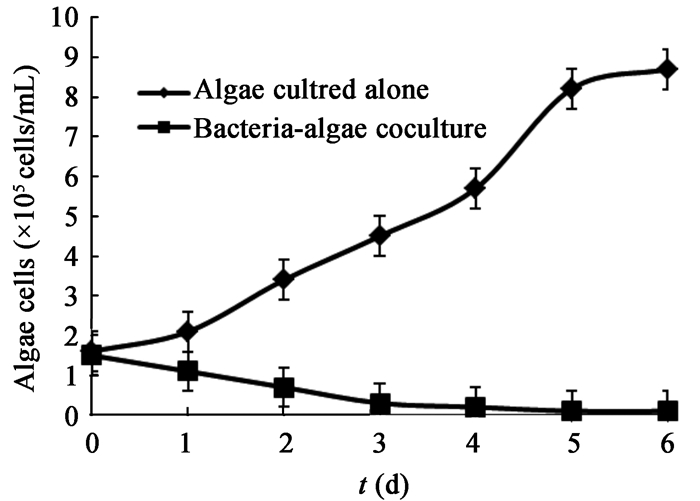 |
| 图 3 溶藻菌对藻细胞生长的抑制 Figure 3 The inhibition of algicidal bacteria on the growth of algae |
| |
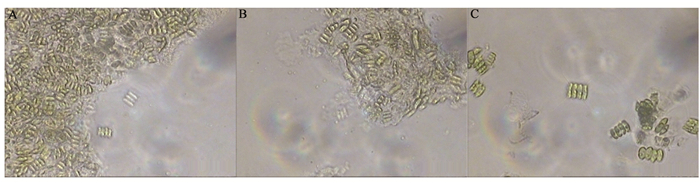
图 4A为溶藻菌R1与栅藻共培养5 d,栅藻颜色明显变黄,而栅藻单独培养5 d后(图 4B),栅藻颜色仍然深绿色。分别取溶藻菌R1与栅藻共培养3 d和5 d,栅藻单独培养7 d时的培养液在相差显微镜下观察,结果分别如图 5A、B和C所示。从图 5A和图 5B可以看出,藻类经过5 d培养后死亡或者是溶解的细胞数量远远高于培养3 d时藻类,原因可能是溶藻菌R1在与藻培养过程中代谢产生的某些物质抑制了或者溶解了藻类细胞,使藻类细胞生长变慢或是直接细胞破裂而死亡。另外,图 5A、B与图 5C比较,藻单独培养时,藻的颜色明显比与溶藻菌R1共培养时绿,因此,溶藻菌R1对藻的生长抑制作用非常明显。
 |
|
图 4 藻在不同培养条件下的生长
Figure 4 The growth of algae under different culture conditions
注:A:藻与菌共培养5 d;B:藻单独培养5 d. Note: A: The coculture of algae with algicidal bacteria for 5 days; B: Singleculture of algae for 5 days. |
| |
 |
|
图 5 不同培养条件下藻生长的相差显微镜图
Figure 5 Phase contrast microscope observation for algae under different culture conditions
注:A:藻与溶藻菌共培养3 d;B:藻与溶藻菌共培养5 d;C:藻单独培养7 d. Note: A: The 3 days coculture of algicidal bacteria with algae after; B: The 5 days coculture of algicidal bacteria with algae; C: The 7 days culture of algae alone. |
| |
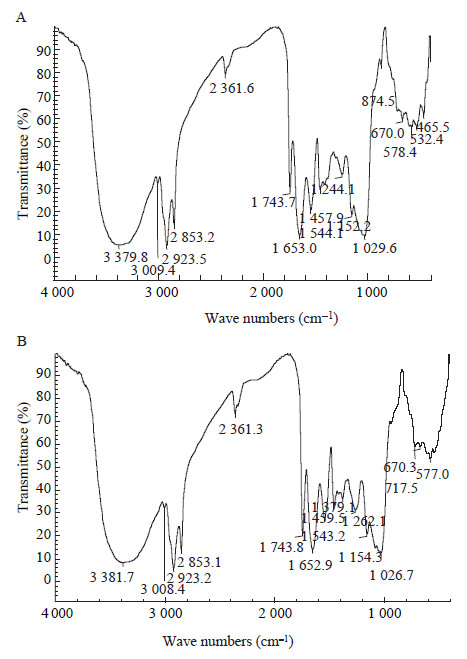
用傅里叶红外光谱对正常藻类(对照组,无溶藻菌加入)细胞及溶藻菌发酵液(实验组)处理后的产物进行分析,结果如图 6A和6B所示。由图 6可见,对照组和处理组中,藻类产物红外吸收光谱中主要的吸收峰位置大致一致,峰形非常相近,但各吸收峰的相对强度有所差异。从峰的归属来看,对照组3 379 cm-1和实验组3 381 cm-1处为O-H伸缩振动区,其振动变弱可能是藻细胞内多糖和蛋白质组分中O-H键遭到破坏;对照组在1 244 cm-1出现吸收峰,而实验组在1 262 cm-1出现较强的吸收峰,这可能是C-C键伸缩振动区受到影响所致,表明藻类细胞结构受到破坏。
 |
|
图 6 藻在不同培养条件下的红外光谱图
Figure 6 Infra-red spectrogram of algae under different culture conditions
注:A:藻单独培养;B:藻与溶藻菌共培养. Note: A: Algae cultured alone; B: The coculture of algae with algicidal bacteria. |
| |
分别对藻单独培养液以及溶藻菌与藻共培养液进行离心,分离到藻类,再用细胞破碎仪破碎藻细胞,并用紫外方法测定处理液中藻蛋白的浓度,结果如表 3所示。从表 3可以看出,藻单独培养时藻蛋白浓度最高,为0.845 7 g/L,与溶藻菌R4共培养下的藻蛋白最低,只有0.192 6 g/L,因此,溶藻菌R1体现除了很强的抑藻效果。
| Alage cultured | Only | R1 | R2 | R3 | R4 |
| Protein concentration | 0.845 7 | 0.192 6 | 0.200 1 | 0.194 5 | 0.556 1 |
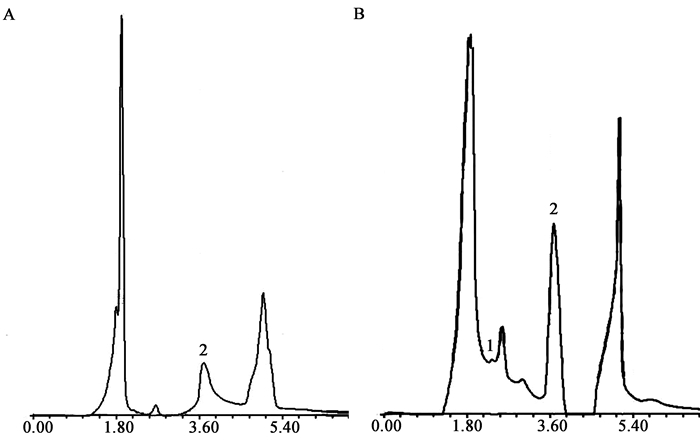
许丽丽[16]报道了甲酸、乙酸是菌藻共处中产生的能够影响藻类光合作用的特性物质。本研究中,通过高效液相色谱HPLC对溶藻菌与栅藻共处培养中甲酸和乙酸的产生进行了测定,结果如图 7所示。图 7中,1号峰代表甲酸,出峰时间大概为2.38 min,2号峰代表乙酸,出峰时间大概为3.68 min,从图 7A可以看出,在菌藻共处培养液中只有乙酸被检测出,从图 7B可以看出,在藻单独培养液中,甲酸、乙酸均被检测到,可能原因是溶藻菌R1与栅藻共培养过程中溶藻菌对栅藻的代谢产生了影响,抑制了藻类对乙酸的产生代谢。
 |
|
图 7 溶藻特性物质的液相色谱测定
Figure 7 Algae-lysing substance determination with HPLC
注:A:藻与溶藻菌共培养;B:藻单独培养. Note: A: Algicidal bacteria cocultured with algae; B: Algae cultured alone. |
| |
关于溶藻机理,一般认为溶藻菌分泌杀藻物质通过作用于藻的生理过程,来达到抑制或杀死藻细胞的结果。Daft等[2]研究发现,细菌可以通过分泌能溶解藻细胞壁的酶来逐渐溶解整个藻细胞。在本研究中,通过HPLC测得溶藻菌R1与栅藻共培养液中只有乙酸没有甲酸,而在栅藻单独培养时甲酸和乙酸均被检测出,可能的原因是溶藻菌与栅藻共培养过程中,溶藻菌R1抑制了栅藻对甲酸的产生代谢。另外,溶藻菌对栅藻蛋白表达量以及细胞结构上的影响在本研究也被证明(表 3和图 6),这可能原因是溶藻菌能分泌溶解栅藻细胞壁的物质。另外,溶藻菌与栅藻共培养体系中溶解氧的浓度明显低于栅藻单独培养(表 2),Banin等[17]和Subashchandrabose等[18]认为溶藻作用是通过抑制或影响藻细胞的光合作用来实验的。据赵鹏[19]研究表明,细菌与藻共培养过程中,由于细菌能消耗藻类光合作用产生的氧气而使共培养体系中溶解氧浓度降低。
本研究中溶藻菌与栅藻共培养体系中溶解氧低的原因,极有可能是溶藻菌对栅藻光合作用的抑制导致,因为溶藻菌对栅藻叶绿素a、栅藻蛋白的表达、代谢过程等都产生了明显的抑制效果,但是溶藻菌抑制栅藻光合作用的机理还需要进一步研究来阐释。
| [1] | Wu G, Xi Y, Zhao YJ. The latest development of research on algae-lysing bacteria[J]. Research of Environmental Sciences, 2002, 15(5): 43-46 (in Chinese) 吴刚, 席宇, 赵以军. 溶藻细菌研究的最新进展[J]. 环境科学研究, 2002, 15(5): 43-46 |
| [2] | Daft MJ, McCord SB, Stewart WDP. Ecological studies on algal-lysing bacteria in fresh waters[J]. Freshwater Biology, 1975, 5(6): 577-596 |
| [3] | Lee YK, Ahn CY, Kim HS, et al. Cyanobactericidal effect of Rhodococcus sp. isolated from eutrophic lake on Microcystis sp.[J]. Biotechnology Letters, 2010, 32(11): 1673-1678 |
| [4] | Imai I, Ishida Y, SakaguchiK, et al. Algicidal marine-bacteria isolated from northern Hiroshima bay, Japan[J]. Fisheries Science, 1995, 61(4): 628-636 |
| [5] | Kato J, Amie J, Murata Y, et al. Development of a genetic transformation system for an alga-lysing bacterium[J]. Applied and Environmental Microbiology, 1998, 64(6): 2061-2064 |
| [6] | Peng C, Wu G, Xi Y, et al. Isolation and identification of three algae-lysing bacteria and their lytic effects on blue-green algae (Cyanobacteria)[J]. Research of Environmental Science, 2003, 16(1): 37-40 (in Chinese) 彭超, 吴刚, 席宇, 等. 3株溶藻细菌的分离鉴定及其溶藻效应[J]. 环境科学研究, 2003, 16(1): 37-40 |
| [7] | Lovejoy C, Bowman JP, Hallegraeff GM. Algicidal effects of a novel marine Pseudoalteromonas isolate (class proteobacteria, gamma subdivision) on harmful algal bloom species of the Genera Chattonella, Gymnodinium, and Heterosigma[J]. Applied and Environmental Microbiology, 1998, 64(8): 2806-2813 |
| [8] | Chow CWK, Drikas M, House J, et al. The impact of conventional water treatment processes on cells of the cyanobacterium Microcystis aeruginosa[J]. Water Research, 1999, 33(15): 3253-3262 |
| [9] | Mayali X, Doucette GJ. Microbial community interactions and population dynamics of an algicidal bacterium active against Kareniabrevis (Dinophyceae)[J]. Harmful Algae, 2002, 1(3): 277-293 |
| [10] | Li YH, Pu YP, Yin LH, et al. Algae-lytic effect of algicidal bacteria mimobilized on Fe2O3 nanoparticles[J]. Journal of Southest University (Natural Science Edition), 2006, 36(6): 986-990 (in Chinese) 李云晖, 浦跃朴, 尹立红, 等. 氧化铁纳米颗粒固定化溶藻菌的除藻作用[J]. 东南大学学报: 自然科学版, 2006, 36(6): 986-990 |
| [11] | Guo J, Pu YP, Yin LH, et al. Isolation and evaluation of algicidal bacteria from Taihu Lake[J]. Journal of Southeast University (Natural Science Edition), 2006, 36(2): 293-297 (in Chinese) 郭吉, 浦跃朴, 尹立红, 等. 太湖溶藻细菌的分离及评价[J]. 东南大学学报: 自然科学版, 2006, 36(2): 293-297 |
| [12] | Jin LN, Zhang WH, Zheng L, et al. Biodegradation of microcystin in Dianchi Lake aquatic environment[J]. China Environmental Science, 2002, 22(2): 189-192 (in Chinese) 金丽娜, 张维昊, 郑利, 等. 滇池水环境中微囊藻毒素的生物降解[J]. 中国环境科学, 2002, 22(2): 189-192 |
| [13] | Kong Y, Miao LH, Zhu L, et al. Effects of algae-lysing Streptomyces on the competition between Microcystis aeruginosa and Chlorella pyrenoidosa[J]. Ecology and Environmental Sciences, 2010, 19(11): 2657-2662 (in Chinese) 孔赟, 缪礼鸿, 朱亮, 等. 溶藻放线菌对铜绿微囊藻和小球藻竞争生长的影响[J]. 生态环境学报, 2010, 19(11): 2657-2662 |
| [14] | Kong Y, Zhu L, Qi JQ, et al. Characteristics of algae removal and nitrogen removal from micro-polluted source water by algae-lysing bacterium[J]. Ecology and Environmental Sciences, 2012, 21(8): 1440-1446 (in Chinese) 孔赟, 朱亮, 戚姣琴, 等. 溶藻菌对受污染水源水除藻及脱氮特性研究[J]. 生态环境学报, 2012, 21(8): 1440-1446 |
| [15] | Weng JZ, Xu HS. Chinese Common Freshwater Planktonic Algae[M]. Shanghai: Shanghai Science and Technology Press, 2010 (in Chinese) 翁建中, 徐恒省. 中国常见淡水浮游藻类图谱[M]. 上海: 上海科学技术出版社, 2010 |
| [16] | Xu LL. Hydrogen production improvement by means of co-cultivation of Chlamydomonas reinhardtii and Bradyrhizobium japonicum and its eco-physiological mechanisms[D]. Shanghai: Doctoral Dissertation of East China Normal University, 2014 (in Chinese) 许丽丽. 莱茵衣藻与根瘤菌共培养提高产氢及其生理生态学机理[D]. 上海: 华东师范大学博士学位论文, 2014 |
| [17] | Banin E, Khare SK, Naider F, et al. Proline-rich peptide from the coral pathogen Vibrio shiloi that inhibits photosynthesis of Zooxanthellae[J]. Applied and Environmental Microbiology, 2001, 67(4): 1536-1541 |
| [18] | Subashchandrabose SR, Ramakrishnan B, Megharaj M, et al. Consortia of cyanobacteria/microalgae and bacteria: biotechnological potential[J]. Biotechnology Advances, 2011, 29(6): 896-907 |
| [19] | Zhao P. Study on the isolation of oleaginous microalgae and their co-cultivation[D]. Kunming: Doctoral Dissertation of Yunnan Normal University, 2014 (in Chinese) 赵鹏. 产油微藻的分离及藻-藻共培养的研究[D]. 昆明: 云南师范大学博士学位论文, 2014 |
 2016, Vol. 43
2016, Vol. 43