扩展功能
文章信息
- 张晔, 高红梅, 陈文丽, 谭青海, 刘静莎, 谷晔, 张健鹏
- ZHANG Ye, GAO Hong-Mei, CHEN Wen-Li, TAN Qing-Hai, LIU Jing-Sha, GU Ye, ZHANG Jian-Peng
- 光声光谱技术用于绿脓杆菌的鉴定
- Identification of Pseudomonas aeruginosaby photoacoustic spectroscopy
- 微生物学通报, 2016, 43(11): 2506-2513
- Microbiology China, 2016, 43(11): 2506-2513
- DOI: 10.13344/j.microbiol.china.160004
-
文章历史
- 收稿日期: 2016-01-04
- 接受日期: 2016-02-04
- 优先数字出版日期(www.cnki.net): 2016-03-04
2. 北京市门头沟区医院 北京 102300 ;
3. 武警总医院呼吸内科 北京 100039
2. Beijing Mentougou District Hospital, Beijing 102300, China ;
3. Department of Respiratory Disease, General Hospital of the Chinese People's Armed Police Forces Beijing 100039, China
绿脓杆菌广泛分布于自然界和人的皮肤、呼吸道及肠道中,是医院内感染常见的机会致病菌之一。绿脓杆菌感染多发生在大面积烧伤、创伤,长期使用免疫抑制剂,全身情况差或有严重基础疾病的患者。近年,其发病率逐年攀升,诊疗效果差,致残率及病死率均较高,已成为一种难治的感染性疾病。因此,实现对绿脓杆菌感染的早期诊断并进行及时、有效的抗生素治疗,有着非常重要的意义。然而,目前的相关诊断技术均存在一些问题,如影像学检查敏感性差,咽拭子培养选择性低、培养周期长,支气管肺泡灌洗有创损伤大,核酸及血清学检测技术要求高、费用昂贵、标本获取困难等[1-5]。
近期相关研究表明,绿脓杆菌是少数几种可以产生HCN的细菌之一(有文献报道,洋葱伯克氏菌Burkholderia cepacia也能产生极低浓度的HCN)[6]。通过检测绿脓杆菌细菌挥发性代谢产物中的HCN,可作为与其它细菌的鉴定依据(其选择性为68%,特异性为99%)[6-9]。此外,绿脓杆菌定殖的病人(如肺囊性纤维化)呼出气中HCN的浓度也显著高于正常人HCN的浓度[10-20]。
光声光谱技术是一种理想的无背景噪声信号技术。与传统光谱分析方法不同,光声光谱技术是监测气体吸收光能后产生的热能中以声压形式表现出来的那部分能量,属于绝对法测量,即使在弱吸收的情况下,吸收能也可被微音器检测,因此具有较高的灵敏度和良好的选择性[21]。从国际上看,光声光谱法气体测量技术是目前最为先进的痕量气体测量技术之一,基于光声光谱原理的气体分析仪产品属于红外类气体分析仪中的高端产品。
本研究中使用的光声光谱分析仪(photoacoustic spectroscopy trace analyzer-1001,PASTA-1001)是由中国航天科技集团某研究所针对载人航天器舱内痕量气体检测需求进行研究开发的,具有小体积、低功耗、高性能的优点。其基本测量原理是红外激光通过光声池,待测气体吸收光能量后产生脉冲压力波,即声信号。硅MEMS悬臂梁光学微音器检测声压的微小变化,其声压信号的幅度与待测气体浓度成正比[21]。
本文使用光声光谱分析仪(PASTA-1001)检测肺部感染性疾病中两种常见致病菌(大肠杆菌和绿脓杆菌)的挥发性代谢产物,获得他们的光声光谱图谱。通过分析其图谱的差异来初步鉴定细菌。
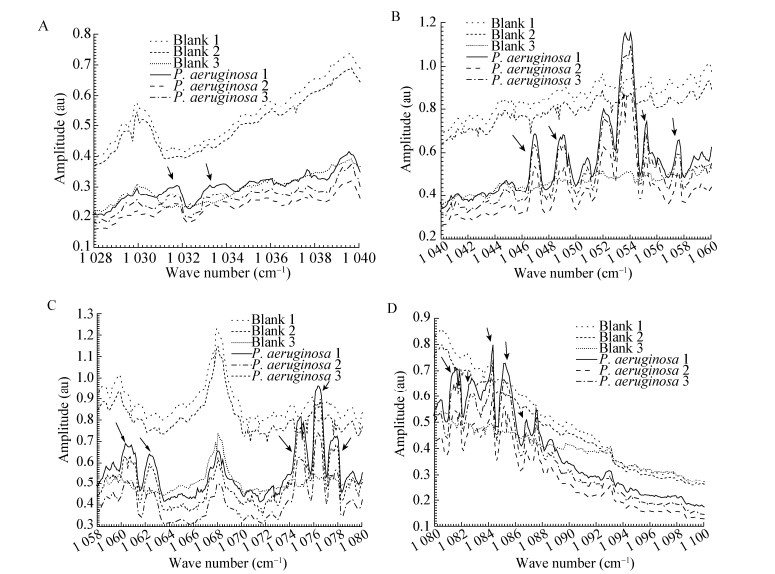
1 材料与方法 1.1 实验材料及仪器 1.1.1 实验菌株: 大肠杆菌ATCC25922标准菌株、绿脓杆菌ATCC27853标准菌株,均由武警总医院检验科微生物室提供,两者均为革兰氏阴性杆菌,大肠杆菌为兼性厌氧,绿脓杆菌为需氧菌。 1.1.2 实验仪器: 光声光谱分析仪(PASTA-1001),中国航天科技集团某研究所;恒温恒湿培养箱,宁波赛福试验仪器有限公司;麦康凯培养皿,上海微蒙生物科技有限公司;自制双通道玻璃气密样品取样瓶,两通道各接有一根橡皮管等。 1.2 实验方法 1.2.1 气体收集: 实验组:分别挑取单菌落绿脓杆菌、大肠杆菌接种在麦康凯培养皿。对照组:空白麦康凯培养皿。实验组和对照组均分别置于玻璃气密样品取样瓶中,并用止血钳夹闭两侧橡皮管,35 ℃培养24 h。为确保实验的可重复性,试验组和对照组分别重复3次。 1.2.2 气体检测: 用光声光谱分析仪(PASTA-1001)分别检测各组取样瓶中的气体,分别获得初始实验数据和初始光谱曲线[X值表示波数(cm-1),Y值表示幅值(au)],检测波数范围为1 000-1 250 cm-1。 2 结果与分析 2.1 对照组和绿脓杆菌组挥发性代谢产物光声光谱测试结果图 1分别显示了对照组和绿脓杆菌在35 ℃培养箱中培养24 h后测得的光声光谱图(每组实验重复3次)。从整体上看,3组对照组及3组绿脓杆菌组图谱的重复性均较好。这表明实验中使用的光声光谱分析仪稳定性较好,且该实验的重复性较高。由于图 1中图谱数据较多,不方便将绿脓杆菌组的图谱与对照组的图谱一一进行比对分析,将其中部分波数段进行了放大,如图 2所示。

|
| 图 1 在35 ℃下培养24 h后对照组和绿脓杆菌的光声光谱测试结果 Figure 1 Photoacoustic spectral measurement results of VCs of Pseudomonas aeruginosa and blank groups after 24 h culture at 35 ℃ |
|
|
从图 2中可以看出,在某些波数段,绿脓杆菌挥发性代谢产物的光声光谱图谱与对照组明显不同。例如,在图 2a中的1 032及1 034两个波数附近,绿脓杆菌组均明显出现了波峰,而在对照组则是平滑曲线。类似地,在图 2B中1 046-1 048、1 048-1 050、1 055、以及1 057波数附近,绿脓杆菌组也都出现了明显的波峰,而对照组则未然。相似情况在图 2C中的1 060-1 064、1 074-1 078波数段以及图 2D中的1 081-1 088以及1 094-1 100波数段均有出现。此外,本文也在1 104-1 106、1 116-1 120、1 126-1 132、1 144-1 150、1 158-1 160、1 164-1 174以及1 178-1 180波数段发现了类似的情况,由于篇幅原因,这些波数段的放大图并未给出。
2.2 标准图谱测试结果为了进一步探究这些波数段出现峰值的原因及其对应物质,进行了大量文献的调研。发现绿脓杆菌在生长过程中会产生大量的HCN气体,而大肠杆菌则鲜有报道[6-9]。考虑实验时不可避免地带入一些水和乙醇,进行了乙醇、水蒸气以及HCN标准图谱的测试,测试结果如图 3所示。

|
| 图 3 HCN、乙醇以及水的标准图谱 Figure 3 Standard photoacoustic spectroscopy of HCN, Ethyl alcohol and H2O Note: A: Ethyl alcohol; B: H2O; C: HCN. |
|
|
从图 3A可以看出,乙醇标准图谱的特征峰主要出现在1 000-1 100这个波数段。对比图 3A和图 1可以发现,在1 000-1 100这个波数段,两者有着惊人的类似。这表明,在绿脓杆菌组和对照组的挥发性气体中均含有乙醇,这可能是实验装置处理阶段留下的或者细菌代谢过程中产生的。类似地,对比图 3B和图 1可以发现,两者在1 150-1 250波数段也非常相似,初步判断绿脓杆菌组和对照组的挥发性气体中都含有水。由于HCN标准图谱较为复杂,很难通过直观对比进行判断,本文利用“逆向思维”的方法进行了分析。将绿脓杆菌组的图谱与HCN标准图谱进行叠加,若叠加后图谱出现峰值的峰型及波数段与叠加前完全一致,则说明绿脓杆菌代谢产物中含有HCN;反之,则不含HCN。叠加前后的图谱如图 4所示。

|
| 图 4 实验测得的绿脓杆菌挥发性代谢产物图谱叠加HCN标准图谱后图谱 Figure 4 The overlapped photoacoustic spectroscopy obtained on the VCs of Pseudomonas aeruginosa and the standard HCN 注:A:整体图谱;B-F:局部放大图. Note: A: The whole photoacoustic spectroscopy; B-F: The partial enlarged photoacoustic spectroscopy. |
|
|
图 4A是叠加前后图谱的整体对比图。可以看出,整体上两者出现波峰的峰型一致,波数段基本相同,吻合性较好。为了能更清楚地对比,将图 3C中HCN图谱出现特征峰的波数段进行放大,如图 4B-F所示。可以看出,在HCN出现特征峰的波数段中,叠加前后图谱出现峰值的波数段及峰型基本一致。换句话说,HCN标准图谱的叠加并未改变绿脓杆菌挥发性代谢产物图谱的峰型及峰位。因此,可以初步判断绿脓杆菌挥发性代谢产物中含有HCN气体。
2.3 大肠杆菌组挥发性代谢产物光声光谱测试结果为了对上述结论进行进一步的验证,进行了大肠杆菌在35 ℃下培养24 h后的光声光谱测试,并将测试得到的图谱与HCN标准图谱进行叠加,叠加前后的图谱如图 5所示。可以看出,大肠杆菌挥发性代谢产物中也含有乙醇和水。此外,叠加后的图谱与叠加前的图谱在1 100-1 200波数段有着明显的不同,而这个波数段正是HCN特征峰的位置。需要指出的是,由于乙醇的特征峰在1 000-1 100这个波数段,且其峰值强度很高,远高于图 3C中HCN在1 025-1 080波数段特征峰的强度,所以图 4A中叠加后图谱在1 025-1 080波数段的波峰被淹没,叠加前后图谱在该波数段均出现了波峰。其中叠加前的波峰是由乙醇引起的,而叠加后的波峰则是乙醇和HCN共同导致的,但前者占主导地位。

|
| 图 5 在35 ℃下培养24 h后测得大肠杆菌挥发性代谢产物的光声光谱图谱叠加HCN标准图谱后的图谱. Figure 5 The overlapped photoacoustic spectroscopy obtained on the VCs of E. coli cultured at 35 ℃ for 24 h and the standard HCN 注:A:整体图谱;B-F:部分波数段的放大图. Note: A: The whole photoacoustic spectroscopy; B-F: The partial enlarged photoacoustic spectroscopy. |
|
|
为了更方便地进行比对,将部分波数段进行放大处理,如图 5B-F所示。可以清楚地看出,叠加后图谱在1 096-1 100、1 104-1 106、1 116-1 120、1 126-1 132、1 144-1 150、1 158-1 160、1 162-1 174以及1 178-1 180这几个波数段均出现了波峰,而叠加前图谱在这个波数段均是较为平坦的曲线。此外,这几个波数段正是HCN标准图谱中出现特征峰的波数段。因此,可以初步判断大肠杆菌的挥发性代谢产物中并没有HCN,这与已有的大肠杆菌代谢产物报道相似[6-19]。同时,这也从侧面证实了该“逆向思维”的可行性。
3 结论光声光谱技术是近年来兴起的一种能够对微量气体进行快速、可靠检测的技术。本文利用光声光谱技术对绿脓杆菌及大肠杆菌挥发性代谢产物进行了检测,并用“逆向思维”的方法对其检测图谱进行了分析。结果发现,绿脓杆菌挥发性代谢产物中含有特征性代谢产物HCN,从而可以对绿脓杆菌进行初步的鉴定。为了验证该方法的可行性,对大肠杆菌的代谢产物进行了光声光谱测试和分析,发现其中并未含有HCN,这与之前的有关报道相符,证实了该方法的可行性。
然而,需要指出的是,目前光声光谱技术在微生物鉴定中的应用正处于研究起步阶段,后期需要大量的研究来将其推广。为此,本文提出了“三步走”策略:第一步,需要收集目前已知细菌的特征性代谢产物,并用光声光谱技术对其标准图谱进行大量的测试,形成一个大型数据库,即大数据[22];第二步,需要进行“比对算法”的完善,通过大量的研究,对本文提出的“逆向思维”算法进行完善,使其可以借助计算机进行自动比对,提高比对的效率和精度;第三步,基于研究成果,建立一套完善的“自动检测-自动比对-自动校对-自动鉴定”系统,从而加速其临床应用。
| [1] | Arslanov DD, Castro MPP, Creemers NA, et al. Optical parametric oscillator-based photoacoustic detection of hydrogen cyanide for biomedical applications[J]. Journal of Biomedical Optics 2013, 18(10) : 107002. DOI:10.1117/1.JBO.18.10.107002 |
| [2] | Meng L, Liu X, Wang B, et al. Simultaneous derivatization and extraction of free cyanide in biological samples with home-made hollow fiber-protected headspace liquid-phase microextraction followed by capillary electrophoresis with UV detection[J]. Journal of Chromatography B 2009, 877(29) : 3645–3651. DOI:10.1016/j.jchromb.2009.09.006 |
| [3] | Shang L, Dong SJ. Design of fluorescent assays for cyanide and hydrogen peroxide based on the inner filter effect of metal nanoparticles[J]. Analytical Chemistry 2009, 81(4) : 1465–1470. DOI:10.1021/ac802281x |
| [4] | Lü JG, Zhang ZJ, Li JD, et al. A micro-chemiluminescence determination of cyanide in whole blood[J]. Forensic Science International 2005, 148(1) : 15–19. DOI:10.1016/j.forsciint.2004.03.032 |
| [5] | Abbaspour A, Asadi M, Ghaffarinejad A, et al. A selective modified carbon paste electrode for determination of cyanide using tetra-3, 4-pyridinoporphyrazinatocobalt (Ⅱ)[J]. Talanta 2005, 66(4) : 931–936. DOI:10.1016/j.talanta.2004.12.062 |
| [6] | Neerincx AH, Mandon J, van Ingen J, et al. Real-time monitoring of hydrogen cyanide (HCN) and ammonia (NH3) emitted by Pseudomonas aeruginosa[J]. Journal of Breath Research 2015, 9(2) : 027102. DOI:10.1088/1752-7155/9/2/027102 |
| [7] | Carroll W, Lenney W, Wang TS, et al. Detection of volatile compounds emitted by Pseudomonas aeruginosa using selected ion flow tube mass spectrometry[J]. Pediatric Pulmonology 2005, 39(5) : 452–456. DOI:10.1002/(ISSN)1099-0496 |
| [8] | Shestivska V, Španĕl P, Dryahina K, et al. Variability in the concentrations of volatile metabolites emitted by genotypically different strains of Pseudomonas aeruginosa[J]. Journal of Applied Microbiology 2012, 113(3) : 701–713. DOI:10.1111/jam.2012.113.issue-3 |
| [9] | Sohrabi M, Zhang L, Zhang K, et al. Volatile organic compounds as novel markers for the detection of bacterial infections[J]. Clinical Microbiology: Open Access 2014, 3(3) : 1000151. |
| [10] | Enderby B, Smith D, Carroll W, et al. Hydrogen cyanide as a biomarker for Pseudomonas aeruginosa in the breath of children with cystic fibrosis[J]. Pediatric Pulmonology 2009, 44(2) : 142–147. DOI:10.1002/ppul.v44:2 |
| [11] | Stutz MD, Gangell CL, Berry LJ, et al. Cyanide in bronchoalveolar lavage is not diagnostic for Pseudomonas aeruginosa in children with cystic fibrosis[J]. European Respiratory Journal 2011, 37(3) : 553–558. DOI:10.1183/09031936.00024210 |
| [12] | Savelev SU, Perry JD, Bourke SJ, et al. Volatile biomarkers of Pseudomonas aeruginosa in cystic fibrosis and noncystic fibrosis bronchiectasis[J]. Letters in Applied Microbiology 2011, 52(6) : 610–613. DOI:10.1111/lam.2011.52.issue-6 |
| [13] | Amann A, Costello BPDL, Miekisch W, et al. The human volatilome: volatile organic compounds (VOCs) in exhaled breath, skin emanations, urine, feces and saliva[J]. Journal of Breath Research 2014, 8(3) : 034001. DOI:10.1088/1752-7155/8/3/034001 |
| [14] | Maswadi SM, Glickman RD, Barsalou N, et al. Investigation of photoacoustic spectroscopy for biomolecular detection[J]. Proceedings of SPIE 2006, 6138(61380) : 1605–7422. |
| [15] | Priya M, Rao BSS, Ray S, et al. Photoacoustic spectroscopy in the monitoring of breast tumor development: A pre-clinical study[J]. Proceedings of SPIE 2014, 8943(894347) : 1–5. |
| [16] | van Belkum A, Durand G, Peyret M, et al. Rapid clinical bacteriology and its future impact[J]. Annals of Laboratory Medicine 2013, 33(1) : 14–27. DOI:10.3343/alm.2013.33.1.14 |
| [17] | Kunze N, G pel J, Kuhns M, et al. Detection and validation of volatile metabolic patterns over different strains of two human pathogenic bacteria during their growth in a complex medium using multi-capillary column-ion mobility spectrometry (MCC-IMS)[J]. Applied Microbiology Biotechnology 2013, 97(8) : 3665–3676. DOI:10.1007/s00253-013-4762-8 |
| [18] | Maddula S, Blank LM, Schmid A, et al. Detection of volatile metabolites of Escherichia coli by multi capillary column coupled ion mobility spectrometry[J]. Analytical and Bioanalytical Chemistry 2009, 394(3) : 791–800. DOI:10.1007/s00216-009-2758-0 |
| [19] | Li XM. Detection of volatile organic compounds emitted by some bacteria and fungi[D]. Hangzhou: Master's Thesis of Zhejiang University, 2012 (in Chinese) 李绚梅.部分细菌和真菌特征性挥发性有机物的研究[D].杭州:浙江大学硕士学位论文, 2012 http://cdmd.cnki.com.cn/Article/CDMD-10335-1012369669.htm |
| [20] | Pan ZF, Tang ZL, Xia YF. Application of photoacoustic spectroscopy technology in the field of modern medicine[J]. Experiment Science and Technology 2009, 7(3) : 33–34, 64. (in Chinese) 潘志方, 唐志列, 夏云飞. 光声光谱技术在现代医学领域的应用[J]. 实验科学与技术 2009, 7(3) : 33–34, 64. |
| [21] | Wang WJ, Zhu YB. The development and applications of the photoacoustic spectral technology in the field of biological and medical science[J]. Acta Laser Biology Sinica 1997, 6(1) : 1024–1029. (in Chinese) 王维江, 朱延彬. 光声光谱技术在生物医学领域的发展与应用[J]. 激光生物学报 1997, 6(1) : 1024–1029. |
| [22] | Li XG, Zhang DW, Liu ZY, et al. Materials science: share corrosion data[J]. Nature 2015, 527(7579) : 441–442. DOI:10.1038/527441a |
 2016, Vol. 43
2016, Vol. 43