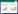扩展功能
文章信息
- 陈伟, 王小利, 付薇, 曾庆飞, 陈莹, 舒健虹
- CHEN Wei, WANG Xiao-Li, FU Wei, ENG Qing-Fei, CHEN Ying, SHU Jian-Hon
- 黑麦草根际产铁载体细菌HMGY6B的筛选鉴定及对病原菌的拮抗作用
- Screening,identification and antagonistic against the pathogens of a siderophore-producing bacteria HMGY6B from rhizosphere of ryegrass
- 微生物学通报, 2016, 43(10): 2207-2215
- Microbiology China, 2016, 43(10): 2207-2215
- DOI: 10.13344/j.microbiol.china.150871
-
文章历史
- 收稿日期: 2015-11-03
- 接受日期: 2016-02-24
- 优先数字出版日期(www.cnki.net): 2016-02-29
铁载体是包括细菌和真菌在内的,几乎所有好氧和兼性厌氧的微生物在铁胁迫条件下向环境分泌的对Fe3+具有极高亲和力的小分子量铁螯合物,这些化合物所起的作用是帮助微生物从环境中获取必需的铁元素[1]。在铁缺乏时,微生物在体内产生特异的铁载体,它可以与Fe3+形成紧密的可溶复合物;同时在革兰氏阴性菌(G-)的细胞外膜上产生受体蛋白,即铁受体蛋白,它可以特异识别Fe3+载体,将Fe3+运输到细胞内[2]。当铁元素供给充足时,铁载体和外膜上受体蛋白的合成将被关闭。现在的一些研究表明,铁载体不光对微生物的铁营养至关重要,而且它在根际促生细菌(PGPR)抑制土壤病害过程中发挥着重要作用[3-5],另外,铁载体还在某些动植物病原菌的致病性等诸多方面起着作用[6]。这些具有铁载体合成能力的微生物通过竞争铁营养,不仅能够改善自身的营养状况,还能够供给植物铁营养或通过与植物病原菌竞争铁营养达到生物防治的作用[7]。
目前,国内外对铁载体合成细菌的研究主要集中在玉米、水稻、小麦、棉花、香蕉、桃树等植物上[8-10],利用产铁载体细菌提高牧草根际及周围土壤Fe3+利用率的研究鲜见报道。据调查,贵州除黔东南州8个县以外,全省其余各县都有大面积石灰土分布,由于石灰性土壤自身碱性反应及氧化作用,使铁形成难溶性化合物而降低其生物学有效性。因此,贵州大部分地区的植物都存在着潜在性缺铁。本研究以贵州适生牧草多年生黑麦草为试验材料,采用刃天青(Chrome azural S,CAS)检测体系、OD630方法、PDA平板,结合形态、生理生化特征、16S rRNA基因全序列分析、病菌生长抑制试验筛选鉴定出铁载体合成能力强、抗病效果好的菌株,为提高贵州石灰性土壤中铁的利用效率,改善植物铁营养状况提供理论依据,也为今后复合型抗病生物菌肥的开发研制提供科学依据。
1 材料与方法 1.1 试验材料1.1.1 菌株采集:2014年9月,分别在威宁(海拔2100 m,年降雨量950 mm)、晴隆(海拔1 927 m,年降雨量1 350 mm)、兴仁(海拔1 963 m,年降雨量1 320.5 mm)、望谟(海拔896 m,年降雨量1 222.5 mm)、独山(海拔970 m,年降雨量1 346.3 mm)、贵阳(海拔1 056 m,年降雨量1 124 mm) 6个牧草试验地中,选取长势较为旺盛的多年生黑麦草植株,去除表层土壤和杂物,采集其土层深度15 cm的根际土样,去除根系上附着的大土粒,用无菌的毛刷将根上粘着的细土扫落到无菌袋后封口,贴上标签,然后将土样用冰盒迅速带回实验室进行根际土壤细菌的分离。
1.1.2 培养基及铁载体检测液:(1) LB培养基[11];(2) MKB液体培养基[5];(3) SA液体培养基(g/L)[6]:蔗糖20.0、L-天门冬酰胺2.0、K2HPO4 0.5、MgSO4·7H2O 0.5,8-羟基喹啉除铁后,无外加铁离子,其本底铁离子浓度约为0.16 μmol/L,pH 7.0;(4) 铁载体检测染液[12]:将0.079 g CAS溶于50 mL去离子水中,再加入10 mL 1 mmol/L FeCl3溶液(含12 mmol/L HCl),溶液A。将0.069 g十六烷基三甲基溴化铵(HDTMA)溶于40 mL的去离子水中,得溶液B。将A溶液沿烧杯壁缓缓加入B溶液中,搅拌混匀即得100 mL CAS蓝色检测液;(5) 0.1 mol/L磷酸盐缓冲液(pH 6.8)[11]:每100 mL含Na2HPO4·12H2O 2.427 g,NaH2PO4·2H2O 0.590 5 g,KH2PO4 0.075 g,NH4Cl 0.250 g,NaCl 0.125 g,使用时稀释10倍;(6) CAS培养基[12]:每1 L含20%蔗糖溶液10 mL,10%酸水解酪素30 mL,1 mmol/L CaCl2 1 000 μL,1 mmol/L MgSO4 20 mL,琼脂18 g,在约60 ℃时缓慢加入磷酸盐缓冲液和CAS检测染液各50 mL;(7) PDA培养基[11]。
1.1.3 病原真菌:水稻纹枯病菌(Rhizoctonia solani strain GZCC14-0001)、黄瓜灰霉病菌(Botrytis cinerea strain GZCC-0002)、黄瓜立枯丝核病菌(Rhizoctonia solani strain AS17)由贵州省植物保护研究所提供。
1.2 试验方法1.2.1 黑麦草根际产铁载体细菌分离纯化与定性检测:称取鲜土样10 g溶于100 mL灭菌的去离子水中,28 ℃、145 r/min培养30 min后进行稀释。吸取上清液50 μl均匀涂抹在CAS平板上,置于28 ℃培养箱培养48 h。菌落表面比较光滑,菌落大而粘稠的菌落接种在CAS检测平板上进行纯化与鉴定,纯培养物保存在LB斜面和甘油管以备菌种鉴定。将细菌纯培养物接种到CAS检测平板上,28 ℃培养48 h,经过培养的CAS检测平板上,分泌铁载体的细菌菌落周围会出现明显的橙黄色晕圈,记录橙黄色晕圈产生的时间、大小、颜色、形态特征。同时,通过计算晕圈比例即可溶性指数[13],对其分泌铁载体能力进行比较分析,以定性筛选铁载体能力强的菌株。
1.2.2 黑麦草根际产铁载体细菌定量检测:挑取晕圈比较明显的菌落,接种于MKB液体培养基中培养,28 ℃、150 r/min振荡培养36 h,然后将菌悬液8 000 r/min离心15 min后,得到上清液,分别取上清液3 mL与CAS检测液3 mL充分混匀,静置1 h后采用721型分光光度计在630 nm波长处测定吸光值(As),并取双蒸水作对照调零,另取3 mL CAS检测液与3 mL未接种的MKB液体培养基充分混匀,同上测定吸光值即为参比值(Ar),计算铁载体活性单位,即:[(Ar-As)/Ar]×100[14]。
1.2.3 产铁载体细菌的鉴定:(1) 菌落形态观察:挑取纯化后的单菌落,四分体划线接种到LB平板培养基上,37 ℃培养48 h,进行菌落形态观察和电镜扫描;(2) 生理生化学试验:采用吲哚试验、V-P试验、H2S试验、精氨酸、双水解、明胶液化等对分离出的产铁载体细菌进行相应的生理生化检测[15];(3) 16S rRNA基因序列分析:采用16S rRNA基因扩增通用引物27F/1495R,以菌株总RNA为模板进行扩增[16],测得的序列与GenBank中已有的16S rRNA基因序列进行相似性比对,用Mega 2法构建系统进化树。
1.2.4 铁载体制备:G-229-21T铁载体的制备参照Risse的方法[17],略有改进:先用活化的XAD-2大孔径树脂吸附按1.2.2方法制备的无菌铁载体上清液(1.1 cm×80 cm玻璃层析柱),再用2倍柱体的ddH2O洗涤除去未被吸附的杂质和其它非铁载体物质,再用4倍柱体积的H2O/CH3OH (1:1,体积比)洗脱到流出的洗脱液无色为止,分段回收,合并CAS检测阳性洗脱液,旋转蒸发除去甲醇和水,将得到的铁载体溶解在ddH2O中,0.22 μm滤膜过滤除菌,4 ℃保存备用。
1.2.5 铁载体类型检测:(1) 异羟肟酸型铁载体[18]:FeCl3 试验:在3 mL离心分离细菌的铁载体溶液中加入1-5 mL 2%的FeCl3,若用紫外可见分光光度计测得在420-450 nm之间有吸收峰,则说明产生的是异羟肟酸型铁载体。四唑试验:在少量四唑盐中加入1-2滴2 mol/L NaOH和1 mL制备的3 mg/L的铁载体溶液中,若立即呈现深红色则说明有异羟肟酸型铁载体的存在。(2) 儿茶酚型铁载体[18]:Arnow’s试验:在1 mL上述制备的3 mg/L的铁载体溶液中加入0.1 mL 5 mol/L HCl,0.5 mL反应液(50 mL水中溶解NaNO2和Na2MoO4·2H2O各10 g),待反应液变成黄色后加入0.1 mL 10 mol/L NaOH (将出现红色)并补足蒸馏水至5 mL。515 nm处将有吸收峰。(3) 羧酸型铁载体[18]:在1 mL上述制备的3 mg/L的铁载体溶液中加入1 mL 250 μmol/L CuSO4和2 mL pH 4.0的醋酸盐缓冲液。波长扫描看形成的复合物在190-280 nm波长范围内是否有相应的吸收峰。
1.2.6 黑麦草根际产铁载体分泌曲线测定:将筛选得到的菌株以1%的接种量接种于MKB培养液中,28 ℃、150 r/min振荡培养,分别于2、4、6、8、10、12、14、16、18、20、22、24、36、48、60、72 h取样,紫外分光光度计检测OD600,同时按照1.2.2步骤检测样品As/Ar (OD630),绘制菌株生长曲线及铁载体分泌曲线图[9]。
1.2.7 产铁载体细菌对病原真菌生长抑制作用:采用PDA平板对峙法,将检测筛选出的铁载体产生菌株与水稻纹枯病、黄瓜灰霉病、黄瓜立枯丝核菌同时接种在PDA平板,25 ℃培养6 d,观察铁载体细菌与真菌拮抗效果[19-20]。将培养7 d的病菌用无菌水配制成孢子悬液(106 mg/L)。取孢子悬液1 mL分别接种到含不同浓度FeCl3 (0.16、2、5、10、50和100 μmol/L)和外加铁载体(0、4、8、12 mg/L)的99 mL SA液体培养基中,150 r/min、28 ℃振荡培养7 d,收获菌丝体,60 ℃烘至恒重后称重测定生长量[21]。
2 结果与分析 2.1 黑麦草根际铁载体细菌分离纯化与定性检测CAS培养基培养48 h后,部分细菌周围出现明显橙黄色晕圈,依据细菌形态、颜色、大小,挑选出64株菌株,继续接种于CAS培养基,经过连续4代培养后,得到9株产铁载体能力较强的菌株(图 1),9份菌株第3天菌落直径大小约1.03-1.43 cm、颜色乳白或淡粉色,可溶性指数1.76-4.13 (表 1)。可溶性指数由大到小依次为HMGY6B (贵阳)>HMDS4B (独山)>HBGY4B (贵阳)>HMXR2D (兴仁)>HMWN1B (威宁)>HMDS2D (独山)>HMDS2A(独山)>HMWN3B(威宁)> HMWN4C (望谟)。
|
| 图 1 菌株HMGY6B 纯化与CAS 检测筛选 Figure 1 Purification and chrome azural S (CAS) assay of the siderophore-producing bacterium HMGY6B |
|
|
| 采集地 Collection site | 菌株编号 Screening number | 菌落直径 Colony diameter (cm) | 菌落+晕圈直径 Colony and halo diameter (cm) | 可溶性指数 Soluble index |
| 威宁 Weining | HMWN1B | 1.17 | 3.45 | 2.95 |
| HMWN3B | 1.29 | 2.68 | 2.08 | |
| 兴仁 xinren | HMXR2D | 1.31 | 4.50 | 3.44 |
| 望谟 Wangmo | HMWN4C | 1.27 | 2.24 | 1.76 |
| 贵阳 Guiyang | HMGY4B | 1.43 | 5.01 | 3.50 |
| HMGY6B | 1.31 | 5.41 | 4.13 | |
| 独山Dushan | HMDS2A | 1.37 | 3.22 | 2.35 |
| HMDS2D | 1.20 | 3.13 | 2.61 | |
| HMDS4B | 1.03 | 3.99 | 3.87 |
在MKB培养基中培养36 h检测9份菌株铁载体产生能力,检测结果如表 2所示。CAS 检测液的吸收值在不同pH条件下极易产生偏差,而且细菌培养液样品pH变化较大,所测数据值有偏差,该种检测方法对铁载体的定量可以通过As/Ar值的降低来衡量,如表 2所示HMGY6B菌株的As/Ar值最低,约0.23,铁载体活性单位(Ar-As)/Ar较高达77%,依据Manjanatha等[22]对细菌产铁载体能力划分,As/Ar从0-1.0之间以0.2为间隔,每减少0.2增加一个+,该菌株分泌铁载体的能力为++++,由此表明HMGY6B为一株产铁载体能力很强的菌株。
| 采集地 Collection site | 菌株编号 Screening number | As | Ar | (Ar-As)/Ar | As/Ar |
| 威宁 Weining | HMWN1B | 0.156 | 0.443 | 0.648 | 0.35 |
| HMWN3B | 0.187 | 0.443 | 0.578 | 0.42 | |
| 兴仁 Xinren | HMXR2D | 0.167 | 0.443 | 0.623 | 0.38 |
| 望谟 wangmo | HMWN4C | 0.201 | 0.443 | 0.546 | 0.45 |
| 贵阳 Guiyang | HMGY4B | 0.142 | 0.443 | 0.679 | 0.32 |
| HMGY6B | 0.101 | 0.443 | 0.772 | 0.23 | |
| 独山 Dushan | HMDS2A | 0.184 | 0.443 | 0.585 | 0.42 |
| HMDS2D | 0.189 | 0.443 | 0.573 | 0.43 | |
| HMDS4B | 0.139 | 0.443 | 0.686 | 0.31 |
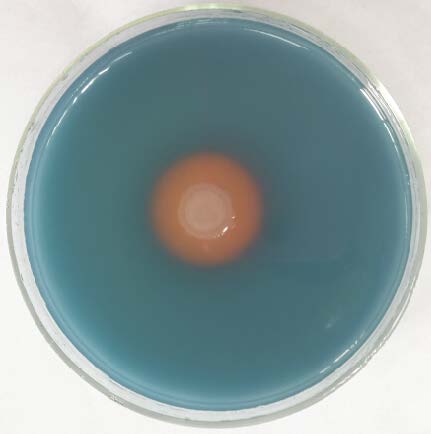
2.3.1 菌株的形态及生理生化特征:在CAS培养基上,菌株HMGY6B菌落较小、淡粉色、表面光滑不透明、边缘整齐、中部略微凸起。HMGY6B革兰氏染色阴性,近椭圆形的短杆状,短径0.5 μm-1.0 μm,长径1 μm-2 μm,具端鞭毛,运动,不产芽孢(图 2)。最适生长温度为28-32 ℃,在4 ℃仍然可以生长,而41 ℃无法生长,最适生长pH为6.8-7.5,pH 9.0时仍然可以生长,pH值小于3.0不能生长。接触酶阳性,氧化酶阳性,明胶液化阴性(表 3),生理生化学特征与假单胞菌属恶臭假单胞菌较为一致。
|
| 图 2 HMGY6B 在扫描电镜下的形态特征(8 000×) Figure 2 The morphological character of strain HMGY6B under the trans-electron microscope (8 000×) |
|
|
| 生理生化特征 physiological and biochemical characteristics | 结果 result |
| 厌氧生长Anaerobic growth | - |
| 葡萄糖氧化发酵Glucose oxidative ferment | - |
| 接触酶Contact enzyme | + |
| 赖氨酸脱酸酶Lysine decarboxylase | - |
| 精氨酸双水解酶Arginine dihydrolase | + |
| 果糖Fructose | + |
| 淀粉水解Starch hydrolysis | - |
| 明胶液化Gelatin liquefaction | - |
| 硫化氢Hydrogen sulfide | - |
| D-葡萄糖D-glucose | + |
| 反硝化作用Denitrification | - |
| 氧化酶Oxidase | + |
| 荧光色素Fluorochrome | - |
| V-P | - |
| 鸟氨酸脱羧酶Ornithine decarboxylase | - |
| 硝酸盐还原Nitrate reduction | + |
| 脓青素Pyocyanine | - |
| 脲酶Urease | - |
| 邻硝基苯酚β-半乳糖苷ONPG | - |
| 精氨酸脱羧酶Arginine decarboxylase | - |
| 甲基红Methyl red | - |
| 注:+:阳性;-:阴性. Note: +: positive reaction; -: negative reaction. | |
2.3.2 菌株HMGY6B的16S rRNA基因序列分析::以HMGY6B菌株总RNA为模版,对其16S rRNA全基因进行测序,得到总长为1 501 bp的16S rRNA基因序列。将HMGY6B的16S rRNA基因序列在BLAST中进行对比,发现HMGY6B与假单胞菌多个不同种相似度均在99%以上。根据16S rRNA基因序列构建的HMGY6B的系统发育树(图 3),结果显示分离菌株HMGY6B与P. putida strain AS90 (AY622320)和P. putida M35 (KC934869)两者最为相近,相似性分别高达99.8%和99.7%,但并未与恶臭假单胞菌Pseudomonas putida其他菌株聚在同一大类,聚类较远,与P. putida strain OK-St (EU439425)相似性为99%,而与P. putida zol-13 (JQ968690)聚类较远,相似性仅为98.1%,相反与P. sp. 4062 (JX566603)和P. sp. 4063 (JX566604)聚类较近,相似性达99.6%。尽管HMGY6B生理生化特征鉴定与恶臭假单胞菌表现较为一致,但因聚类分析中还有其他种类菌株,因此仅将其鉴定为假单胞菌属菌株,具体分类地位有待进一步的明确。

|
| 图 3 菌株HMGY6B 的系统进化树 Figure 3 A Neighbor-Joining bootstrap consensus tree based on 16S rRNA gene sequences of isolate HMGY6B 注:标尺0.1 表示序列差异的分支长度;发育树节点的数值表示Bootstrap 值;括号内数值为GenBank 数据库的登录号. Note: Bar 0.1 nucleotide divergence. Numbers at note present bootstrap percentages. Those in parentheses are GenBank accession number. |
|
|
在3 mL离心分离细菌的铁载体溶液中加入0.1 mL 5 mol/L HCl,0.5 mL反应液(50 mL水中溶解NaNO2和Na2MoO4·2H2O各10 g),溶液呈现黄色,加入0.1 mL 10 mol/L NaOH,在510 nm波长处扫描,发现有吸收峰出现,表明菌株HMGY6B所分泌的铁载体含有儿茶酚型铁载体。但异羟肟酸型铁载体和羧酸型铁载体未检测出。
2.5 菌株HMGY6B生长及产铁载体分泌规律HMGY6B对数生长时期主要在8-24 h,这一时期菌株生长速度明显增快,铁载体分泌量快速增加,As/Ar值持续下降,12-14 h左右降到最低(As/Ar=0.23,++++)。随着菌体逐渐成熟及细菌数量的增加,对数生长后期As/Ar值缓慢上升,但仍维持在0.3左右。36 h之后细菌生长趋于稳定,此时As/Ar值基本维持在0.3-0.4之间(图 4)。

|
| 图 4 菌株HMGY6B 生长曲线及铁载体分泌曲线图 Figure 4 Growth curve and siderophore-producing curve of strain HMGY6B |
|
|
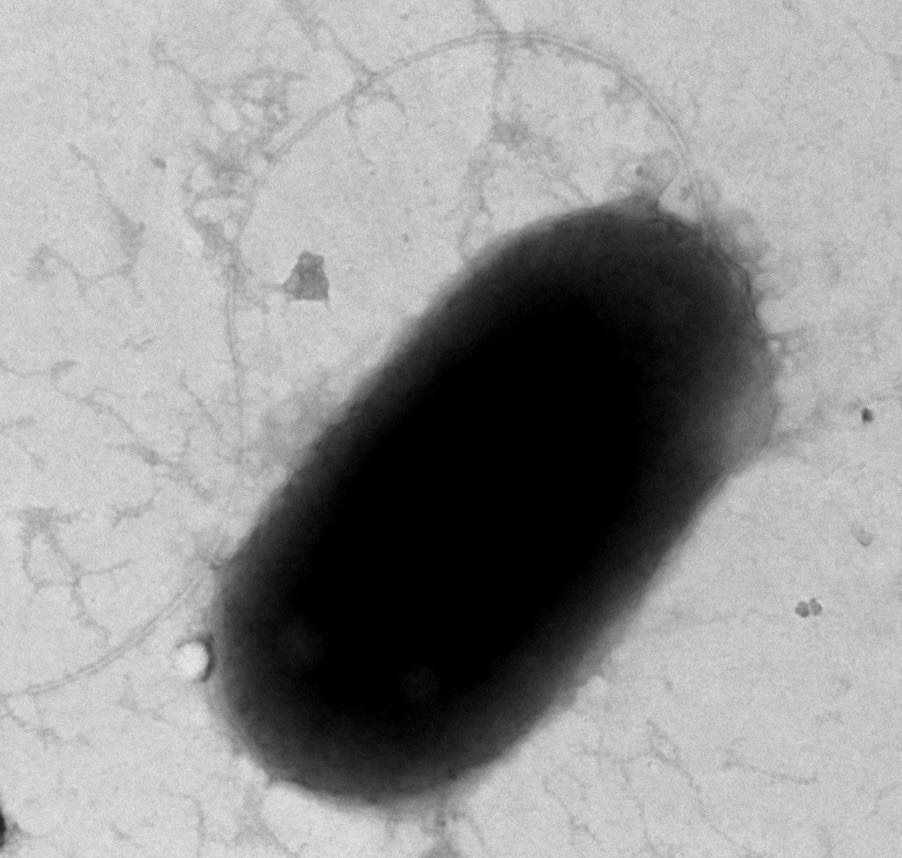
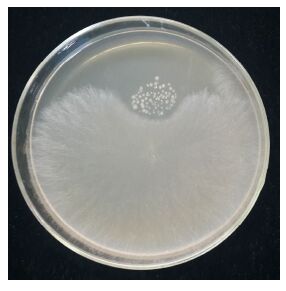
在平板对峙拮抗试验中,菌株HMGY6B被水稻纹枯病、黄瓜立枯丝核菌不同程度覆盖,但对黄瓜灰霉病有较好的拮抗作用,由此初步筛选出一株产生高亲和力铁载体且拮抗黄瓜灰霉病的细菌HMGY6B (图 5)。黄瓜灰霉病菌的生长与铁离子浓度有很大的相关性,当FeCl3浓度为0.16、2、5、10、50和100 μmol/L时,黄瓜灰霉病菌生长量抑制率分别为71.2%、57.8%、46.3%、35.6%、18.3%和3.2%,结果显示随着铁离子浓度的增加,对灰霉病抑菌作用逐渐减弱,铁离子浓度为50 μmol/L时抑制率为21.66%,100 μmol/L时抑制率仅为4.28%,对黄瓜灰霉病几乎没有抑制作用。在低铁条件下(0.16、2、5、10 μmol/L),添加铁载体对黄瓜灰霉病有十分显著的抑制作用,铁载体浓度越高抑制效果越加明显,当铁载体浓度为12 mg/L时,4种低铁条件下黄瓜灰霉病抑制率分别为91.2%、87.3%、84.6%、80.2%,随着铁离子浓度的增加,对黄瓜灰霉病的抑制作用显著降低,50 μmol/L FeCl3时抑制率下降至30.2%,100 μmol/L FeCl3浓时抑制率仅为5.5%,对黄瓜灰霉病基本没有抑制作用(图 6)。
|
| 图 5 菌株HMGY6B 对黄瓜灰霉病菌的拮抗作用 Figure 5 Antagonism against the cucumber gray mold (Botrytis cinerea) of strain HMGY6B |
|
|

|
| 图 6 菌株HMGY6B 对黄瓜灰霉病的抑制作用 Figure 6 Antagonisation of siderophore produced by isolate HMGY6B against cucumber gray mold (Botrytis cinerea) 注:每个处理3 次重复;柱状图上不同小写字母代表在0.05 水平上差异显著. Note: Experiments were repeated three times. Columns with different letters indicate significant differences at P<0.05. |
|
|
本研究从多年生黑麦草根际土壤里筛选得到一株对黄瓜灰霉病有明显拮抗作用的铁载体产生细菌HMGY6B。通过分离纯化、定性定量检测、菌落形态、生理生化、16S rRNA基因序列分析,对HMGY6B进行了系统鉴定。将HMGY6B的16S rRNA基因序列在BLAST中进行对比,发现HMGY6B与P. putida strain AS90相似性高达99.8%,其生理生化特征与恶臭假单胞菌 Pseudomonas putida最相似,但因聚类分析中并未与全部Pseudomonas putida菌株聚在一起,中间还有其他种类菌株,因此仅能将其鉴定为假单胞菌属菌株,具体分类地位有待进一步的鉴定。分析该种情况存在的原因,很有可能是GenBank数据库中不规范16S rRNA基因序列的存在[23],一定程度上影响了BLAST比对结果的可信度。
通过SA液体培养基限铁实验,研究了6种不同铁离子浓度下,不同铁载体添加量对黄瓜灰霉病的生长抑制实验,结果表明,在低铁条件下,黄瓜灰霉病菌的生长与铁载体浓度有很大的相关性,铁载体浓度越高抑制效果越明显,这与田方等[21]研究结果相一致,其发现一株产羧酸型铁载体细菌,在低铁条件下(0.16-10.00 μmol/L FeCl3)对烟草疫霉的抑制率达92.3%以上,而在富铁条件下(100 μmol/L FeCl3)抑制率仅为2.0%。推断HMGY6B对黄瓜灰霉病的拮抗机理,可能是HMGY6B菌株通过产生超强螯合能力的铁载体,从而螯合了环境中痕量的铁供自身代谢利用,黄瓜灰霉病菌自身无法产生铁载体或产生的铁载体螯合铁的能力没有HMGY6B菌株铁螯合能力强,加之黄瓜灰霉病菌本身无法吸收利用HMGY6B菌株产生的铁载体,因而在拮抗实验中被HMGY6B菌株所抑制。研究表明,利用微生物铁载体还可防治植物在石灰性土壤上的缺铁黄化,Jurkevitch等[24]利用假单胞菌Pseudomonas sp.合成的铁载体,使双子叶植物花生的缺铁黄化在石灰性土壤上得以改善,进一步表明石灰性土壤上双子叶植物的缺铁失绿症状能够通过微生物分泌的铁载体缓解。Yehuda等[25]研究也发现,缺铁黄花的植物通过添加少根根霉菌Rhizopus arrhizus分泌的铁载体,螯合铁离子后逐渐恢复正常生长。有关HMGY6B菌株对贵州植物缺铁黄化防治和石灰性缺铁土壤真菌病害的盆栽试验以及菌株自身的生防安全性正在进行当中,作者将对有关的研究结果作进一步报道。
本研究还利用XAD-2大孔径树脂吸附层析法获得了HMGY6B菌株产生的铁载体,通过FeCl3试验、Arnow’s试验、CuSO4实验检测了其铁载体类型,明确了其主要的功能基团为儿茶酚型铁载体,儿茶酚型铁载体主要是一些2,3-二羟基苯甲酸(2,3-DHBA)的简单衍生物,它们主要特征是有1-3个氨基酸连接于2,3-DHBA的羧基上[26],其铁载体的详细结构将在今后的研究中通过RP-HPLC等分析仪器进一步明确。研究发现,一些细菌能分泌不止一种类型铁载体,赵翔等[13]用反向高效液相色谱检测无铁环境和高铁环境下培养液上清,比较发现铁载体细菌上清含有3种含儿茶酚胺类基团铁载体,其中包括荧光和非荧光性的脓菌素,200 μmol/L Fe2+可完全抑制荧光性质脓菌素的分泌,而非荧光性质脓菌素则不能被完全抑制,铁载体的组成型随着培养条件的变化发生了变化。
| [1] | Haas D, Défago G. Biological control of soil-borne pathogens by fluorescent Pseudomonads[J]. Nature Reviews Microbiology , 2005, 3 (4) : 307–319. DOI:10.1038/nrmicro1129 |
| [2] | Taghavi S, van der Lelie D, Hoffman A, et al. Genome sequence of the plant growth promoting endophytic bacterium Enterobacter sp[J]. PLoS Genetics , 2010, 6 (5) : e1000943. DOI:10.1371/journal.pgen.1000943 |
| [3] | Catara V. Pseudomonas corrugata: plant pathogen and/or biological resource?[J]. Molecular Plant Pathology , 2007, 8 (3) : 233–244. DOI:10.1111/mpp.2007.8.issue-3 |
| [4] | Lodewyckx C, Vangronsveld J, Porteous F, et al. Endophytic bacteria and their potential applications[J]. Critical Reviews in Plant Sciences , 2002, 21 (6) : 583–606. DOI:10.1080/0735-260291044377 |
| [5] | Xie XJ, Wang JG. Study on effect factor of the production of catechol-type siderophores secreted by a strain of soil bacteria[J]. Microbiology China , 2006, 33 (1) : 105–109. (in chinese) 谢小军, 王敬国. 一株细菌儿茶酚型铁载体分泌的影响因素研究[J]. 微生物学通报 , 2006, 33 (1) : 105–109. |
| [6] | Manninen M, Mattila-Sandholm T. Mmethods for the detection Pseudomonas siderophores[J]. Journal Microbiological Methods , 1994, 19 (3) : 223–234. DOI:10.1016/0167-7012(94)90073-6 |
| [7] | Barzanti R, Ozino F, Bazzicalupo M, et al. Isolation and characterization of endophytic bacteria from the nickel hyperaccumulator plant Alyssum bertolonii[J]. Microbial Ecology , 2007, 53 (2) : 306–316. DOI:10.1007/s00248-006-9164-3 |
| [8] | Zhu PL, Du BH, Ding YQ, et al. Genetic diversity and phylogeny of siderophore producing bacteria isolated from cotton rhizosphere in China’s Xinjiang[J]. Scientia Agricultura Sinica , 2009, 42 (5) : 1568–1574. (in chinese) 朱彭玲, 杜秉海, 丁延芹, 等. 新疆棉花根际土壤铁载体产生菌的遗传多样性及系统发育研究[J]. 中国农业科学 , 2009, 42 (5) : 1568–1574. |
| [9] | He M, Huang Y, Wang J, et al. Isolation,characterization and mutation breeding of siderophore-producing bacterium MX-26 of peach rhizosphere[J]. Acta Phytophylacica Sinica , 2011, 38 (5) : 432–436. (in chinese) 何苗, 黄云, 王靖, 等. 桃树根际铁载体产生菌MX-26的分离鉴定及诱变选育[J]. 植物保护学报 , 2011, 38 (5) : 432–436. |
| [10] | Yu SF, Ding YQ, Yao LT, et al. Isolation and identification of siderophores producting bacteria E19 from cotton rhizosphere[J]. Biotechnology , 2007, 17 (6) : 19–21. (in chinese) 于素芳, 丁延芹, 姚良同, 等. 一株棉花根际铁载体产生菌E19的分离鉴定[J]. 生物技术 , 2007, 17 (6) : 19–21. |
| [11] | Fang ZD. 植病研究方法[M]. 北京: 中国农业出版社, 1998: 41 -50. |
| [12] | Schwyn B, Neilands JB. Universal chemical assay for the detection and determination of siderophores[J]. Analytical Biochemistry , 1987, 160 (1) : 47–56. DOI:10.1016/0003-2697(87)90612-9 |
| [13] | Zhao X, Chen SX, Xie ZX, et al. Isolation,identification and over-siderophores production of Pseudomonas fluorescens sp-f[J]. Acta Microbiologica Sinica , 2006, 46 (5) : 691–695. (in chinese) 赵翔, 陈绍兴, 谢志雄, 等. 高产铁载体荧光假单胞菌Pseudomonas fluorescens sp-f的筛选鉴定及其铁载体特性研究[J]. 微生物学报 , 2006, 46 (5) : 691–695. |
| [14] | Machuca A, Milagres AMF. Use of CAS-agar plate modified to study the effect of different variables on the siderophore production by Aspergillus[J]. Letters in Applied Microbiology , 2003, 36 (3) : 177–181. DOI:10.1046/j.1472-765X.2003.01290.x |
| [15] | Xiao YH, Li J, Liu ZX, et al. Isolation,screening and identification of sidero-carrier bacteria from Huperzia serrata Rhizosphere[J]. Journal of Microbiology , 2013, 33 (2) : 63–67. (in chinese) 肖艳红, 李菁, 刘祝祥, 等. 1株蛇足石杉根际铁载体细菌的分离、筛选与鉴定[J]. 微生物学杂志 , 2013, 33 (2) : 63–67. |
| [16] | Alain B, Isabelle G, Henri M, et al. Characterization of fluorescent and nonfluorescent peptide siderophores produced by Pseudomonas syringae strains and their potential use in strain identification[J]. Applied and Environmental Microbiology , 2001, 67 (4) : 1718–1727. DOI:10.1128/AEM.67.4.1718-1727.2001 |
| [17] | Risse D, Beiderbeck H, Taraz K, et al. Corrugatin,a lipopeptide siderophore from Pseudomonas corrugata[J]. Zeitschrift für Naturforschung. C , 1998, 53 (5/6) : 295–304. |
| [18] | Baakza A, Vala AK, Dave BP, et al. A comparative study of siderophore production by fungi from marine and terrestrial habitats[J]. Journal of Experimental Marine Biology and Ecology , 2004, 311 (1) : 1–9. DOI:10.1016/j.jembe.2003.12.028 |
| [19] | Rong LY, Yao T, Zhao GQ, et al. Screening of siderophore- producing PGPR bacteria and their antagonism against the pathogens[J]. Plant Protection , 2011, 37 (1) : 59–64. (in chinese) 荣良燕, 姚拓, 赵桂琴, 等. 产铁载体PGPR菌筛选及其对病原菌的拮抗作用[J]. 植物保护 , 2011, 37 (1) : 59–64. |
| [20] | Lin TX, Tang M, Huang MY, et al. Screening and identification of a high yield sideropho-resproducing bacteria SS05 isolated from cotton soil[J]. Microbiology China , 2012, 39 (5) : 668–676. (in chinese) 林天兴, 唐梅, 黄明远, 等. 高产铁载体棉田土壤细菌SS05的筛选与鉴定[J]. 微生物学通报 , 2012, 39 (5) : 668–676. |
| [21] | Tian F, Ding YQ, Zhu H, et al. Screening,identification and antagonistic activity of a siderophore-producing bacteria G-229-21T from rhizosphere of tobacco[J]. Acta Microbiologica Sinica , 2008, 48 (5) : 631–637. (in chinese) 田方, 丁延芹, 朱辉, 等. 烟草根际铁载体产生菌G-229-21T的筛选、鉴定及拮抗机理[J]. 微生物学报 , 2008, 48 (5) : 631–637. |
| [22] | Manjanatha MG, Loynachan TE, Atherly AG. Tn5 mutagenesis of Chinese Rhizobium fred Ⅱ for siderophore overproduction[J]. Soil Biology Biochemistry , 1992, 24 (2) : 151–155. DOI:10.1016/0038-0717(92)90271-X |
| [23] | Ashelford KE, Chuzhanova NA, Fry JC, et al. At least 1 in 20 16S rRNA sequence records currently held in public repositories is estimated to contain substantial anomalies[J]. Applied and Environmental Microbiology , 2005, 71 (12) : 7724–7736. DOI:10.1128/AEM.71.12.7724-7736.2005 |
| [24] | Jurkevitch E, Chen Y, Hadar Y. Involvement of bacterial siderophores in the remedy of lime-induced chlorosis in peanut[J]. Soil Science Society of America Journal , 1988, 52 (4) : 1032–1037. DOI:10.2136/sssaj1988.03615995005200040025x |
| [25] | Yehuda Z, Shenker M, RomheldV, et al. The role of ligand exchange in the uptake of iron from microbial siderophores by gramineous plants[J]. Plant Physiology , 1996, 112 (3) : 1273–1280. DOI:10.1104/pp.112.3.1273 |
| [26] | Barton LL. Iron Chelation in Plants and Soil Microorganisms[M]. New York: Academic Press, 1993: 261 . |
 2016, Vol. 43
2016, Vol. 43