中国科学院微生物研究所、中国微生物学会主办
文章信息
- 张璐, 王云龙, 李玉林, 王继创, 于茵茵, 张恒, 张怡青, 程蕾, 张守涛
- Zhang Lu, Wang Yunlong, Li Yulin, Wang Jichuang, Yu Yinyin, Zhang Heng, Zhang Yiqing, Cheng Lei, Zhang Shoutao
- 细胞骨架蛋白4荧光免疫层析检测方法的建立
- Establishment of fluorescence immunochromatography detection for cytoskeleton-associated protein 4
- 生物工程学报, 2020, 36(6): 1216-1222
- Chinese Journal of Biotechnology, 2020, 36(6): 1216-1222
- 10.13345/j.cjb.190412
-
文章历史
- Received: September 11, 2019
- Accepted: February 17, 2020
2. 河南省生物工程技术研究中心,河南 郑州 450000;
3. 河南省职工医院,河南 郑州 450000
2. Henan Bioengineering Technology Research Center, Zhengzhou 450000, Henan, China;
3. Henan Provincial Staff Hospital, Zhengzhou 450000, Henan, China
肝癌是常见的恶性肿瘤,由于起病隐匿,早期没有症状或症状不明显,进展迅速,确诊时大多数患者已经达到局部晚期或发生远处转移,治疗困难,预后很差。我国是肝癌高发国家,慢性乙肝病毒携带者基数庞大,肝癌的早期诊断对于有效治疗和长期生存至关重要,因此早发现早治疗成为肝癌防治工作的重点与难点[1]。目前针对肝癌筛查诊断的主要方法有肝穿刺活检、电子计算机断层成像(CT)、磁共振(MRI或MR)、选择性肝动脉造影(DSA)等。此类方法虽然特异性高,但操作繁琐,对操作人员要求较高,不易被早期患者所接受[2]。
近年来血清标志物在肿瘤的辅助诊断中起着越来越重要的作用,血清AFP及其异质体是诊断肝癌的重要指标,国内常用于肝癌的普查、早期诊断、术后监测和随访。AFP对肝癌诊断的阳性率一般为60%–70%,容易引起误诊和漏诊。李双喜等[3]研究发现标志物CKAP4在肝癌组织中高表达。最新研究表明CKAP4可作为血清诊断标志物[4],朱锦舟等[5]研究表明对于早期HCC患者CKAP4特异性、敏感性均高于AFP,CKAP4可成为肝细胞癌诊断的血清肿瘤标记物。目前对于CKAP4的检测方法较少,市面上有商业化的ELISA试剂盒,本研究主要研究血清中CKAP4的检测方法的建立,以期能够实现CKAP4的快速诊断。
1 材料与方法 1.1 材料硝酸纤维素膜(CN-140)、吸水纸、玻璃纤维棉(BXM Z80)、PVC底板购自郑州宝赛生物科技公司;CKAP4参考品(抗原标定)、CKAP4单克隆抗体、多克隆抗体(兔IgG)由河南省生物工程技术研究中心提供;羊抗兔IgG购自生工生物工程(上海)股份有限公司;Eu3+羧基荧光微球购自上海溯源生物;1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDC)和N-羟基琥珀酰亚胺(NHS)购自Sigma公司;HM3030型三维划膜喷金仪、ZQ2002型微电脑自动斩切机购自上海金标生物科技有限公司;FIC-S2011-D5荧光定量分析仪购自杭州峰航科技有限公司;各类缓冲液等试剂均为国药化学纯;ELISA试剂盒购自CUSABIO公司;临床血清样本收集于郑州大学第一附属医院。
1.2 方法 1.2.1 荧光微球标记物的制备微球-抗体络合物制备:吸取40 μL荧光微球加至500 μL硼酸缓冲液(0.05 mol/L)中,分别加50 μL EDC (10 mg/mL)、NHS (10 mg/mL),混匀后超声5 min,摇床振荡活化40 min,离心后弃上清,用700 μL硼酸缓冲液(0.05 mol/L)重悬颗粒;加入60 μg CKAP4-02抗体,摇床偶联2 h,离心后弃上清,加微球保护液(0.05 mol/L Tris-HCl缓冲液,pH 8.0、1% T-20、0.2% BSA、0.5%酪蛋白、5%海藻糖、0.05%NaN3),5% BSA加30 μL摇床封闭1 h。
1.2.2 微球垫喷涂微球垫预处理:使用微球垫处理液(0.001 mol/L Tris-HCl缓冲液,pH 8.0、3%海藻糖、0.01%甘氨酸、1% T-20、0.05% NaN3)按照1.5 mL/条比例对微球垫进行预处理,37 ℃干燥2 h。
将制备好的微球-抗体络合物以5 μL/cm单位量喷涂于预处理的微球垫上,37 ℃过夜干燥。
1.2.3 包被板的制备将质控线抗体及检测线抗体喷涂与粘贴有NC膜的PVC板上,CKAP4-06抗体作为包被抗体1.5 μg/cm喷涂于T线,羊抗兔IgG 2.5 μg/cm喷涂于C线。
1.2.4 组条将样品垫、微球垫、NC膜、吸水纸按顺序粘贴于PVC底板上,切裁至4 mm试纸条。
1.2.5 检测吸取75 μL的样品沿试纸条下端2/3处进行滴加,5 min后进行检测,记录荧光定量分析仪上的T值、C值。
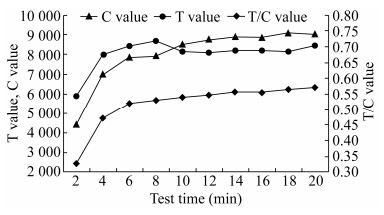
1.2.6 检测时间的确定用浓度为200 pg/mL的参考品按照现有工艺70 μL/条的加样量进行点样,取10个试纸条分别在点样后4、6、8、10、12、14、16、18、20 min检测C值、T值,计算T/C值。
1.3 性能评估 1.3.1 线性范围使用CKAP4高值线性参考品1 000 pg/mL进行倍比稀释(25、50、100、200、400、800、1 000 pg/mL)对试纸条进行检测,以参考品浓度为横坐标,T/C值为纵坐标,确定CKAP4试纸条检测范围,建立标准曲线。
1.3.2 最低检出限采用阴性参考品作为样品对试纸条进行检测,共重复检测20次,根据所测得结果的T/C值,计算相应的平均值x及标准差(s),以阴性参考品和相邻浓度线性参考品之间的浓度,进行两点拟合,得出一次线性方程,将x值带入到上述一次线性方程中,得出试纸条的最低检出限。
1.3.3 精密度检测取3个不同批次制备的试纸条分别检测3个浓度(50、200、400 pg/mL)精密性参考品,每个浓度重复检测10条,计算批内批间的精密度。
1.3.4 准确度测定通过在阴性样本中分别添加不同量的CKAP4参考品,使CKAP4浓度为50、200、400 pg/mL,采用CKAP4荧光免疫试纸条进行检测,每个浓度重复测定10次,分别计算各浓度回收率的平均值和变异系数,分析准确度。
1.3.5 特异性将高浓度的肝癌常用标志物甲胎蛋白、凝血酶原按比例分别添加至CKAP4参考品中,采用CKAP4荧光免疫层析试纸条进行检测,测定CKAP4浓度。
1.3.6 稳定性将制备好的试纸条干燥后封装,置于37 ℃进行加速破坏,使用相同浓度的参考品分别于0、1、3、5、7、14、20 d进行检测,根据加速破坏期间T值、C值、T/C值变化,分析试纸条的稳定性。
1.3.7 方法学对比采用本方法制备的试纸条以及商业化的ELISA试剂盒分别对从医院收集的87份临床血清样本进行检测,根据检测结果,得出本研究所建立的方法与商业化ELISA试剂盒的相关性。
1.3.8 临床评价采用本研究建立的CKAP4蛋白荧光免疫层析检测方法制备的试纸条检测经临床病理确诊的肝癌患者样本67份以及CKAP4阴性样本45份。
2 结果与分析 2.1 检测结果判读紫外分析仪检测结果如图 1。C线有荧光,若T线有荧光则为阳性,T线无荧光则为阴性;若C线无荧光,T线有无荧光都判定为试纸条无效或取样失败。

|
| 图 1 试纸条的判读 Fig. 1 Interpretation of test strips. |
| |
加样10 min后T/C值趋于平缓,故加样后10 min为最佳检测时间,结果见图 2。
|
| 图 2 检测时间结果 Fig. 2 Detection time results. |
| |
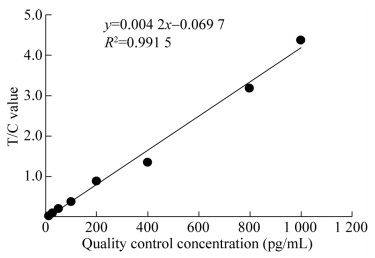
通过使用CKAP4线性参考品进行加样检测,结果如图 3所示,CKAP4在25–1 000 pg/mL线性范围内线性较好,y=0.004 2x–0.069 7,R2=0.991 5。
|
| 图 3 标准曲线的确定 Fig. 3 Determination of standard curve. |
| |
结果如表 1所示,计算20次检测结果的平均值x及标准差(s=0.004),将x+2s带入到以阴性参考品和相邻浓度线性参考品两点进行拟合得出的一次线性方程(y=1 893.94×x–41.85)中,求得本研究所建立的CKAP4蛋白检测试纸条最低检出限为15 pg/mL。
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 0.027 6 | 0.026 9 | 0.017 2 | 0.018 1 | 0.019 3 | 0.022 4 | 0.017 6 | 0.027 7 | 0.018 1 | 0.025 5 |
| 0.019 2 | 0.021 7 | 0.024 2 | 0.018 5 | 0.022 8 | 0.018 4 | 0.025 4 | 0.026 1 | 0.017 5 | 0.029 7 |
通过制备3批试纸条对3个浓度CKAP4参考品进行检测,精密性结果见表 2,批内批间变异系数均在15%以内,符合精密度要求。
| Reference concentration (pg/L) | Detection result (pg/L) | s | CV | |
| Batch 1 | 50 | 47.08 | 3.56 | 0.07 |
| 200 | 195.34 | 16.54 | 0.08 | |
| 400 | 361.14 | 38.05 | 0.10 | |
| Batch 2 | 50 | 50.67 | 5.20 | 0.10 |
| 200 | 230.97 | 23.90 | 0.10 | |
| 400 | 417.02 | 40.68 | 0.09 | |
| Batch 3 | 50 | 52.60 | 6.44 | 0.12 |
| 200 | 198.03 | 21.38 | 0.10 | |
| 400 | 441.24 | 35.65 | 0.08 | |
| Inter batch | 50 | 50.11 | 5.53 | 0.11 |
| 200 | 208.11 | 25.99 | 0.12 | |
| 400 | 408.03 | 49.83 | 0.12 |
CKAP4准确度检测结果见表 3,分别检测浓度为50、200、400 pg/mL的样本,其回收率分别为96.8%、104.71%、105.32%,符合回收率85%–115%的要求。
| High value | Median | Low value | |
| Addition concentration (pg/mL) | 400 | 200 | 50 |
| Determination of concentration (pg/mL) | 387.2±6.7 | 209.41±1.4 | 52.66±0.3 |
| Recovery rate (%) | 96.8 | 104.71 | 105.32 |
特异性检测结果见表 4,甲胎蛋白与凝血酶原均对CKAP4检测无影响,特异性较好。
| Cross-reactive substance | Theoretical concentration of CKAP4 (pg/mL) | Measured concentration of CKAP4 (pg/mL) | |
| 1 | AFP 400 µg/L | 200 | 213.47±2.6 |
| 2 | PIVKA-Ⅱ300 ug/L | 200 | 206.54±1.7 |
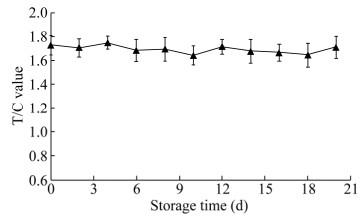
稳定性结果见图 4,37 ℃加速20 d,T/C值在1.7左右,试纸条稳定性良好。
|
| 图 4 稳定性检测结果 Fig. 4 Stability detection results. |
| |
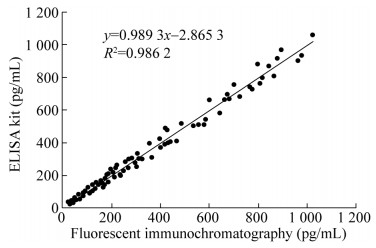
方法学比对结果见图 5,由结果可知,采用本工艺制备的试纸条商业化ELISA试剂盒相关性良好,R2=0.986 2。
|
| 图 5 方法学对比结果 Fig. 5 Methodological comparison results. |
| |
检测结果见表 5,本研究建立的CKAP4荧光免疫层析方法检测肝癌敏感性为91%,特异性到达100%。
| CKAP4 | HCC | Health | Total |
| Positive | 61 | 0 | 61 |
| Negative | 6 | 45 | 51 |
| Total | 67 | 45 | 112 |
肝癌是病死率最高的恶性肿瘤之一。我国是肝癌高发国家,肝癌发生率、死亡率较高[1]。肝癌的发生是体内多因素、多步骤的复杂过程,且当前肝癌诊断方法不易被早期患者接受,AFP作为当前临床上原发性肝癌的血清标志物,在多种肿瘤中均可表现出较高浓度,可作为多种肿瘤的阳性检测指标,其在肝癌的诊断上只有60%左右的阳性率,如果能找到相对肝癌特异的蛋白或基因,将会对研究肝癌的发病机制以及提高早期诊断有重要的意义。
近年来CKAP4成为研究的热点,CKAP4是一种可逆性棕榈酰化的Ⅱ型跨膜蛋白,最初被发现是一种主要局限于内质网(ER)的蛋白质[6]。2016年,Hirokazu等[7]研究表明细胞骨架相关蛋白4 (CKAP4)是DKK1受体,CKAP4和DKK1的结合打开封闭区域,当细胞表面膜上存在CKAP4时,DKK1可通过激活PI3K-AKT信号级联来促进细胞增殖[6]。李双喜等[3]研究发现CKAP4在肝癌组织中高表达,CKAP4在肝癌血清中浓度高于正常,在AFP < 10 ng/mL时,CKAP4作为肝癌诊断指标较AFP效能较高,有望作为评估肝癌预后的一项有前景的指标。2018年,Yanagita团队[4]制备了一种能够识别血清CKAP4的单克隆抗体,表明CKAP4是一种新的肺癌早期血清学诊断标志物。2019年,朱锦舟等[5]研究表明HCC患者的判定CKAP4与AFP无明显差异,早期患者CKAP4灵敏度、特异性更高,弥补了AFP假阳性高的缺点,提示CKAP4可作为临床实践中HCC早期筛查诊断的血清标记物。
免疫层析试纸作为快速检测领军先锋发展很快,现今国内外免疫层析试纸条技术较成熟应用最广泛的是胶体金免疫层析试纸条,主要因其操作简便、快速、特异,适用于广大基层单位并能在现场作检测和诊断,目前主要存在的问题是灵敏度相对较低,大多难以实现定量分析[8-9]。荧光免疫层析技术是结合了免疫反应和色谱层析的一项新的诊断技术,既保留了传统免疫层析技术可现场快速检测的优点,又加入了荧光检测技术灵敏度高、可定量检测的特点,近几年来成为检验学和诊断学的研究热点[10-11]。白亚龙等[12]通过探究量子点与抗体的偶联方式以及交联剂的比例表明判断灵敏度比胶体金免疫层析体系高4–20倍。Zhao等[13]通过羧基纳米颗粒与抗体偶联作为荧光探针,比已报道的酶联免疫检测方法检测限位低100倍。Wu等[14]荧光微球免疫层析检测方法的检测限更低,准确度、精确度、重现性更好。
本研究通过羧基荧光微球标记抗体建立的荧光免疫层析法对于检测CKAP4具有快速、准确、灵敏度高等优点,且试纸条检测所需设备小巧便携,通过电脑连接设备即可即时检测,检测时间仅需10 min,操作人员无需接受专业培训,单人份成本仅为ELISA的1/10,基本能够满足床旁及基层快速诊断的需求。但由于本研究检测样本数较少,后期需加大临床样本检测进行验证。
| [1] |
Wei KR, Peng XB, Liang ZH, et al. Liver cancer epidemiology worldwide. China Cancer, 2015, 24(8): 621-630 (in Chinese). 魏矿荣, 彭侠彪, 梁智恒, 等. 全球肝癌流行概况. 中国肿瘤, 2015, 24(8): 621-630. |
| [2] |
Li Z, Zhu JY. Diagnosis, management, and treatment of hepatocellular carcinoma (V2017). J Clin Hepatol, 2017, 33(8): 1419-1431 (in Chinese). 李照, 朱继业. 原发性肝癌诊疗规范(2017年版). 临床肝胆病杂志, 2017, 33(8): 1419-1431. DOI:10.3969/j.issn.1001-5256.2017.08.003 |
| [3] |
Li SX. Cytoskeleton-associated membrane protein 4 as a tumor suppressor highly expressed in hepatocellular carcinoma and predicted patients outcome after surgery resection[D]. Shanghai: Second Military Medical University, 2012 (in Chinese). 李双喜. CKAP4在肝癌中的生物学作用及机制研究[D].上海: 第二军医大学, 2012. |
| [4] |
Yanagita K, Nagashio R, Jiang SX, et al. Cytoskeleton-associated protein 4 is a novel serodiagnostic marker for lung cancer. Am J Pathol, 2018, 188(6): 1328-1333. DOI:10.1016/j.ajpath.2018.03.007 |
| [5] |
Zhu JZ, Zhang HX, Xi LT, et al. Diagnostic value of serum cytoskeleton-associated protein 4 in hepatocellular carcinoma. China J Mod Med, 2019, 29(17): 84-87 (in Chinese). 朱锦舟, 张慧娴, 奚黎婷, 等. 血清细胞骨架蛋白4检测对肝细胞癌的诊断价值. 中国现代医学志杂, 2019, 29(17): 84-87. |
| [6] |
Kikuchi A, Kimura H, Fumoto K. The Dickkopf1-CKAP4 pathway, a novel cancer signaling, represents molecular targets for cancer therapy. Cancer Sci, 2018, 109: 1071-1071. DOI:10.1111/bph.13863 |
| [7] |
Kimura H, Fumoto K, Shojima K, et al. CKAP4 is a Dickkopf1 receptor and is involved in tumor progression. J Clin Invest, 2016, 126(7): 2689-2705. DOI:10.1172/JCI84658 |
| [8] |
Li JW, Song CM, Liu F, et al. Immunochromatographic strip technology and its application in food safety detection. Food Sci, 2014, 35(8): 36-41 (in Chinese). 李建武, 宋春美, 刘芳, 等. 免疫层析试纸技术及其在食品安全检测中的应用. 食品科学, 2014, 35(8): 36-41. |
| [9] |
Zhu WC, Kong FD, Lin XM, et al. Prospect and application of immune colloidal gold technique. Biotechnol Bull, 2010(4): 81-87 (in Chinese). 朱文钏, 孔繁德, 林祥梅, 等. 免疫胶体金技术的应用及展望. 生物技术通报, 2010(4): 81-87. |
| [10] |
Hu JL, Yu DS, Liu XL, et al. Rapid detection of cefalexin residues in milk by fluorescent immunochromatography assay. Chin J Food Hyg, 2014, 26(4): 362-366 (in Chinese). 胡佳丽, 于东升, 刘小雷, 等. 荧光免疫层析法快速测定牛奶中头孢氨苄残留量. 中国食品卫生杂志, 2014, 26(4): 362-366. |
| [11] |
Shi QF. Research on key technology of preparing and quantitative detecting the immunofluorescence chromatography test strip[D]. Beijing: Beijing Institute of Technology, 2016 (in Chinese). 施青峰.荧光免疫层析试纸条制备及定量检测关键技术研究[D].北京: 北京理工大学, 2016. |
| [12] |
Bai YL. Preliminary study of a high-sensitivity immunochromatographic technique based on quantum dot fluorescent microspheres[D]. Shanghai: Shanghai Normal University, 2010 (in Chinese). 白亚龙.一种基于量子点荧光微球的高灵敏度免疫层析技术初步研究[D].上海: 上海师范大学, 2010. |
| [13] |
Zhao P, Wu YY, Zhu YH, et al. Upconversion fluorescent strip sensor for rapid determination of Vibrio anguillarum. Nanoscale, 2014, 6(7): 3804-3809. DOI:10.1039/C3NR06549A |
| [14] |
Wu CH, Hu LM, Xia J, et al. Comparison of immunochromatographic assays based on fluorescent microsphere and quantum-dot submicrobead for quantitative detection of aflatoxin M1 in milk. J Dairy Sci, 2017, 100(4): 2501-2511. DOI:10.3168/jds.2016-12065 |
 2020, Vol. 36
2020, Vol. 36




