中国科学院微生物研究所、中国微生物学会主办
文章信息
- 付妍, 张君轩, 付雪蓉, 解雨晨, 任泓宇, 刘佳, 陈修来, 刘立明
- Fu Yan, Zhang Junxuan, Fu Xuerong, Xie Yuchen, Ren Hongyu, Liu Jia, Chen Xiulai, Liu Liming
- 三酶级联催化L-苏氨酸生产L-2-氨基丁酸
- Production of L-2-aminobutyric acid from L-threonine using a trienzyme cascade
- 生物工程学报, 2020, 36(4): 782-791
- Chinese Journal of Biotechnology, 2020, 36(4): 782-791
- 10.13345/j.cjb.190256
-
文章历史
- Received: June 14, 2019
- Accepted: June 24, 2019
2. 江南大学 生物工程学院,江苏 无锡 214122;
3. 江南大学 工业生物技术教育部重点实验室,江苏 无锡 214122
2. School of Biotechnology, Jiangnan University, Wuxi 214122, Jiangsu, China;
3. Key Laboratory of Industrial Biotechnology, Ministry of Education, Jiangnan University, Wuxi 214122, Jiangsu, China
L-2-氨基丁酸(L-ABA)作为一种非天然氨基酸和重要的医药中间体,广泛应用于药物合成领域,如抑菌抗结核药物盐酸乙胺丁醇[1-2]、新型抗癫痫药物左乙拉西坦和布瓦西坦[3]等。L-ABA合成方法包括化学法和生物法。化学法主要采用酮丁酸还原法[4]、脱硫反应法[5]、卤代氨解法[6-7]、化学拆分法[8],但缺点是易形成消旋体,不利于手性化合物的合成,且反应条件严苛、环境污染严重、不易进行工业化生产。生物法因反应条件温和、立体选择性高和绿色环保等特点而广受关注,其中生物发酵法是对生产L-苏氨酸的大肠杆菌Escherichia coli进行代谢改造,在含有30 g/L葡萄糖的培养基中合成5.4 g/L的L-ABA[9]。另一方法是生物酶催化法,包括腈水解酶法、转氨酶法和氨基酸脱氢酶法等。腈水解酶法是以DL-氨基丁腈为底物,直接水解L-氨基丁腈获得L-ABA,或通过腈水合酶结合L-氨基酸酰胺酶将L-氨基丁腈转化成L-ABA[10]。转氨酶法是以2-酮丁酸(2-OBA)及提供氨基供体的L-天冬氨酸或L-谷氨酸等为底物,通过氨基转移酶或者氨基酸脱氢酶制备L-ABA,这一方法缺点是副产物草酰乙酸容易脱羧得到丙酮酸,进而生成副产物L-丙氨酸,不利于后续分离纯化[11-12]。L-氨基酸脱氢酶法是借助于中间型高温放线菌Thermoactinomyces intermedius的亮氨酸脱氢酶(LDH)将2-OBA转化为36 g/L L-ABA,产率达到88%[12]。但由于2-OBA成本高且不稳定,因此,研究人员利用苏氨酸脱氨酶(TD)将较为廉价的L-苏氨酸转化为生产2-OBA,在此基础上通过过量表达LDH和辅酶NADH再生用酶甲酸脱氢酶(FDH),高效制备L-ABA。如Tao等[13]在E. coli BL21 (DE3)中分别过表达TD、LDH、FDH,转化体系中需要同时添加3种湿菌体,采用“一锅法”在30 L转化体系中将30 mol L-苏氨酸转化为29.2 mol L-ABA,产率为97.3%。
脱氢酶法具有底物成本低廉和反应不可逆等优点,但是上述研究的催化体系中通常需要添加多种酶液,并进行酶活优化配比[12-13],增加了工艺的复杂性和生产成本,若将TD、LDH和FDH这3种酶在单一细胞中表达,可以简化生产工艺便于对反应条件进行精确调整和优化。本研究利用TD、LDH和FDH构建了体外催化L-苏氨酸生产L-ABA的级联路径,在E. coli BL21中对3种酶共表达方式进行优化,构建了重组菌株E. coli 3FT+L,实现三酶的协调稳定表达,并对转化体系进行优化,最终实现了L-ABA的高效生产。
1 材料与方法 1.1 材料 1.1.1 菌株和质粒本研究使用的质粒pET28a、pETDuet、pRSFDuet均购自Novagen公司,使用的菌株见表 1。
| Strains | Relevant characteristics | References |
| E. coli BL21(DE3) | F- ompT hsdSB (rB- mB-) gal dcm (DE3) | Novagen |
| BL21-BsTD | E. coli BL21 (DE3)(pET28a-BsilvA) | This study |
| BL21-CgTD | E. coli BL21 (DE3)(pET28a-CgilvA) | This study |
| BL21-EcTD | E. coli BL21 (DE3)(pET28a-EcilvA) | This study |
| BL21-BtLDH | E. coli BL21 (DE3)(pET28a-BtleuB) | This study |
| BL21-BsLDH | E. coli BL21 (DE3)(pET28a-BsleuB) | This study |
| BL21-BlLDH | E. coli BL21 (DE3)(pET28a-Blldh) | This study |
| BL21-MtLDH | E. coli BL21 (DE3)(pET28a-MtleuB) | This study |
| BL21-TiLDH | E. coli BL21 (DE3)(pET28a-Tildh) | This study |
| BL21-CbFDH | E. coli BL21 (DE3)(pET28a-Cbfdh) | This study |
| E. coli FT+L | E. coli BL21 (DE3) (pRSFDuet-BtleuB +pETDuet-fdh-EcilvA) | This study |
| E. coli 2FT+L | E. coli BL21 (DE3) (pRSFDuet-BtleuB +pETDuet-fdh-fdh-EcilvA) | This study |
| E. coli 3FT+L | E. coli BL21 (DE3) (pRSFDuet-BtleuB +pETDuet-fdh-fdh-fdh-EcilvA) | This study |
| E. coli 4FT+L | E. coli BL21 (DE3) (pRSFDuet-BtleuB +pETDuet-fdh-fdh-fdh-fdh-EcilvA) | This study |
分子生物学工具酶、SDS-PAGE Protein Marker、质粒提取试剂盒、胶回收试剂盒等分子生物学试剂购自TaKaRa有限公司;2-OBA和L-ABA标准品购自Sigma公司;异丙基-β-D-硫代半乳糖(IPTG)、硫酸卡那霉素(Kan)、氨苄青霉素(Amp)购自生工生物工程(上海)股份有限公司;其余常规试剂购自国药集团。
1.2 方法 1.2.1 重组菌株的构建使用特异性引物分别从不同微生物中克隆编码TD、LDH和FDH的目的基因,限制内切酶双酶切目的条带,然后连接于同样双酶切的表达载体pET28a获得重组质粒,将构建完成质粒导入E. coli BL21 (DE3)后获得基因工程菌株。
构建共表达菌株时,从苏云金芽孢杆菌Bacillus thuringiensis基因组中克隆编码LDH的基因leuB,连接于高拷贝质粒pRSFDuet,构建重组质粒pRSFDuet-BtleuB;将博伊丁假丝酵母Candida boidinii来源的fdh基因连接于pETDuet,构建重组质粒pETDuet-Cbfdh,从E. coli K12基因组中克隆编码TD的基因ilvA连接于质粒pETDuet-fdh,构建重组质粒pETDuet-fdh-EcilvA,将上述两种重组质粒导入E. coli BL21 (DE3),在含有Amp和Kan的平板上筛选阳性克隆,得到双质粒共表达菌株E. coli FT+L。
E. coli FT+L菌株中重复表达fdh基因,即在pETDuet-fdh-EcilvA质粒上分别通过一步克隆试剂盒连接不同个数的fdh基因构建质粒pETDuet- 2fdh-EcilvA、pETDuet-3fdh-EcilvA和pETDuet- 4fdh-EcilvA。
1.2.2 培养基与培养方法LB培养基:胰蛋白胨10 g/L,酵母粉5 g/L,NaCl 10 g/L,用于质粒的构建、扩增和种子液的培养。
TB培养基:甘油4 g/L,胰蛋白胨12 g/L,酵母粉24 g/L,KH2PO4 2.31 g/L,K2HPO4 12.54 g/L,用于重组菌株发酵培养。
补料培养基:甘油500 g/L,MgSO4·7H2O 30 g/L。
种子培养条件:从斜面保藏培养基中接一环菌种至25 mL LB培养基中,根据重组菌选择压力添加100 μg/mL Kan或Amp,37 ℃、200 r/min振荡培养10 h。
摇瓶培养与诱导条件:取1 mL的种子培养液接种于25 mL TB培养基中,根据重组菌选择压力添加100 mg/L Kan或Amp,37 ℃、200 r/min培养OD600至0.6时,添加100 mg/L的IPTG于25 ℃下诱导8–12 h。
发酵罐培养与诱导条件:将种子液按照5%接种量转接于发酵罐,初始发酵温度37 ℃、500 r/min下培养至OD600为12–14时,溶氧突然上升,此时开始流加补料培养基,通过补料控制溶氧水平在30%–40%,当OD600在25左右时,添加5 g/L的乳糖于25 ℃下诱导,总发酵周期24 h,发酵结束后发酵液经4 ℃离心收集菌体。
1.2.3 共表达重组菌转化条件250 mL摇瓶转化条件优化:转速为200 r/min,温度为30 ℃,根据不同条件添加不同酶活TD、LDH、FDH,不同浓度的L-苏氨酸,甲酸铵与苏氨酸摩尔浓度比为1:1,NAD+ 30 mg/L,使用20 mmol/L磷酸盐缓冲液(pH 7.5)定容至20 mL。
30 L发酵罐全细胞转化条件:搅拌转速400 r/min,通气量15 L/min,温度37 ℃,用4 mol/L NaOH溶液控制pH 8.0,湿菌体20 g/L,L-苏氨酸80 g/L,甲酸铵与苏氨酸摩尔浓度比为1:1,NAD+为30 mg/L,反应体积为15 L。
1.2.4 酶活测定单酶表达重组菌株使用冻干菌体或纯酶检测酶活。共表达菌株超声破碎细胞,离心取上清液检测粗酶液酶活。TD、LDH、FDH的酶活性测定参考文献报道[14-16]。
1.2.5 检测方法高效液相色谱法检测L-Thr、2-OBA和L-ABA浓度[13-14]。
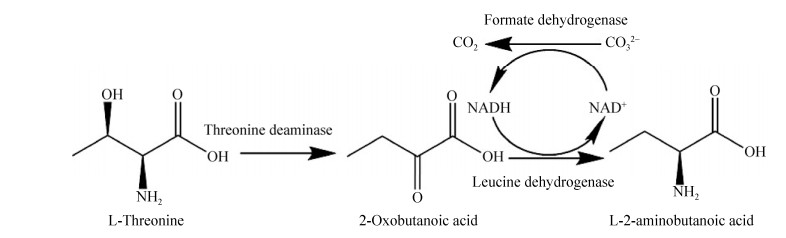
2 结果与分析 2.1 L-苏氨酸合成L-ABA的级联反应设计与体外构建如图 1所示,L-苏氨酸转化生产L-ABA的反应分为两步:第一步是利用L-苏氨酸脱氨酶(L-threonine deaminase,TD,EC 4.3.1.19)将L-苏氨酸脱去羟基和氨基转化为2-OBA;第二步反应利用亮氨酸脱氢酶(Leucine dehydrogenase, LDH, EC1.4.1.9)将2-OBA的羰基不对称还原为氨基生成L-ABA。由于第二步是氧化还原反应,需要辅酶NADH参与,因此在设计级联反应时需要偶联辅酶再生系统。
通过Brenda数据库(https://www.brenda-enzymes.org/),选取来源于枯草芽孢杆菌Bacillus subtilis、谷氨酸棒杆菌Corynebacterium glutamicum和E. coli K12的TD,因其具有较高的比酶活[17],将3种酶基因克隆表达于E. coli BL21中,构建获得重组菌株BL21-BsTD、BL21-CgTD和BL21-EcTD。摇瓶发酵14 h收集湿菌体冷冻干燥,测定不同来源的TD对L-苏氨酸活性,BL21- BsTD、BL21-CgTD和BL21-EcTD的冻干细胞对L-苏氨酸的比活力分别为2.04、3.21 U/mg、15.8 U/mg,因此选择来源于E. coli的EcTD用于第一步转化反应。采用类似的策略,将来源于B. thuringiensis、B. subtilis、地衣芽孢杆菌Bacillus licheniformis、热醋穆尔氏菌Moorella thermoacetica、T. intermedius的亮氨酸脱氢酶LDH[12, 18],分别克隆表达于E. coli BL21构建重组菌株BL21-BtLDH、BL21-BsLDH、BL21-BlLDH、BL21-MtLDH、BL21-TiLDH。摇瓶发酵14 h收集湿菌体冷冻干燥,测定不同菌株的LDH对2-OBA的酶活,其中BL21-BsLDH和BL21-BlLDH对2-OBA无催化活性,BL21-BtLDH、BL21-MtLDH和BL21-TiLDH的冻干细胞对2-OBA比活力分别为1.56、0.28、1.01 U/mg,因此选择B. thuringiensis来源的BtLDH用于第二步转化。由于C. boidinii来源的CbFDH具有广泛的工业应用潜力[19-20],因此在E. coli BL21(DE3)中表达C. boidinii来源fdh构建重组菌BL21-CbFDH,比活力为1.38 U/mg。
使用镍柱将EcTD、BtLDH和CbFDH进行蛋白质纯化(图 2A),将纯化所获得的纯酶添加到5 mL的体外转化体系中,添加10 g/L底物L-苏氨酸,采用LC-MS结构鉴定转化液中是否催化合成了L-ABA,对转化液中产物进行检测,L-ABA分子量为103.1,使用阴离子色谱检测分子量为102.05 (图 2B),证明获得目标产物L-ABA,说明采用EcTD、BtLDH和CbFDH级联催化L-苏氨酸生成L-ABA是可行的。为了获得更高的转化率,对体外转化体系的3种酶的浓度及其配比进行优化。L-苏氨酸浓度为50 g/L,固定EcTD酶活为12 U/mL,优化EcTD与BtLDH酶活比例,结果如图 2C所示,在EcTD与BtLDH酶活比为1.0:1–2.0:1时,L-ABA产量((40.7±0.2) g/L)和摩尔转化率(94.0%±0.5%)达到较高水平。固定EcTD与BtLDH酶活比为1:1 (固定LDH酶活为12 U/mL),体系中添加BtLDH与CbFDH酶活比为1:0.05–1:0.3,结果如图 2D所示。当酶活比例为1:0.2–1:0.3时,L-ABA产量达到40.0 g/L以上,当低于该比例时,L-ABA产量和摩尔转化率均下降,说明体系中FDH酶活至少达到LDH的20%及以上,才能够保证提供充足的辅酶NADH。因此确定EcTD、BtLDH和CbFDH最佳比例为1:1:0.2,此时酶添加量最低且能够保证L-苏氨酸高效转化。

|
| 图 2 体外催化TD、LDH和FDH酶活比例优化 Fig. 2 Optimization of activity ratio of EcTD/BtLDH and BtLDH/CbFDH in vitro. (A) SDS-PAGE analysis of purified protein. (B) Analysis of the product with LC-MS. (C) Effect of different activity ratios of EcTD/BtLDH on L-ABA production. (D) Effect of different activity ratios of BtLDH/CbFDH on L-ABA production. |
| |
为了进一步简化工艺,将EcTD、BtLDH和CbFDH在E. coli BL21(DE3)中共表达,使用pRSFDuet质粒连接BtleuB,质粒pETDuet将fdh与EcilvA串联表达,构建重组菌株E. coli FT+L,菌体破碎后进行蛋白电泳验证,结果如图 3A所示。EcTD、BtLDH和CbFDH理论蛋白分子量分别为56.2、39.8、40.4 kDa,目的蛋白条带大小符合预期,由于BtLDH和CbFDH蛋白分子量相近,出现重叠条带。对重组菌E. coli FT+L的催化性能进行评价,在20 mL体系中添加L-苏氨酸10– 50 g/L,底物与湿菌体质量比为2.5:1。当L-苏氨酸浓度从10增加至50 g/L时,摩尔转化率从95.0%降至45.2%,而中间产物2-OBA浓度从0.43 g/L上升至25.8 g/L (图 3B)。其原因是3种酶的酶活不均衡导致2-OBA无法持续转化为L-ABA,进一步测定湿细胞中3种酶的酶活,在E. coli FT+L湿细胞中,EcTD、BtLDH和CbFDH酶活分别为1508.8、885.0、117.1 U/g,酶活比为1.7:1:0.13,与体外最佳比例为1:1:0.2不符,CbFDH酶活偏低导致NADH再生效率低下,转化通路不平衡,导致中间产物出现积累,因此对E. coli FT+L进行表达水平优化。

|
| 图 3 重组菌株E. coli FT+L的构建与转化效果评价 Fig. 3 Construction of E. coli FT+L. (A) SDS-PAGE analysis of strain E. coli FT+L from cell-free extracts. (B) Effect of substrate concentration on L-ABA production by strain E. coli FT+L. |
| |
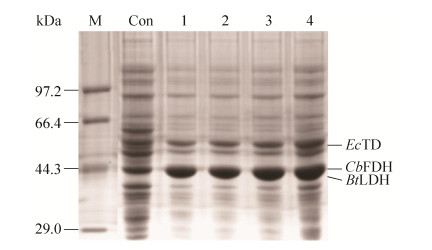
重复表达目标基因可以显著提高目标酶的酶活[21-22],在E. coli FT+L中重复表达fdh基因2–4次获得重组菌株E. coli 2FT+L、E. coli 3FT+L和E. coli 4FT+L,蛋白电泳图谱如图 4所示,表达的目的蛋白条带大小与理论值一致,菌株构建成功。检测E. coli FT+L、E. coli 2FT+L、E. coli 3FT+L和E. coli 4FT+L湿菌体中EcTD、BtLDH和CbFDH酶活,结果如图 5A所示。随着fdh 重复次数的增加,CbFDH酶活从117.1 U/g分别上升至164.6、179.0、191.9 U/g,EcTD酶活从1 508.8 U/g分别下降至1 158.0、855.9、706.3 U/g,BtLDH酶活呈略微下降的趋势。结果显示,E. coli 3FT+L中EcTD、BtLDH和CbFDH酶活比接近1:1:0.2。以E. coli 3FT+L为催化剂,L-ABA产量达到42.4 g/L,摩尔转化率达到98.0%,质量转化率为84.8%,未检测到L-Thr积累,2-OBA残留仅0.23 g/L(图 5B),表明反应体系中辅酶NADH供应正常,3种酶实现均衡协调表达。
|
| 图 4 fdh重复表达菌株的SDS-PAGE分析 Fig. 4 SDS-PAGE analysis of recombinant strains with fdh gene duplicated for different copies. Lane M: marker; lane Con: control E. coli BL21 (DE3); lane 1–4: recombination strain E. coli FT+L, E. coli 2FT+L, E. coli 3FT+L, E. coli 4FT+L. |
| |

|
| 图 5 fdh基因重复表达菌株酶活检测与转化效果评价 Fig. 5 Optimization of co-expressed strain in the activity ratio of EcTD/BtLDH/CbFDH in vivo. (A) The assay of enzymes activity in recombinant strains with fdh gene duplicated for different copies. (B) Effect of different fdh copies on L-ABA production. |
| |
为了进一步提高L-ABA的生产效率,5 L发酵罐上对转化条件进行优化。固定湿菌体质量为25 g/L,不同L-苏氨酸浓度(70–90 g/L)对L-ABA生产的影响如图 6A所示。当苏氨酸浓度达到80 g/L时,L-ABA产量达到最高为62.6 g/L,摩尔转化率为90.4%,继续增加L-苏氨酸的浓度,L-ABA产量不再增加。在此基础上,固定L-苏氨酸浓度为80 g/L,不同湿菌体浓度(15–35 g/L)对L-ABA生产的影响如图 6B所示。当添加湿菌体为20 g/L时,L-ABA产量达到63.7 g/L,摩尔转化率为92.0%,继续增加湿菌体质量,L-ABA产量也不增加。

|
| 图 6 L-苏氨酸和菌体浓度对L-ABA产量及转化率的影响 Fig. 6 Effect of mass ratio of L-Thr (A) and wet cell weight (B) on L-ABA production. |
| |
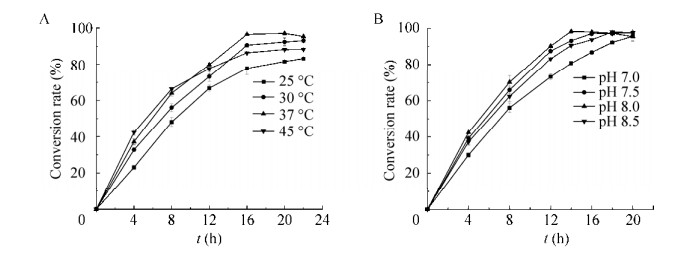
考察不同温度对E. coli 3FT+L全细胞级联催化性能的影响,在E. coli 3FT+L湿菌体20 g/L、L-苏氨酸80 g/L时,研究不同转化温度(25–45 ℃)对L-ABA生产的影响,当转化最适温度为37 ℃,16 h时摩尔转化率达到96.5%;当转化温度低于37 ℃,转化周期延长至22 h以上;当转化温度为45 ℃时,摩尔转化率只能达到88.2% (图 7A)。于是在37 ℃下考察不同pH对全细胞转化生产L-ABA的影响,在pH 7.0–8.5范围内,L-ABA摩尔转化率均能达到95.0%以上,在最适pH为8.0时转化周期最短为14 h,L-ABA摩尔转化率达到98.2% (图 7B)。
|
| 图 7 温度和pH对转化反应的影响 Fig. 7 Effect of reaction temperature (A) and pH (B) on the whole-cell catalyst. |
| |
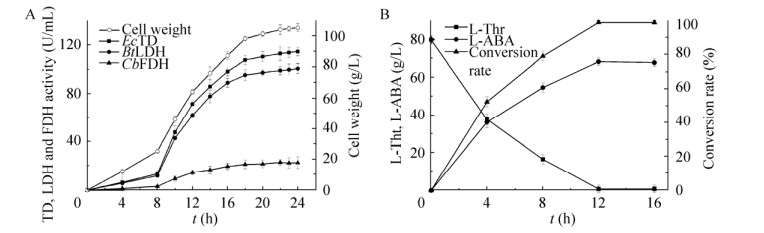
在30 L发酵罐上采用分批补料的方式培养E. coli 3FT+L,随着菌体浓度不断增加,酶活不断提高,发酵24 h湿菌体浓度达到105.9 g/L,此时发酵液中EcTD、BtLDH和CbFDH的酶活分别达到114.7、101.0、22.3 U/mL (图 8A),EcTD、BtLDH和CbFDH酶活比为1:1:0.2。
|
| 图 8 E. coli 3FT+L高密度发酵与转化生产L-ABA Fig. 8 High density fermentation process of E. coli 3FT+L (A) and whole-cell catalyst production of L-ABA (B). |
| |
30 L发酵罐中转化体积为15 L,E. coli 3FT+L湿菌体20 g/L,L-苏氨酸80 g/L,温度37 ℃,使用NaOH调节pH为8.0,随着转化时间的增加,L-ABA逐渐积累,当12 h时L-ABA产量最高达到68.5 g/L,摩尔转化率达到99.0%,质量转化率达到85.6%,L-ABA生产速率为5.71 g/(L·h) (图 8B)。
3 结论利用TD、LDH和FDH三酶级联转化L-苏氨酸生产L-ABA,目前存在辅因子NADH再生用酶的效率较低、多酶催化的转化速率协同性差、需要培养多种基因工程菌使成本高等问题。针对上述问题,本研究开发了一种高效简约制备L-ABA工艺路线,采用一次性投料,转化体系中添加单一细胞E. coli 3FT+L 20 g/L,转化12 h,L-ABA产量达到68.5 g/L,摩尔转化率达99.0%,为后续酶法规模化生产L-ABA奠定一定的理论基础。
| [1] |
Goncalves RSB, da Silva ET, de Souza N, et al. An environmentally friendly, scalable and highly efficient synthesis of (S, S)-ethambutol, a first line drug against tuberculosis. Lett Org Chem, 2015, 12(7): 478-481. DOI:10.2174/1570178612666150521235908 |
| [2] |
Bai GY, Chen LG, Xing P, et al. Synthesis of ethambutol. Fine Chem, 2004, 21(12): 943-945, 949 (in Chinese). 白国义, 陈立功, 邢鹏, 等. 乙胺丁醇的合成. 精细化工, 2004, 21(12): 943-945, 949. DOI:10.3321/j.issn:1003-5214.2004.12.018 |
| [3] |
Shin JS, Kim BG. Transaminase-catalyzed asymmetric synthesis of L-2-aminobutyric acid from achiral reactants. Biotechnol Lett, 2009, 31(10): 1595-1599. DOI:10.1007/s10529-009-0057-7 |
| [4] |
Fujii C, Yasui M, Ishimathu Y. Process for production of (+)-2-amino-1-butanol: US, 3979457, 1976-09-07.
|
| [5] |
Zhou XB, Xu GY, Zhou Y, et al. Synthesis of anticonvulsant drug levetiracetam. Fine Chem Intermed, 2005, 35(2): 27-28 (in Chinese). 周先波, 徐广宇, 周伊, 等. 抗癫痫治疗药物左乙拉西坦的合成研究. 精细化工中间体, 2005, 35(2): 27-28. DOI:10.3969/j.issn.1009-9212.2005.02.008 |
| [6] |
Yin XQ, Sun F, Ge SX. Development of synthesis of α-aminobutyric acid. Fine Chem Intermed, 2010, 40(1): 12-14 (in Chinese). 尹先清, 孙芳, 葛胜祥. α-氨基丁酸化学合成研究进展. 精细化工中间体, 2010, 40(1): 12-14. |
| [7] |
Jeffery EA, Meisters A. Electrochemical synthesis of amino acids by reductive amination of keto acids. Ⅰ. Reduction at mercury electrodes. Aust J Chem, 1978, 31(1): 73-78. DOI:10.1071/CH9780073 |
| [8] |
Synoradzki L, Ruškowski P, Bernaś U. Tartaric acid and its O-acyl derivatives. Part 1. Synthesis of tartaric acid and O-acyl tartaric acids and anhydrides. Org Prep Proced Int, 2005, 37(1): 37-63. DOI:10.1080/00304940509355401 |
| [9] |
Zhang KC, Li H, Cho KM, et al. Expanding metabolism for total biosynthesis of the nonnatural amino acid L-homoalanine. Proc Natl Acad Sci USA, 2010, 107(14): 6234-6239. DOI:10.1073/pnas.0912903107 |
| [10] |
Fotheringham IG, Grinter N, Pantaleone DP, et al. Engineering of a novel biochemical pathway for the biosynthesis of L-2-aminobutyric acid in Escherichia coli K12. Bioorgan Med Chem, 1999, 7(10): 2209-2213. DOI:10.1016/S0968-0896(99)00153-4 |
| [11] |
Li T, Kootstra AB, Fotheringham IG. Nonproteinogenic α-amino acid preparation using equilibrium shifted transamination. Orga Proc Res Dev, 2002, 6(4): 533-538. DOI:10.1021/op025518x |
| [12] |
Galkin A, Kulakova L, Yoshimura T, et al. Synthesis of optically active amino acids from alpha-keto acids with Escherichia coli cells expressing heterologous genes. Appl Environ Microbiol, 1997, 63(12): 4651-4656. DOI:10.1128/AEM.63.12.4651-4656.1997 |
| [13] |
Tao RS, Jiang Y, Zhu FY, et al. A one-pot system for production of L-2-aminobutyric acid from L-threonine by L-threonine deaminase and a NADH-regeneration system based on L-leucine dehydrogenase and formate dehydrogenase. Biotechol Lett, 2013, 36(4): 835-841. |
| [14] |
Umbarger HE, Brown B. Threonine deamination in Escherichia coli. Ⅱ. Evidence for two L-threonine deaminases. J Bacteriol, 1957, 73(1): 105-112. DOI:10.1128/JB.73.1.105-112.1957 |
| [15] |
Ansorge MB, Kula MR. Production of recombinant L-leucine dehydrogenase from Bacillus cereus in pilot scale using the runaway replication system E. coli[piet98]. Biotechnol Bioeng, 2000, 68(5): 557-562. DOI:10.1002/(SICI)1097-0290(20000605)68:5<557::AID-BIT10>3.0.CO;2-J |
| [16] |
Berríos-Rivera SJ, Bennett GN, San KY. Metabolic engineering of Escherichia coli: increase of NADH availability by overexpressing an NAD+-dependent formate dehydrogenase. Metab Eng, 2002, 4(3): 217-229. DOI:10.1006/mben.2002.0227 |
| [17] |
Yu XF, Li Y, Wang XY. Molecular evolution of threonine dehydratase in bacteria. PLoS ONE, 2013, 8(12): e80750. DOI:10.1371/journal.pone.0080750 |
| [18] |
Song W, Wang JH, Wu J, et al. Asymmetric assembly of high-value α-functionalized organic acids using a biocatalytic chiral-group-resetting process. Nat Commun, 2018, 9: 3818. DOI:10.1038/s41467-018-06241-x |
| [19] |
Zhang C, Xing XH. Research progress in cofactor regeneration systems. Chin J Biotech, 2004, 20(6): 811-816 (in Chinese). 张翀, 邢新会. 辅酶再生体系的研究进展. 生物工程学报, 2004, 20(6): 811-816. DOI:10.3321/j.issn:1000-3061.2004.06.001 |
| [20] |
Zhao HM, van der Donk WA. Regeneration of cofactors for use in biocatalysis. Curr Opin Biotechnol, 2003, 14(6): 583-589. DOI:10.1016/j.copbio.2003.09.007 |
| [21] |
Hepworth LJ, France SP, Hussain S, et al. Enzyme cascades in whole cells for the synthesis of chiral cyclic amines. ACS Catal, 2017, 7(4): 2920-2925. DOI:10.1021/acscatal.7b00513 |
| [22] |
Qian YY, Liu J, Song W, et al. Production of β-alanine from fumaric acid using a dual-enzyme cascade. ChemCatChem, 2018, 10(21): 4984-4991. DOI:10.1002/cctc.201801050 |
 2020, Vol. 36
2020, Vol. 36