中国科学院微生物研究所、中国微生物学会主办
文章信息
- 车雪梅, 司徒卫, 余柳松, 王辉, 陈亚精, 司徒建崧, 李耀, 余景升, 陈国强
- Che Xuemei, Si tuWei, Yu Liusong, Wang Hui, Chen Yajing, Situ Jiansong, Li Yao, Yu Jingsheng, Chen Guo-Qiang
- 聚羟基脂肪酸酯的应用展望
- Application perspectives of polyhydroxyalkanoates
- 生物工程学报, 2018, 34(10): 1531-1542
- Chinese Journal of Biotechnology, 2018, 34(10): 1531-1542
- 10.13345/j.cjb.180329
-
文章历史
- Received: August 15, 2018
- Accepted: September 3, 2018
2 广东省化学纤维研究所,广东 广州 510245;
3 圣之力(广州)科技有限公司,广东 广州 511458;
4 中山大学附属第六医院,广东 广州 510655
2 Guangdong Chemical Fiber Research Institute, Guangzhou 510245, Guangdong, China;
3 STL (Guangzhou) Technology Ltd., Guangzhou 511458, Guangdong, China;
4 The Sixth Affiliated Hospital of Sun Yat-sen University, Guangzhou 510655, Guangdong, China
聚羟基脂肪酸酯(Polyhydroxyalkanoates,简称PHA)是一类高分子聚酯的统称,完全由微生物合成[1]。PHA具有生物可降解性和生物相容性,因而被认为是环境友好型材料,广泛应用于生物医疗、组织工程、绿色包装和手性中间体等各个领域。
1 聚羟基脂肪酸酯(PHA)概述PHA是微生物体内的一类3-羟基脂肪酸组成的线性聚酯,其基本结构见图 1。其分子量多为50 000–20 000 000 Da不等。不同的PHA主要区别于C-3位上不同的侧链基团,以侧链为甲基的聚3-羟基丁酸(PHB)最为常见。PHA的结构通式和胞内形状如图 1所示。PHA的结构变化多样,不仅侧链的“R”和主链单体链长“m”均可变化。另一方面,不同的单体还可以形成不同的共聚物,包括二元共聚物如3-羟基丁酸(HB)和3-羟基己酸(HHx)的共聚酯PHBHHx,三元共聚物如3-羟基丁酸(HB),3-羟基戊酸(HV)和3-羟基己酸(HHx)的共聚酯PHBVHHx。同时,单体在共聚物中比例的变化也带来共聚物性能的许多变化[1]。此外,根据单体的不同的排列方式,PHA还可以形成均聚物、无规共聚物和嵌段共聚物等多种结构[2]。
PHA可以根据单体的碳原子数分为两类:短链(short-chain-length,SCL) PHA,其单体由3–5个碳原子组成,如PHB、聚羟基戊酸酯(Polyhydroxyvalerate,简称PHV)等;中长链(Medium-chain-length,MCL) PHA,其单体由6−14个碳原子组成,如聚羟基己酸酯(Polyhydroxyhexanoate,简称PHHx)、聚羟基辛酸酯(Polyhydroxyoctanoate,简称PHO)等。
大多数微生物只能合成其中一类PHA,PHA单体的碳原子数不同与PHA合酶的底物特异性息息相关。由短链和中长链单体组成的PHA聚合物可以结合短链PHA和中长链PHA的优异性能,从而引起了学术界和产业界越来越多的关注。除此之外,还有许多侧链含有功能团如苯环、卤素、不饱和键等的PHA,这些PHA可以进行许多化学修饰,使PHA具有新的功能。另外,通过嵌段共聚,使不同性能的高聚物通过化学键连在一起,我们可以获得无数种性能各异的材料,这些材料的性能还可通过调节不同嵌段的比例得到控制[2]。
由于PHA的单体种类多样、彼此之间链长差别很大,这就使不同的PHA材料学性质有很大的不同,从坚硬质脆的硬塑料到柔软的弹性体。表 1列出了几种PHA和传统塑料的性能比较[3]。
| PHA | Melting temperature (Tm, ℃) | Glass transition temperature (Tg, ℃) | Tensile strength (MPa) | Elongation at break (%) |
| PHB | 177 | 4 | 43 | 5 |
| PHO | 61 | –35 | 10 | 300 |
| P(3HB-co-3mol% 3HV) | 170 | – | 38 | – |
| P(3HB-co-9mol% 3HV) | 162 | – | 37 | – |
| P(3HB-co-14mol% 3HV) | 150 | – | 35 | – |
| P(3HB-co-20mol% 3HV) | 145 | – | 32 | – |
| P(3HB-co-25mol% 3HV) | 137 | – | 30 | – |
| P(3HB-co-3mol% 4HB) | 166 | – | 28 | 45 |
| P(3HB-co-10mol% 4HB) | 159 | – | 24 | 242 |
| P(3HB-co-16mol% 4HB) | – | – | 26 | 444 |
| P(3HB-co-64mol%4HB) | 50 | – | 17 | 591 |
| P(3HB-co-90mol% 4HB) | 50 | – | 65 | 1 080 |
| P(3HB-co-10mol%HHx) | 151 | 0 | 21 | 400 |
| P(3HB-co-17mol%HHx) | 120 | –2 | 20 | 850 |
| P(3HB-co-25mol%HHx) | 52 | –4 | – | – |
| PP | 186 | –10 | 38 | 400 |
| PET | 262 | – | 56 | 8 300 |
| HDPE | 135 | – | 29 | – |
| PP(Polypropylene); PET(Polyethylene terephthalate); HDPE(High density polyethylene). | ||||
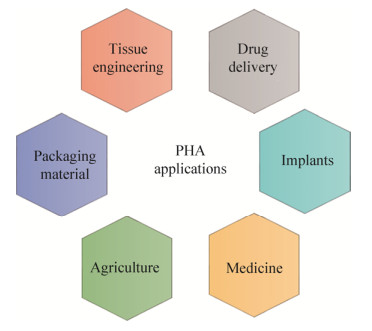
PHA在某些性能上可以媲美传统的热塑性塑料,它还具有一些独特的生物可降解性、生物相容性、光学异构性、提高微生物的抗逆性等性能,在医学、农业和包装业等领域具有广泛的应用前景(图 2)。
PHA是一种细胞和组织相容性良好的材料,植入体内引起的组织学反应极其微弱[5]。在3-羟基丁酸-3-羟基戊酸共聚酯(PHBV)膜移植入肌肉内90周的研究中,在植入区内未发现肿胀或组织坏死[6]。将聚羟基丁酸酯(Poly-hydroxybutyrate,PHB)及PHBV植入小鼠皮下也观察到相似结果[7]。中长链3-羟基丁酸-3-辛酸共聚酯[P (3HB-co-3HO)]植入小鼠皮下2周时即出现很小的组织反应,移植体被一层薄的成纤维细胞包裹,约有4−6层细胞厚;植入40周未见巨噬细胞,组织应答非常温和,移植体周围的结缔组织细胞数量恒定;聚合物在组织内异常惰性,与周围组织无粘连,极易被移走[8]。Han等开发了利用嗜盐古菌合成新型PHA的方法,获得了无规共聚和高规整共聚PHBV,3HV单体由10 mol%提高到60 mol%。与细菌PHB/PHBV及医用PLA相比,嗜盐古菌PHBV更有利于成纤维细胞和成骨细胞的贴附和增殖,表现出更好的细胞相容性[9-11]。随后,基于嗜盐古菌PHBV开发的抗菌材料也显示出优异的抗菌性能[9]。2007年取得突破性的进展,由美国Tepha公司生产的以P4HB为原料的TephaFLEX®可吸收缝合线,正式被食品药品监督管理局(Food and Drug Administration,FDA)认证,获准进入市场,标志着PHA材料的实际医学应用的开始[12]。目前,PHA材料已被用于组织工程、植入材料、药物缓释、医疗保健等多个领域的研究中[4]。
2.1 组织工程和植入材料组织工程支架是为了满足不同人体组织替代的需要而设计的具有独特形态和功能的材料框架,支持并帮助细胞形成特定组织器官。目前,根据PHA材料的特性,PHA组织工程支架的研究包括:心血管、骨、软骨、神经导管、食管和皮肤等[13] (图 3)。
MCL-PHA具有良好的柔韧性,接近于三尖瓣心脏瓣膜中的小叶,因而被用于心脏瓣膜支架的研究。Sodian等用聚3-羟基己酸辛酸酯[P(3HHx-co-3HO)]材料制作了一个三尖瓣心脏瓣膜形状的支架,并接种上自体血管细胞,植入羔羊肺部血管,120 d后只发生了血管轻微狭窄,未见血管栓塞[14]。同时,与其他高分子材料共混,能够改善PHA心脏瓣膜的性状。在P (3HHx-co-3HO)中混入少量PGA材料,能够在植入6个月后观察到非连续的轻微的瓣膜回流现象[15]。Stamm等的研究使用了灌注有PHB的猪动脉脱细胞支架,在体外实验中,这种基质/聚合物杂合支架比单纯脱细胞支架血浆凝集更少且矿化程度更低[16]。
PHA材料具有生物相容性良好,降解速度以及机械性能可调的优势,因此也被用于血管组织工程研究中[13]。最早被应用于血管组织工程的PHA是柔韧性较强的PHO和P4HB。Opitz等在体外生物反应器中培养血管平滑肌细胞(Vascular smooth muscle cells,vSMCs)与P4HB支架复合血管,观察到血管组织层状汇合,获得了与大动脉机械性能相似的P4HB组织工程血管[17]。
PHBHHx也被证明具有良好的血液相容性[18]。PHBHHx材料表面血小板粘附较少,溶血反应程度较低,被证明是一种良好的血液接触材料。Puppy等利用计算机辅助湿法纺丝制备了PHBHHx/PCL支架,体外培养实验中,人脐静脉血管内皮细胞在PHBHHx/PCL支架上维持了两周以上的正常增殖,证明了这种材料作为血管移植物的巨大潜力[19]。
2.1.2 骨和软骨组织工程高机械性能是骨组织的显著特征,因而早期PHA骨组织工程研究人员较多地使用短链PHA,如PHB和PHBV来构建骨组织工程支架[20]。Kose等发现,成骨细胞在大孔的PHBV多孔支架上增殖和矿化水平更优,骨髓干细胞(Bone marrow stromal cells,BMSC)在PHBV发泡材料上碱性磷酸酶活性增加,骨钙素(Osteocalcin)分泌增多,表现出成骨分化特征[21]。他们随后的体内实验也证实了将骨髓干细胞预先接种到PHBV支架上形成细胞支架复合物,更加有利于体内的组织修复。
为加强支架硬度,组成骨基质主要矿物成分(65%−70%)的羟基磷灰石(Hydroxylapatite,HA)也常被用于共混修饰PHA支架。HA共混有助于提高PHB支架的机械性能以及与骨细胞的生物相容性[22-23]。体内修复效果评估发现,PHBV/HA支架在植入兔胫骨后,成骨细胞和骨细胞被观察到广泛出现在植入材料与组织的界面区域;界面处薄层状的新骨形成,伴随着支架聚合物材料的降解;新生骨的厚度在植入后第1个月为130 µm,到植入后第6个月时已经增加到770 µm[24]。
除了骨组织工程支架外,PHA也被用于软骨组织支架的研究[25]。与骨组织工程相类似,组织工程软骨支架首先是需要提供合适的机械性能和软骨组织修复的空间支持;其次是与组织修复速度相匹配的降解速度;然后是生物活性,诱导细胞成软骨分化。在近期的研究中,Mota等开发新型湿法纺丝技术制备PHBHHx支架,基于逐层添加方法,制备纤维可控排列并且完全互联的多孔网络,支架的孔隙率在该范围内为79%−88%,纤维直径为47−76 μm,孔径为123−789 μm。由于PHBHHx溶液凝固过程中的相转化过程,所得纤维显示出与外部纤维表面良好连接的内部孔隙结构。结果表明,支架的压缩模量、屈服应力和屈服应变均可通过改变参数来调整到一定程度。在PHBHHx支架上培养3周的MC3T3-E1小鼠成骨细胞细胞表现出可观的增殖和分化[26]。后续研究中,作者使用计算机辅助湿法纺丝制备具有特定形状和多孔结构的PHBHHx组织工程支架。通过形态学和热机械表征评估制造过程对材料特性的影响,PHBHHx支架的压缩和机械性能表明,多孔结构显示出各向异性行为,形成的宏观通道增强了支架的抗压刚度,PHBHHx支架在高压缩刚度和增强拉伸方面显著优于PCL支架[27]。
2.1.3 神经导管组织工程PHB支架可以促进神经细胞的增殖和分化,Young等用PHB导管成功修复了兔腓总神经(Common peroneal nerve) 4 cm长的神经缺失[28]。为进一步改善PHB导管的生物活性,外周神经支持细胞施旺细胞(Schwann cells)被接种到导管支架的内表面,这样的细胞材料复合支架能够发挥施旺细胞营养功能而促进神经再生,在植入神经缺损处后能够更好地指导损伤神经再生[29]。PHBHHx相较于PHB,具有更好的弹性,在体外实验中也表现出与神经细胞良好的相容性[30]。Xu等比较了PHB、P3HB4HB和PHBHHx促进中枢神经系统(NSC)生长和分化的潜能,其中PHBHHx显示出最强促进CNS修复的能力[31]。另外,一种3-羟基丁酸酯、3-羟基戊酸酯和3-羟基己酸酯的三元酯,缩写为PHBVHHx,相较于PLA和PHBHHx,更有利于人类骨髓间充质细胞分化为神经细胞[32]。除了单一一种PHA,不同比例的PHB/PHO的共混材料也用来进行神经细胞的培养和研究,随着PHB比例的增加,共混膜的表面粗糙度和刚度也随之增加,当PHB比例增加至75%的时候,最有利于神经细胞的增殖和分化[33]。除了单纯PHA材料,PHA/多壁碳纳米管复合材料也发现可以促进原始大鼠中脑细胞的分化活性[34]。
2.2 可控药物载体材料PHA的生物降解性以及生物相容性使其成为药物载体的一个很好的选择。PHA作为可降解的载体用于药物、激素、杀虫剂和除草剂等的可控释放也越来越多的引起研究者的关注。通常情况下,药物微纳载体是将材料加工为微米/纳米级大小的颗粒,将药物等小分子包裹在纳米颗粒之中或吸附在其表面,同时在颗粒表面耦联特异性的靶向分子,如特异性配体、单克隆抗体等,通过靶向分子与细胞表面特异性受体结合,在细胞摄取作用下进入细胞内,实现安全有效的靶向性药物治疗的方法[35]。和其他高分子一样,PHA微纳载体主要通过溶剂挥发的方法制备成纳米微球,纤维和微胶囊等载体。
由于PHA的聚酯疏水性,是疏水药物的理想载体,在药物缓释及药物靶向传递方面具有独特的优势。Rezaie及其同事制备了加载了芬戈莫德的PHBV微球,通过包封效率,加载,释放动力学和形态等性质的研究,发现芬戈莫德、乳化剂聚乙烯醇(PVA)和PHBV的浓度明显影响封装效率[36]。和体外模拟条件下进行的药物载体释放研究不同,Xiong等[37]研究了不同大小粒径的PHB和PHBHHx纳米颗粒在活细胞内的降解和药物缓释情况。通过不同的方法可制备出平均粒径大小为160 nm和250 nm两种纳米颗粒,并以PLA作为对照。同时加入脂溶性色素罗丹明B异硫氰酸酯(RBITC)作为药物模型,用来研究PHB和PHBHHx作为亲脂性药物载体的包封率及长期的缓慢释放行为。结果表明,在巨噬细胞吞噬后,3种材料制备的纳米颗粒均能缓慢释放RBITC,PHB和PHBHHx基本能维持在20 d,而PLA纳米颗粒释放的药物只持续了15 d。这项研究首次表明PHB和PHBHHx可以被有效地用于实现细胞内控制药物释放。近期,Scheithauer等[38]利用电喷雾方法成功制备了载有植物雌激素大豆黄酮的PHBV微球。这种新方法实现了微球表面均匀的形态和窄粒径分布,平均球直径约为5 μm,并未对药物施加剪切或温度应力;此外,初始爆发释放大豆苷元在1 h内可以忽略不计,但随后在3 d内持续释放。加载了大豆苷元PHBV微球的有望提供一种骨质疏松症激素疗法。
PHA载体亦可以通过PHA颗粒表面蛋白对PHA微纳载体颗粒的修饰来实现靶向给药[39]。Parlane等通过融合蛋白的方法,直接将组织特异性蛋白抗体连接到PHB颗粒上:将病毒抗体多肽片段与PHB颗粒结合蛋白PhaC融合表达,细菌合成PHB的同时会将PhaC-抗体多肽片段装配到PHB纳米颗粒的表面,直接在菌体内实现“靶向”蛋白修饰[40]。
PHA也用于释放核酸,Jeff等合成带有正电荷的PHA材料PHON, PHON可以结合并将DNA压缩成为小于200 nm的带正电的粒子,PHON能对DNA进行保护30 min以上,并在哺乳动物细胞中表达目的蛋白[41]。
PHA作为生物可降解性材料,目前被广泛研究用于组织工程材料。然而,它从大规模低成本的生产到医用市场仍有很长的路要走,有着更好的浸润性和优异机械强度的PHA共聚物有待被开发。
2.3 PHA降解产物的医疗保健作用研究作为可降解材料,PHA材料降解所产生的小分子寡聚物或是单体成分及材料与体内/体外细胞或组织的长期接触的相容性息息相关。因而,降解产物的生物效应是PHA医学应用的研究方向之一。PHA降解产物的生物活性研究表明,这些小分子的化合物无细胞毒性,而且对细胞内钙流、线粒体活性等生理生化有影响,尤其在骨质疏松,糖尿病和神经退行性疾病的治疗上表现出潜在的医疗保健药用价值[39]。
Xiao等发现,D-3-羟基丁酸、DL-3-羟基丁酸以及3-羟基丁酸甲酯都能明显促进神经胶质细胞的生长,而且3-羟基丁酸甲酯的作用最为明显[42]。Cheng等的研究也表明,DL-β-羟基丁酸对于鼠成纤维细胞L929、脐静脉内皮细胞、兔关节软骨细胞都有促进细胞增殖的作用[43]。Sun等的研究中,利用脂质体包裹寡聚PHA (Oligohydroxyalkanoate,OHA)来处理鼠成纤维细胞L929,结果显示不同的OHA脂质体对细胞的存活率有不同的作用。而与对照组相比,含量低于20 mg/L OHA脂质体未表现出明显的抑制作用;当浓度或OHAs含量高于40 mg/L时OHA都能明显地抑制细胞生长。引人注意的是,OHAs对细胞生长的抑制作用随着OHAs链长的增加而降低[44]。另外,3-HB能够刺激成骨细胞MC3T3-E1的增殖、分化(碱性磷酸酶的活性)和矿化(在一定浓度范围内,矿化结的形成随着3-HB浓度提高而增多),抑制血清饥饿诱导的细胞凋亡[45]。Zhang等的研究[46]发现,3-HBME对于阿尔茨海默症的模型小鼠也有提升其学习记忆能力的功效,而此效果可能的机制,一方面是通过抑制某些在阿尔茨海默症中高表达基因的转录,如凋亡相关蛋白caspase 3和载脂蛋白E (Apolipoprotein E,APOE);另一方面是通过其对线粒体的保护作用,如抑制细胞内ROS的产生,稳定线粒体膜电位,保护线粒体呼吸链酶的活性,同时利用3-HBME作为替代葡萄糖的能量物质以增加ATP的产量。这些结果都说明,3-HBME可能成为一种很有潜力的治疗阿尔茨海默症的药物。
3 PHA在农业领域应用在农业中,PHA被看作天然复合材料,可以在土壤中自然降解。具有10 wt%蒸馏干燥谷物(DDGS)的PHA复合物比不含DDGS的PHA降解得更好。PHA和DDGS的复合物显示出良好的机械和生物降解性能,并在土壤中作为有机物降解[47]。对于涂覆PHBV生物塑料的种子的研究中发现,PHBV的涂覆对于土壤中种子的萌发活性没有影响[48]。由Procter & Gamble生产商业名字为NodaxTM的农膜也正在逐步推广,研究发现它可以保护水分以提高土壤质量和肥力。NodaxTM的降解是通过厌氧方法进行的,因此它可以加载肥料和杀虫剂[49]。农药的缓释也是PHA在农业领域的应用之一,Prudnikova等研究了PHA作为除草剂的载体在土壤中可控释放,实验发现包被在PHA中的除草剂逐步缓慢释放,可以有效抑制杂草的生长,随后PHA被土壤微生物降解[50]。在某些情况下,土壤中会加入特定的细菌以增加植物的固氮作用,PHA有助于提高细菌的抗逆性,增强固氮作用。
在畜牧业有研究表明,PHB可以为肉鸡、绵羊和猪等提供额外的营养物质[51]。在水产养殖中,PHA作为饲料添加剂表现出抑制细菌性病原体的效果[52]。研究表明,水体中存在一定量的PHB可以起到抑制弧菌生长并保护被弧菌感染的卤虫的作用[53];De Schryver等研究发现饲料中添加适量的PHB可以促进欧洲鲈鱼和罗氏沼虾的生长并有助于其肠道益生菌群的形成[54],采用PHB强化的轮虫和卤虫投喂中华绒螯蟹蚤状幼体,可显著提高其蜕皮和抗弧菌能力[55]。虽然目前PHB表现出良好的促进水产品的生长性能,但是其机理还未明确,有待进一步的研究。
|
| 图 4 PHA在农业领域的应用 Figure 4 Application of PHA in agriculture. (A) PHA film. (B) Fish fed with PHA. |
| |
PHA的工业化生产已经经历了4代产品的更新换代。第一代商业化的PHA是聚3-羟基丁酸酯(PHB),具有与聚丙烯类似的热塑性,但它的脆性和较差的热稳定性限制了它的工业应用。第二代热塑性PHA材料为3-羟基丁酸-3-羟基戊酸共聚酯(PHBV),可由混合碳源培养微生物获得,并可以制造出一系列的塑料产品。3-羟基丁酸-3-羟基己酸共聚酯(PHBHHx)是第三代新型PHA共聚物,具有比PHB更好的柔韧性。第四代PHA材料是3-羟基丁酸-4-羟基丁酸共聚酯(P3HB4HB),可以通过单体比例调节,得到不同性能的材料。因为优异的生物可降解性和可以媲美石油基材料的力学性能,PHA成为绿色包装的首选[56]。PHA用于包装膜,主要用于袋、包装箱、纸的包装。类似于传统塑料,PHA也用于诸如剃刀、器具、高尔夫球座、鱼饵、尿布、妇女卫生用品、洗发水瓶和化妆品的包装等[56]。Bourbonnais等利用PHA乳胶制备纸张的防水层,研究中对比了PHB和PHBV的效果,发现PHB均聚物的施胶效果明显优于共聚物[57]。通常情况下,理想的塑料制品应具有如下特点,如:坚韧、抗压、有弹性、有回弹性、疏水、抗酯、抗热等,PHA的原始状态并不能很好地满足工业产品的要求,常采用化学和物理等方法对其改性以满足不同的性能要求,最简单的方法就是通过和其他聚合物物理共混改变结晶性能,以提高其机械性能。其中,PHA和PLA是最常见的共混体系,中国科学院宁波材料技术与工程研究所研究人员将PLA与PHBV反应性共混,再经熔融纺丝制得品质优异的新型生物基化学纤维——禾素TM[58]。在加工过程中,PHBV和PLA二者相互促进结晶,短时间内可以达到较高的结晶度,得到性能优异的纤维,其风格与手感等方面与真丝、铜氨等高档纤维品种相媲美。
除了聚合物,一些纳米材料比如纳米纤维素、纳米黏土、碳纳米管和纳米氧化物等也用来增强PHA材料的性能,这些纳米材料的引入可以有效提高PHA的成核速率、机械性能和热稳定性等。其中,纤维素因其来源丰富、可再生、成本低、可降解和生态环保等特性,被越来越多地作为生物基纳米填料在复合物中使用[59]。Sara Malmir等利用溶液浇注方法制备PHBV和纤维素纳米微晶(CNC)的复合材料,发现CNC可以显著提高PHBV的成核速率,而且当CNC的添加量为4%的时候,复合材料的氧气和水的阻隔率提高4倍。Yu等制备了PHBV和PHBV接枝多壁碳纳米管(PHBV-g-MWCNTs)复合材料,PHBV-g-MWCNTs均匀分散在PHBV的基体中个,提高材料的热稳定性,阻隔性能和力学性能。当PHBV-g-MWCNTs的添加量为7%的时候,复合材料的拉伸性能和杨氏模量分别提高了88%和172%[60]。

|
| 图 5 PHA在塑料和工业领域的应用 Figure 5 Applications in materials industry. (A) PHA pellets. (B) tableware made by PHA composites. (C) 3D printing materials. (D) PHA textiles. |
| |
从商业化的PHA发展过程,4代商业化的PHA即PHB、PHBV、PHBHHx和P3HB4HB,从短链PHA的共聚物逐渐发展为短链和中长链的共聚物,学者预测羟基丁酸(HB)与羟基辛酸(HO)或羟基癸酸(HD)的共聚物以一定比例共聚时将会获得物化性能更优秀的PHA,这方面已看到曙光[61]。与此同时,研究者也致力于合成性能优异的嵌段共聚物和带有功能基团(如碳碳双键,三键等)的PHA,通过化学修饰,有望得到多功能PHA,PHA多样性的日益拓宽,PHA的应用领域也必然越来越广。在医学方面,除了传统的组织工程支架外,魏岱旭等[62]设计出一种新型的可注射开放式多孔微球(Open porous microsphere,OPM),可作为细胞生长和运输的微载体(Microcarrier)。PHA-OPM具备了PHA良好的生物相容性、微球的可注射性和组织工程支架的开放式三维空间结构的三重优势,是一种特殊的球状的三维培养载体。其特殊的开放式多孔结构能在体外培养时帮助细胞向内生长;在注射运输过程中起到支撑作用,保护微球内部的细胞免于挤压和摩擦;并能实现动物体内释放细胞和组织修复的目的,有望为微创手术及干细胞治疗提供一种新的工具。除了常规的包装和医学领域的应用,研究者发现PHA可以作为缓释碳源用于水和废水的反硝化脱氮的固体基质,在脱氮过程中,PHA不仅提供了连续的资源也有利于生物膜的培养和生成,表现出良好的应用前景[63]。PHA的大规模产业化和商业化一直受到生产成本的制约,在一定程度上限制了对其应用研究的开展。通过生物技术的发展,最终将有可能降低所有种类PHA的生产成本,推进PHA的应用。基于PHA的生物相容性和可降解性,PHA有望在医学上有更多的突破与应用,而且其寡聚物作为某些疾病的潜在药物,也有望为PHA的应用开拓新的领域。同时,PHA应用的拓展也需要不同领域的学者共同协作,构筑一个更加环保的未来。
| [1] | Pbs A, Malafaia CB. Perspectives on the production, structural characteristics and potential applications of bioplastics derived from polyhydroxyalkanoates. Int J Biol Macromol, 2017, 107(Pt A): 615–625. |
| [2] | Raza ZA, Abid S, Banat IM. Polyhydroxyalkanoates: characteristics, production, recent developments and applications. Int Biodeter Biodegr, 2018, 126: 45–56. DOI: 10.1016/j.ibiod.2017.10.001 |
| [3] | Chen GQ, Wang Y. Medical applications of biopolyesters polyhydroxyalkanoates. Chin J Polym Sci, 2013, 31(5): 719–736. DOI: 10.1007/s10118-013-1280-1 |
| [4] | Gadgil BST, Killi N, Rathna GVN. Polyhydroxyalkanoates as biomaterials. MedChemComm, 2017, 8(9): 1774–1787. DOI: 10.1039/C7MD00252A |
| [5] | Valappil SP, Misra SK, Boccaccini AR, et al. Biomedical applications of polyhydroxyalkanoates, an overview of animal testing and in vivo responses. Expert Rev Med Dev, 2006, 3(6): 853–868. DOI: 10.1586/17434440.3.6.853 |
| [6] | Volova T, Shishatskaya E, Sevastianov V, et al. Results of biomedical investigations of PHB and PHB/PHV fibers. Biochem Engin J, 2003, 16(2): 125–133. DOI: 10.1016/S1369-703X(03)00038-X |
| [7] | Gogolewski S, Jovanovic M, Perren S, et al. Tissue response and in vivo degradation of selected polyhydroxyacids: Polylactides (PLA): poly(3- hydroxybutyrate) (PHB): and poly (3-hydroxybutyrate- co-3-hydroxyvalerate)(PHB/VA). J Biomed Mater Res, 1993, 27(9): 1135–1148. DOI: 10.1002/(ISSN)1097-4636 |
| [8] | Rai R, Keshavarz T, Roether JA, et al. Medium chain length polyhydroxyalkanoates, promising new biomedical materials for the future. Mat Sci Eng R, 2011, 72(3): 29–47. DOI: 10.1016/j.mser.2010.11.002 |
| [9] | Xue Q, Liu XB, Lao YH, et al. Anti-infective biomaterials with surface-decorated tachyplesin I. Biomaterials, 2018, 178: 351–362. DOI: 10.1016/j.biomaterials.2018.05.008 |
| [10] | Han J, Wu LP, Hou J, et al. Biosynthesis, characterization, and hemostasis potential of tailor- made Poly(3-hydroxybutyrate-co-3-hydroxyvalerate) produced by Haloferax mediterranei. Biomacromolecules, 2015, 16(2): 578–588. DOI: 10.1021/bm5016267 |
| [11] | Han J, Wu LP, Liu XB, et al. Biodegradation and biocompatibility of haloarchaea-produced poly (3-hydroxybutyrate-co-3-hydroxyvalerate) copolymers. Biomaterials, 2017, 139: 172–186. DOI: 10.1016/j.biomaterials.2017.06.006 |
| [12] | Pakalapati H, Chang CK, Show PL, et al. Development of polyhydroxyalkanoates production from waste feedstocks and applications. J Biosci Bioeng, 2018, 126(3): 282–292. DOI: 10.1016/j.jbiosc.2018.03.016 |
| [13] | Koller M. Biodegradable and biocompatible polyhydroxy-alkanoates (PHA): Auspicious microbial macromolecules for pharmaceutical and therapeutic applications. Molecules, 2018, 23(2): 362. DOI: 10.3390/molecules23020362 |
| [14] | Sodian R, Hoerstrup SP, Sperling JS, et al. Early in vivo experience with tissue-engineered trileaflet heart valves. Circulation, 2000, 102(19 Suppl 3): Ⅲ22–29. |
| [15] | Sodian R, Hoerstrup SP, Sperling JS, et al. Evaluation of biodegradable, three-dimensional matrices for tissue engineering of heart valves. ASAIO J, 2000, 46(1): 107–110. DOI: 10.1097/00002480-200001000-00025 |
| [16] | Stamm C, Khosravi A, Grabow N, et al. Biomatrix/polymer composite material for heart valve tissue engineering. Ann Thor Surg, 2004, 78(6): 2084–2093. DOI: 10.1016/j.athoracsur.2004.03.106 |
| [17] | Opitz F, Schenke-Layland K, Richter W, et al. Tissue engineering of ovine aortic blood vessel substitutes using applied shear stress and enzymatically derived vascular smooth muscle cells. Ann Biomed Eng, 2004, 32(2): 212–222. DOI: 10.1023/B:ABME.0000012741.85600.f1 |
| [18] | Zaharia C, Vasile E, Galateanu B, et al. Bacterial Cellulose-polyhydroxyalkanoates Composites Synthesis, physico-chemical characterization and biological evaluation for tissue engineering. Mater Plast, 2014, 51(1): 1–5. |
| [19] | Puppi D, Pirosa A, Lupi G, et al. Design and fabrication of novel polymeric biodegradable stents for small caliber blood vessels by computer-aided wet-spinning. Biomed Mater, 2017, 12(3): 035011. DOI: 10.1088/1748-605X/aa6a28 |
| [20] | Lim J, You M, Li J, et al. Emerging bone tissue engineering via Polyhydroxyalkanoate (PHA)-based scaffolds. Mater Sci Eng C Mater Biol Appl, 2017, 79: 917–929. DOI: 10.1016/j.msec.2017.05.132 |
| [21] | Köse GT, Ber S, Korkusuz F, et al. Poly(3-hydroxybutyric acid-co-3-hydroxyvaleric acid) based tissue engineering matrices. J Mater Sci Mater Mater Med, 2003, 14(2): 121–126. DOI: 10.1023/A:1022063628099 |
| [22] | Ramier J, Bouderlique T, Stoilova O, et al. Biocomposite scaffolds based on electrospun poly (3-hydroxybutyrate) nanofibers and electrosprayed hydroxyapatite nanoparticles for bone tissue engineering applications. Mater Sci Eng C, 2014, 38: 161–169. DOI: 10.1016/j.msec.2014.01.046 |
| [23] | Sadat-Shojai M, Khorasani MT, Jamshidi A. A new strategy for fabrication of bone scaffolds using electrospun nano-HAp/PHB fibers and protein hydrogels. Chem Eng J, 2016, 289: 38–47. DOI: 10.1016/j.cej.2015.12.079 |
| [24] | Luklinska ZB, Schluckwerder H. In vivo response to HA‐polyhydroxybutyrate/polyhydroxyvalerate composite. J Microscopy, 2003, 211(2): 121–129. DOI: 10.1046/j.1365-2818.2003.01204.x |
| [25] | Puppi D, Chiellini F, Piras AM, et al. Polymeric materials for bone and cartilage repair. Prog Polym Sci, 2010, 35(4): 403–440. DOI: 10.1016/j.progpolymsci.2010.01.006 |
| [26] | Mota C, Wang SY, Puppi D, et al. Additive manufacturing of poly[(R)-3-hydroxybutyrate-co- (R)-3-hydroxyhexanoate] scaffolds for engineered bone development. J Tissue Eng Regen Med, 2017, 11(1): 175–186. DOI: 10.1002/term.v11.1 |
| [27] | Puppi D, Pirosa A, Morelli A, et al. Design, fabrication and characterization of tailored poly[(R)-3-hydroxybutyrate-co-(R)-3-hydroxyexanoate] scaffolds by computer-aided wet-spinning. Rapid Prototyp J, 2018, 24(1): 1–8. DOI: 10.1108/RPJ-03-2016-0037 |
| [28] | Young R, Terenghi G, Wiberg M. Poly-3-hydroxybutyrate(PHB): a resorbable conduit for long-gap repair in peripheral nerves. Brit J Plast Surg, 2002, 55(3): 235–240. DOI: 10.1054/bjps.2002.3798 |
| [29] | Novikov LN, Novikova LN, Mosahebi A, et al. A novel biodegradable implant for neuronal rescue and regeneration after spinal cord injury. Biomaterials, 2002, 23(16): 3369–3376. DOI: 10.1016/S0142-9612(02)00037-6 |
| [30] |
Yang YY, Li XH, Li GF, et al. Study on chitosan and PHBHHx used as nerve regeneration conduit material.
J Biomed Eng, 2002, 19(1): 25–29.
(in Chinese). 杨吟野, 李训虎, 李国富, 等. 壳聚糖和PHBHHx用作神经修复导管材料的研究. 生物医学工程学杂志, 2002, 19(1): 25-29. DOI:10.3321/j.issn:1001-5515.2002.01.007 |
| [31] | Xu XY, Li XT, Peng SW, et al. The behaviour of neural stem cells on polyhydroxyalkanoate nanofiber scaffolds. Biomaterials, 2010, 31(14): 3967–3975. DOI: 10.1016/j.biomaterials.2010.01.132 |
| [32] | Wang L, Wang ZH, Shen CY, et al. Differentiation of human bone marrow mesenchymal stem cells grown in terpolyesters of 3-hydroxyalkanoates scaffolds into nerve cells. Biomaterials, 2010, 31(7): 1691–1698. DOI: 10.1016/j.biomaterials.2009.11.053 |
| [33] | Lizarraga‐Valderrama LR, Nigmatullin R, Taylor C, et al. Nerve tissue engineering using blends of poly(3‐hydroxyalkanoates) for peripheral nerve regeneration. Eng Life Sci, 2015, 15(6): 612–621. DOI: 10.1002/elsc.201400151 |
| [34] | Vallejo-Giraldo C, Pugliese E, Larrañaga A, et al. Polyhydroxyalkanoate/carbon nanotube nanocomposites: flexible electrically conducting elastomers for neural applications. Nanomedicine, 2016, 11(19): 2547–2563. DOI: 10.2217/nnm-2016-0075 |
| [35] | Peer D, Karp JM, Hong S, et al. Nanocarriers as an emerging platform for cancer therapy. Nat Nanotechnol, 2007, 2(12): 751–760. DOI: 10.1038/nnano.2007.387 |
| [36] | Rezaie SL, Bahari JN, Khoshayand MR, et al. Nanoparticulate fingolimod delivery system based on biodegradable poly (3-hydroxybutyrate-co-3- hydroxyvalerate) (PHBV): design, optimization, characterization and in-vitro evaluation. Pharm Dev Technol, 2017, 12(7): 860–870. |
| [37] | Xiong YC, Yao YC, Zhan XY, et al. Application of polyhydroxyalkanoates nanoparticles as intracellular sustained drug-release vectors. J Biomat Sci Polym Ed, 2010, 21(1): 127–140. DOI: 10.1163/156856209X410283 |
| [38] | Scheithauer EC, Li W, Ding YP, et al. Preparation and characterization of electrosprayed daidzein-loaded PHBV microspheres. Mater Lett, 2015, 158: 66–69. DOI: 10.1016/j.matlet.2015.05.133 |
| [39] | Zhang JY, Shishatskaya EI, Volova TG, et al. Polyhydroxyalkanoates (PHA) for therapeutic applications. Mater Sci Eng C, 2018, 86: 144–150. DOI: 10.1016/j.msec.2017.12.035 |
| [40] | Parlane NA, Grage K, Lee JW, et al. Production of a particulate hepatitis C vaccine candidate by an engineered Lactococcus lactis strain. Appl Environ Microbiol, 2011, 77(24): 8516–8522. DOI: 10.1128/AEM.06420-11 |
| [41] | Sparks J, Scholz C. Evaluation of a cationic poly(β-hydroxyalkanoate) as a plasmid DNA delivery system. Biomacromolecules, 2009, 10(7): 1715–1719. DOI: 10.1021/bm900372x |
| [42] | Xiao XQ, Zhao Y, Chen GQ. The effect of 3-hydroxybutyrate and its derivatives on the growth of glial cells. Biomaterials, 2007, 28(25): 3608–3616. DOI: 10.1016/j.biomaterials.2007.04.046 |
| [43] | Cheng S, Wu Q, Yang F, et al. Influence of DL-β-hydroxybutyric acid on cell proliferation and calcium influx. Biomacromolecules, 2005, 6(2): 593–597. DOI: 10.1021/bm049465y |
| [44] | Sun J, Dai ZW, Zhao Y, et al. In vitro effect of oligo-hydroxyalkanoates on the growth of mouse fibroblast cell line L929. Biomaterials, 2007, 28(27): 3896–3903. DOI: 10.1016/j.biomaterials.2007.05.011 |
| [45] | Zhao Y, Zou B, Shi ZY, et al. The effect of 3-hydroxybutyrate on the in vitro differentiation of murine osteoblast MC3T3-E1 and in vivo bone formation in ovariectomized rats. Biomaterials, 2007, 28(20): 3063–3073. DOI: 10.1016/j.biomaterials.2007.03.003 |
| [46] | Zhang JY, Cao Q, Li SW, et al. 3-Hydroxybutyrate methyl ester as a potential drug against Alzheimer's disease via mitochondria protection mechanism. Biomaterials, 2013, 34(30): 7552–7562. DOI: 10.1016/j.biomaterials.2013.06.043 |
| [47] | Madbouly SA, Schrader JA, Srinivasan G, et al. Biodegradation behavior of bacterial-based polyhydroxyalkanoate (PHA) and DDGS composites. Green Chem, 2014, 16(4): 1911–1920. DOI: 10.1039/C3GC41503A |
| [48] | Arcos-Hernandez MV, Laycock B, Pratt S, et al. Biodegradation in a soil environment of activated sludge derived polyhydroxyalkanoate(PHBV). Polym Degrad Stabil, 2012, 97(11): 2301–2312. DOI: 10.1016/j.polymdegradstab.2012.07.035 |
| [49] | Hassan MK, Abou-Hussein R, Zhang XJ, et al. Biodegradable copolymers of 3-Hydroxybutyrate- co-3-Hydroxyhexanoate(NodaxTM): including recent improvements in their mechanical properties. Mol Cryst Liq Cryst, 2006, 447(1): 23/[341]–44/[362]. |
| [50] | Prudnikova SV, Boyandin AN, Sinskey AJ. Degradable polyhydroxyalkanoates as herbicide carriers. J Polym Environ, 2013, 21(3): 675–682. DOI: 10.1007/s10924-012-0561-z |
| [51] | Hoseinifar SH, Sun YZ, Caipang CM. Short‐chain fatty acids as feed supplements for sustainable aquaculture: an updated view. Aquac Res, 2017, 48(4): 1380–1391. DOI: 10.1111/are.13239 |
| [52] | Duan YF, Zhang Y, Dong HB, et al. Effect of dietary poly-β-hydroxybutyrate (PHB) on growth performance, intestinal health status and body composition of Pacific white shrimp Litopenaeus vannamei (Boone, 1931). Fish Shellfish Immun, 2017, 60: 520–528. DOI: 10.1016/j.fsi.2016.11.020 |
| [53] | Najdegerami EH, Baruah K, Shiri A, et al. Siberian sturgeon (Acipenser baerii) larvae fed Artemia nauplii enriched with poly-β-hydroxybutyrate (PHB): effect on growth performance, body composition, digestive enzymes, gut microbial community, gut histology and stress tests. Aquac Res, 2015, 46(4): 801–812. DOI: 10.1111/are.12231 |
| [54] | De Schryver P, Sinha AK, Kunwar PS, et al. Poly-β-hydroxybutyrate (PHB) increases growth performance and intestinal bacterial range-weighted richness in juvenile European sea bass, Dicentrarchus labrax. Appl Microbiol Biotechnol, 2010, 86(5): 1535–1541. DOI: 10.1007/s00253-009-2414-9 |
| [55] | Sui L, Cai J, Sun H, et al. Effect of poly‐β‐hydroxybutyrate on Chinese mitten crab, Eriocheir sinensis, larvae challenged with pathogenic Vibrio anguillarum. J Fish Dis, 2012, 35(5): 359–364. DOI: 10.1111/jfd.2012.35.issue-5 |
| [56] | Muhammadi, Shabina, Afzal M, et al. Bacterial polyhydroxyalkanoates-eco-friendly next generation plastic: production, biocompatibility, biodegradation, physical properties and applications. Green Chem Lett Rev, 2015, 8(3/4): 56–77. |
| [57] | Bourbonnais R, Marchessault RH. Application of polyhydroxyalkanoate granules for sizing of paper. Biomacromolecules, 2010, 11(4): 989–993. DOI: 10.1021/bm9014667 |
| [58] | Li LZ, Huang W, Wang BJ, et al. Properties and structure of polylactide/poly (3-hydroxybutyrate-co- 3-hydroxyvalerate)(PLA/PHBV) blend fibers. Polymer, 2015, 68: 183–194. DOI: 10.1016/j.polymer.2015.05.024 |
| [59] | Fortunati E, Luzi F, Yang WJ, et al. Bio-based nanocomposites in food packaging//Nanomaterials for Food Packaging. Amsterdam: Elsevier, 2018: 71–110. |
| [60] | Yu HY, Qin ZY, Sun B, et al. Reinforcement of transparent poly(3-hydroxybutyrate-co-3-hydroxyvalerate) by incorporation of functionalized carbon nanotubes as a novel bionanocomposite for food packaging. Compos Sci Technol, 2014, 94: 96–104. DOI: 10.1016/j.compscitech.2014.01.018 |
| [61] | Tappel RC, Pan WY, Bergey NS, et al. Engineering Escherichia coli for improved production of short-chain-length-co-medium-chain-length poly[(R)-3- hydroxyalkanoate] (SCL-co-MCL PHA) copolymers from renewable nonfatty acid feedstocks. ACS Sustain Chem Eng, 2014, 2(7): 1879–1887. DOI: 10.1021/sc500217p |
| [62] | Wei DX, Dao JW, Chen GQ. A micro‐ark for cells: highly open porous polyhydroxyalkanoate microspheres as injectable scaffolds for tissue regeneration. Adv Mater, 2018, 30(31): 1802273. DOI: 10.1002/adma.v30.31 |
| [63] | Zhang SS, Sun XB, Wang XM, et al. Bioaugmentation with Diaphorobacter polyhydroxybutyrativorans to enhance nitrate removal in a poly(3-hydroxybutyrate-co- 3-hydroxyvalerate)-supported denitrification reactor. Biores Technol, 2018, 263: 499–507. DOI: 10.1016/j.biortech.2018.04.115 |
 2018, Vol. 34
2018, Vol. 34