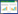中国科学院微生物研究所、中国微生物学会主办
文章信息
- 田德桥, 陈薇
- Deqiao Tian, Wei Chen
- 寨卡病毒及其疫苗研究
- Progress in Zika virus and its vaccines
- 生物工程学报, 2017, 33(1): 1-15
- Chin J Biotech, 2017, 33(1): 1-15
- 10.13345/j.cjb.160361
-
文章历史
- Received: September 28, 2016
- Accepted: November 8, 2016
寨卡病毒 (Zika virus) 和黄热病毒(Yellow fever virus) 、登革热病毒 (Dengueviruses)、日本脑炎病毒 (Japanese encephalitisvirus)和西尼罗病毒 (West Nile virus) 等都属于蚊媒传播的黄病毒属病毒。虽然1947 年就分离到病毒,但寨卡病毒之前并没有引起太多的关注,这一方面是由于其发病症状较轻微,再有是分布区域有限。但根据世界卫生组织 (WHO)公布的数据,自2007 年以来,截至2016 年11月2 日,有73 个国家或地区发生蚊媒传播的寨卡病毒感染,26 个国家或地区存在与寨卡病毒感染相关的新生儿小头畸形,19 个国家或地区存在与寨卡病毒感染相关的格林巴利综合征病例数增加[1]。根据泛美卫生组织 (PAHO) 的统计数据,截至2016 年11 月2 日,美洲地区2015到2016 年间的寨卡病毒本地感染疑似病例数51.5 万例,确诊病例16.8 万例[2]。世界卫生组织2016 年2 月1 日宣布寨卡病毒为全球紧急公共卫生事件。并且,寨卡病毒所致寨卡热有进一步全球蔓延的趋势。2016 年11 月,《柳叶刀·传染病》期刊刊登的一项研究列出了8 个寨卡病毒传播风险最大的亚洲和非洲国家,印度和中国排在前两位[3]。
疫苗是感染性疾病应对至关重要的一种手段,近些年包括SARS、H1N1 流感、埃博拉出血热等新发和再发传染病疫情发生后,全球很多机构都开展了相应的疫苗研发,寨卡病毒也不例外。当前全球有近30 个研究机构正在进行寨卡病毒疫苗研发。寨卡病毒疫苗研发是一项具有挑战性的工作,黄病毒属的其他几种病毒有些已有批准的疫苗,有些虽进行了多年的研发,但尚没有批准的人用疫苗。
本文在对寨卡病毒生物学特征、流行情况及临床特征概述的基础上,重点分析了当前全球寨卡疫苗研发现状,并对其他几种黄病毒属病毒疫苗的研发历史与现状进行了综述。
1 Zika 病毒概述 1.1 生物学寨卡病毒按病毒学分类属于黄病毒科 (Flaviviridae) 的黄病毒属 (Flavivirus)。黄病毒科病毒主要感染哺乳类动物,为单股线型RNA,包括3 个病毒属: 黄病毒属、瘟病毒属(Pestivirus) 和丙型肝炎病毒属 (Hepacivirus)。黄病毒属包括黄热病毒、登革热病毒、日本脑炎病毒、西尼罗病毒、蜱传脑炎病毒 (Tick-borneencephalitis viruses)和寨卡病毒等。
黄热病毒分布于南美洲和非洲的热带和亚热带地区,由埃及伊蚊Aedes aegypti 传播。世界卫生组织估计黄热病毒每年导致20 万病例,3 万人死亡,其中大多数在非洲[4]。
登革热病毒分布于亚洲、太平洋、美洲、非洲的至少100 多个国家,由埃及伊蚊和白纹伊蚊Aedes albopictus 传播,有4 种血清型。现在全球大约25 亿人口生活在登革热流行区域。世界卫生组织估计每年有5 000 万到1 亿的感染者,导致2.2 万人死亡。
日本脑炎病毒分布于亚洲和西太平洋地区,三带喙库蚊Culex tritaeniorhynchus 是主要传播媒介。日本脑炎每年可导致大约67 900 病例,20 400 人死亡[4]。
蜱传脑炎病毒在自然界的一些哺乳动物,尤其是啮齿动物间传播,蜱虫为传播媒介。蜱传脑炎病毒包括3 种基因型:欧洲型 (TBEV-Eu),分布于整个欧洲地区;远东型 (TBEV-Fe),分布于中国、日本和俄罗斯东部; 西伯利亚型(TBEV-Si),分布于西伯利亚和俄罗斯的一些地区。蜱传脑炎在全球每年大约有6 000 至12 000的报告病例,各型的病死率分别为TBEV-Fe≥20%,TBEV-Si 6%-8%,TBEV-Eu 1%-2%[4]。
西尼罗病毒广泛分布于非洲、欧洲、亚洲、澳大利亚和美洲地区,主要通过库蚊传播,可感染人和马等。在美国,1999 到2012 年间,有3.7 万西尼罗病毒病例发生,其中1 549 人死亡,病死率为4.2%[5]。
寨卡病毒1947 年在乌干达的猴体内分离,1948 年从同一地区的非洲伊蚊Aedes africanus分离到病毒[6]。2007 年之前,虽然寨卡病毒分布于非洲和亚洲的一些地区,但在全球范围内仅有14 例报道病例,其中13 例自然感染,1 例实验室感染[6]。
寨卡病毒是有包膜的球状病毒,属于蚊媒传播的黄病毒属病毒,斯庞德温尼病毒血清群。伊蚊的很多型具有潜在传播寨卡病毒的能力,但埃及伊蚊和白纹伊蚊由于分布区域广受到广泛关注[6]。
寨卡病毒和其他黄病毒一样,为单股正链RNA,长11 kb,基因组编码一个开放读码框(Open reading frame,ORF),包括3 种结构单位和7 种非结构蛋白 (图 1)[6-7]。黄病毒结构蛋白包括核衣壳蛋白C、包膜糖蛋白E 和prM/M,E蛋白与病毒进入、组装、出芽有关,是中和抗体首要的目标蛋白,几乎所有针对黄病毒属病毒的疫苗都包括E 抗原[4]。非结构蛋白 (NS1,NS2A,NS2B,NS3,NS4A,NS4B,NS5) 参与病毒的复制、组装等[7]。NS1 蛋白是寨卡病毒一个重要的致病因子[8]。
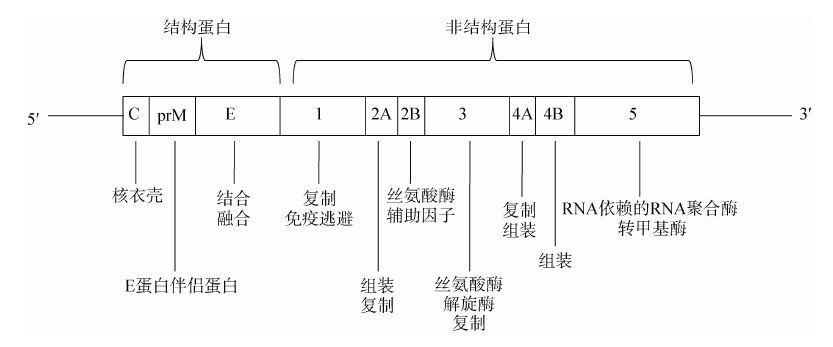
黄病毒属病毒通过受体介导的内吞作用进入细胞,形成内体,此后病毒膜与内体发生pH依赖的膜融合。病毒基因组释放入细胞质,在宿主细胞翻译系统作用下进行蛋白翻译。病毒基因组编码多聚蛋白 (大约3 400 个氨基酸)。多聚蛋白被宿主蛋白酶和病毒编码的NS2B/NS3 蛋白酶切割成3 个结构蛋白和7 个非结构蛋白。病毒非结构蛋白参与病毒复制。在病毒出芽前,prM 蛋白被细胞丝氨酸酶切割,成为M 蛋白。感染性病毒颗粒通过胞吐作用释放[7] (图 2)。研究表明磷脂酰丝氨酸受体AXL 是寨卡病毒进入细胞过程中一种重要的受体[9]。
基于蛋白质和核酸序列分析,寨卡病毒至少包括两个主要的遗传谱系:非洲谱系和亚洲谱系[10]。寨卡病毒被认为主要在自然界中的非人灵长类和蚊媒之间丛林传播,人偶尔感染,也可在人群之间传播[6]。寨卡病毒主要通过感染的蚊媒叮咬在人群中传播,但也存在性传播、母婴传播、输血传播的可能性[11]。
1.2 流行情况寨卡病毒首先分离于1947 年乌干达的猕猴,1948 年从非洲伊蚊分离到病毒。随后在非洲、印度和东南亚地区人群中检测到寨卡病毒抗体[12]。人感染寨卡病毒首先发现于1953 年的尼日利亚。1966 年首次在亚洲马来西亚的埃及伊蚊分离到寨卡病毒。
在非洲和亚洲以外,2007 年首次在西太平洋的Yap 岛暴发了寨卡疫情。在这次暴发中,有49 例确诊和59 例疑似的寨卡病毒感染病例[13]。Yap 岛的寨卡疫情暴发之后,在东南亚地区有寨卡病毒感染零星病例,如2010 年在柬埔寨、2012年在菲律宾发现寨卡病毒感染病例。
2013 年10 月,在法属波利尼西亚群岛暴发寨卡疫情。一年时间内,有1.9 万疑似病例[14]。序列分析表明在波利尼西亚的寨卡病毒与2010年在柬埔寨,2007 年在Yap 岛的病毒序列类似,属于亚洲谱系。随后的序列分析表明,其较Yap岛的病毒株,更加接近于在东南亚的病毒株[6]。本次疫情感染了当地66%的居民。并且,2013年11 月到2014 年2 月间有42 例格林巴利综合征的发生,而在整个2012 年只有3 例[14]。
此后,寨卡病毒在南太平洋地区传播。最早证实的寨卡病毒在美洲出现于2014 年末,在巴西东北部,并在巴西迅速传播[15]。进化分析表明,导致该暴发的病毒株来源于南太平洋地区,属于亚洲谱系[16]。到2016 年6 月,在美洲地区有超过35 个国家报道了寨卡病毒的地区传播[17]。
1.3 临床特征寨卡病毒感染症状较轻,一般在感染6 d 后发病,95%的感染者在11 d 内发病[12]。在Yap岛报告的31 例确诊病例中,主要症状包括:斑丘疹 (90%)、发热 (65%)、关节痛或关节炎(65%)、非化脓性结膜炎 (55%)、肌痛 (48%)、头痛 (45%)、眼窝疼痛 (39%)、水肿 (19%)和呕吐 (10%) 等[13]。
在波利尼西亚的感染者大约出现70 例格林巴利综合征[18],其他一些严重症状包括脑膜脑炎、脊髓炎等。在波利尼西亚,寨卡疫情暴发期间,格林巴利的发生率为2.4×10-4[14],而美国每年的发生率为1.8×10-5[19]。
另外,巴西的寨卡疫情暴发与新生儿小头畸形病例数增加相关联,较之前增加了20 倍[20]。从寨卡病毒出现到2016 年5 月7 日,在巴西有7 438 例疑似小头畸形病例报告,而在暴发前每年的病例数少于200 例[21]。动物模型研究进一步证实了小头畸形与寨卡病毒感染的关联[22-23]。
2 Zika 疫苗研究进展疫苗是应对寨卡疫情的重要手段。目前,全球有近30 个研究机构在进行寨卡疫苗的研发(表 1)。
| Country | Institutes | Vaccine type | Location |
| DNA疫苗 减毒活疫苗(与巴西Butantan合作) | |||
| NIAID | 水泡口炎病毒(VSV)载体疫苗 灭活疫苗 自复制RNA疫苗(与GSK合作) | Bethesda,马里兰州 | |
| Walter Reed Army Institute of Research | 灭活疫苗(与赛诺菲•巴斯德合作) | Spring,马里兰州 | |
| Harvard University | DNA疫苗 腺病毒载体疫苗 | 波士顿,马萨诸塞州 | |
| Inovio Pharmaceuticals | DNA疫苗(与韩国Gene one life合作) | Plymouth Meeting,宾夕法尼 亚州 | |
| 美国 | Emergent BioSolutions | / | Gaithersburg,马里兰州 |
| GeoVax | MVA-VLP疫苗(与乔治亚大学和CDC合作) | 亚特兰大,乔治亚州 | |
| Hawaii Biotech | 昆虫细胞表达亚单位疫苗 | 擅香山,夏威夷州 | |
| Infectious Disease Research Institute | RNA疫苗 | 西雅图,华盛顿州 | |
| Moderna Therapeutics | RNA疫苗 | Cambridge,马萨诸塞州 | |
| NewLink Genetics | 灭活疫苗 | Ames,爱荷华州 | |
| PaxVax | / | Redwood City,加利福尼亚州 | |
| Protein Sciences | 重组疫苗(与阿根廷Sinergium Biotech合作) | Meriden,康捏狄格州 | |
| Replikins | 合成疫苗 | 波士顿,马萨诸塞州 | |
| Texas Universities | /(与巴西 Evandro Chagas 合作) | Galveston,德克萨斯州 | |
| University of Connecticut | 痘苗病毒载体疫苗 | Storrs,康涅狄格州 | |
| VaxInnate | 融合蛋白疫苗 | Cranbury,新泽西州 | |
| Bio-Manguinhos | 灭活疫苗 | 里约热内卢 | |
| 巴西 | Instituto Butantan | 灭活疫苗 | 圣保罗 |
| Evandro Chagas Institute | /(与美国德克萨斯大学合作) | 贝伦 | |
| 阿根廷 | Sinergium Biotech | 重组疫苗(与Protein Sciences合作) | Buenos Aires |
| 印度 | Bharat Biotech | 灭活疫苗 重组疫苗 | Hyderabad |
| 曰本 | Takeda Pharmaceutical | 灭活疫苗 | 大阪 |
| 法国 | Sanofi Pasteur | 灭活疫苗(与美国华尔特里德陆军研究所合作) | 巴黎 |
| Valneva | 灭活疫苗 | 里昂 | |
| 奥地利 | Themis Bioscience | 麻疹病毒载体疫苗 | 维也纳 |
| 英国 | Jenner Institute | 腺病毒载体疫苗 | 牛津 |
| 澳大利亚 | Sementis | 痘苗病毒载体疫苗 | 里士满 |
病毒类灭活疫苗是一种经典的疫苗形式,也是一种易于快速研发和制备的有效疫苗。过去的经验表明,一旦有病毒性传染病发生时,人们在考虑研发病毒疫苗时,优先选择的是灭活疫苗[24]。病毒类灭活疫苗是指病毒经适当的方法进行批量培养、灭活和处理之后制备而成的。
日本脑炎病毒分离于1935 年,第一种日本脑炎疫苗是一种鼠脑来源的灭活疫苗,1954 年在日本研发[4]。鼠脑来源疫苗在韩国、印度、中国、泰国、越南等地生产[4]。由于鼠脑细胞疫苗潜在的安全问题,细胞培养的疫苗被研发。2009年,两种Vero 细胞来源的灭活疫苗被批准。其中IXIARO 由奥地利Intercell AG 公司 (现属于法国Valneva SE 公司) 研发,JEBIKV 由日本BIKEN 公司研发[4]。另外一种Vero 细胞来源的灭活疫苗ENCEVAC 由日本Kaketsuken 研究所研发,2011 年获得批准[4]。
蜱传脑炎病毒在1937 年被分离。第一个蜱传脑炎疫苗FSME-IMMUN 由奥地利Baxter AG公司研发,是鸡胚细胞来源的灭活疫苗,在奥地利1976 年被批准[4]。FSME-IMMUN 主要针对TBEV-Eu[4]。Encepur 由Chiron Behring 公司研发,现属于瑞士诺华公司,为鸡胚细胞来源的灭活疫苗,疫苗株来源于TBEV-Eu,1991 年批准,主要针对TBEV-Eu[4]。另外两种疫苗在俄罗斯和前苏联一些共和国使用。TBE-Moscow由俄罗斯脊髓灰质炎和脑炎研究所研发,也是一种鸡胚来源的灭活疫苗,针对TBEV-Fe,1982年批准。EnceVir 由俄罗斯Microgen 公司研发,同样是鸡胚来源的灭活疫苗,2001 年批准,针对TBEV-Fe[4]。
登革热病毒4 价灭活疫苗由葛兰素史克(GSK) 以及美国华尔特里德陆军研究所(WRAIR) 联合研发,病毒在Vero 细胞培养,在美国和波多黎各完成了Ⅰ期临床试验[4]。
第1 种批准的兽用西尼罗病毒疫苗WESTNILE-INNOVATOR 是一种灭活疫苗,由美国Dodge Animal Health 研发,2001 年批准。
鸡蛋培养来源的黄热病毒减毒活疫苗存在一定的副作用。为此,Vero 细胞来源的灭活疫苗被研发。XRX-001 是一种黄热病毒灭活疫苗,由美国Xcellerex 公司研发,Vero 细胞培养,β丙内酯灭活,该疫苗完成了Ⅰ期临床试验[25]。
华尔特里德陆军研究所基于其他黄病毒属病毒灭活疫苗的研发经验和技术进行了寨卡病毒灭活疫苗研究。病毒株PRVABC59 来源于波多黎各。在小鼠试验中,小鼠接受疫苗的单次肌肉和皮下注射。经检测,肌肉注射的小鼠较皮下注射的小鼠抗体滴度高。在疫苗接种4 周后的攻毒试验中,肌肉注射的小鼠100%观察到保护作用,皮下注射组有2 只小鼠存在低水平的病毒血症[26]。在非人灵长类动物实验中,灭活疫苗免疫了8 只恒河猴,在0 和4 周分别进行皮下疫苗接种,所有的受试恒河猴均产生了特异性的抗体。在寨卡病毒攻毒试验中,免疫的恒河猴全部产生了保护作用,在血液、尿液等中未检测到病毒[27]。2016 年7 月,法国赛诺菲·巴斯德公司与华尔特里德陆军研究所达成一项合作研发协议,开发寨卡病毒灭活疫苗。该灭活疫苗Ⅰ期临床试验计划在2016 年年底进行。
法国Valneva 公司2016 年7 月宣布其正在研发一种灭活的针对寨卡病毒的疫苗,其使用与日本脑炎疫苗相同的研发平台。Valneva 公司的日本脑炎灭活疫苗已经被美国FDA、欧盟等批准。
2016 年9 月,美国卫生与公众服务部 (HHS)资助日本武田 (Takeda) 公司在美国伊利诺伊州的子公司1 980 万美元进行寨卡疫苗的研发,用于在美国的使用。该疫苗是一种灭活疫苗,含
有佐剂。Takeda 是日本最大的制药公司,具有登革热病毒、基孔肯亚病毒、诺瓦克病毒、脊髓灰质炎病毒和大流行流感病毒的疫苗研发基础。
Bharat Biotech 位于印度的海得拉巴(Hyderabad),其开展了包括灭活疫苗在内的寨卡病毒疫苗研究。
巴西免疫生物技术研究所 (Bio-Manguinhos)属于奥斯瓦尔多·克鲁斯基金会 (Oswaldo CruzFoundation,Fiocruz),成立于1976 年,致力于发展疫苗和生物制品。2001 年,该研究所通过了世界卫生组织作为其提供黄热疫苗的预认证。Bio-Manguinhos 正在开展寨卡病毒灭活疫苗的研究。
Instituto Butantan 是巴西免疫生物制品研发、生产的一个主要机构,其正在开展寨卡病毒灭活疫苗研究。
美国NewLink 公司2005 年成立,2014 年其与默克公司合作进行了埃博拉疫苗的研究。NewLink 计划进行寨卡病毒灭活疫苗的研发。
2.2 减毒活疫苗减毒活疫苗是病毒疫苗研发的一个重要方向。防病效果较好的痘苗 (天花疫苗)、麻疹疫苗、脊髓灰质炎疫苗以及腮腺炎、风疹、水痘等疫苗均属于减毒活疫苗。减毒活疫苗接种次数少,获得的免疫力较持久[24]。
黄热病毒1927 年分离,此后开始疫苗的研发[4]。研究人员在英国 (1928 年)、巴西 (1929年) 和法国 (1931 年) 等进行了灭活疫苗的一些尝试,但均不能产生足够的保护作用。17D疫苗是黄热病毒减毒活疫苗,从加纳的一名患者分离获得,该病毒株在鼠胚组织传代18 代,鸡胚组织传代58 代,去除脑和神经组织的鸡胚传代100 代,在176 代被命名为17D。1937 年,17D 疫苗开始在人体进行试验。当前,17D 疫苗有3 个亚株用于疫苗生产,17D-204 疫苗几乎在全球各个国家使用,17DD 疫苗在巴西使用,德国的罗伯特科赫研究所在20 世纪80 年代建立了17D-204 的1 个新的病毒种,被称为17D-213[28]。17D-204 疫苗在法国、塞内加尔、美国、荷兰、英国、德国、印度和中国生产,17DD 疫苗在巴西和哥伦比亚生产,17D-213 疫苗在尼日利亚和俄罗斯生产[28]。我国批准的黄热病毒减毒活疫苗由北京天坛生物制品股份有限公司生产,毒种源自17D-204 株。
1988 年,一种减毒的日本脑炎 (乙型脑炎)疫苗在中国研发成功,其替代了1968 年以来使用的地鼠肾来源的灭活疫苗[4]。该疫苗株病毒SA14-14-2 的母株SA14 是1954 年从西安一种库蚊幼虫分离得到的,在小鼠脑内传代11 代,在地鼠肾细胞传代100 代,以及在小鼠腹腔、乳鼠皮下传代等获得。对SA14-14-2 弱毒株和强毒株的基因分析显示,两者之间存在57−66个核苷酸差别,导致24−31 个氨基酸发生改变,其中以外膜E 蛋白突变率最高,有8 个氨基酸发生了突变。经试验证实该8 个氨基酸突变与毒力减弱密切相关。该乙型脑炎减毒活疫苗1989年获新药证书并由成都生物制品研究所生产。该疫苗除在国内大规模应用外,近年来已出口到韩国、尼泊尔、印度和泰国等国。大量人群应用后表明疫苗十分安全[24]。该疫苗于2013 年10 月9日通过了世界卫生组织的预认证。
对于登革热病毒,之前存在的针对一种血清型的抗体可以加重另外一种血清型登革热病毒感染的症状,这种机制称为抗体依赖的感染增强效应 (Antibody-dependent enhancement,ADE)[29]。流行病学研究表明首次感染一种登革热病毒血清型后,再感染另外一种血清型后的严重病理反应是首次感染的15−80 倍[4]。因此有效的登革热疫苗应当是4 价疫苗。第1 种进入临床试验的4 价登革热疫苗是一种传统的减毒疫苗,由泰国玛希隆大学 (Mahidol University)研发,后授权给赛诺菲·巴斯德公司。其在狗和猴的肾脏细胞进行传代减毒。另一种传统的减毒活疫苗由美国华尔特里德陆军研究所研发,授权给葛兰素史克公司,在狗肾细胞和猴肺细胞传代减毒。这些疫苗单价使用时可以产生很好的免疫效果,但是当这些疫苗4 价使用时,之间的干扰是面临的一个巨大问题[4]。因此,赛诺菲·巴斯德的疫苗Ⅱ期临床试验终止[4]。葛兰素史克的疫苗当前处于Ⅱ期临床试验阶段。
目前,对于寨卡病毒疫苗没有传统的减毒活疫苗研发报道。
2.3 嵌合病毒疫苗基因工程技术可以发展嵌合病毒疫苗,如赛诺菲·巴斯德公司针对登革热的Dengvaxia 疫苗,其包括登革热各种血清型来源的prM/E 基因,替代黄热病毒疫苗株YFV-17D 的相应基因[30]。赛诺菲·巴斯德公司的嵌合病毒登革热疫苗三期临床实验在拉丁美洲的巴西、哥伦比亚、墨西哥、洪都拉斯、波多黎各等地以及亚洲的印度尼西亚、马来西亚、菲律宾、泰国、越南等地进行。2015 年,墨西哥和菲律宾先后批准了该疫苗,使其成为全球第1 个批准的登革热疫苗。截至2016 年6 月,该疫苗已经被墨西哥、菲律宾、巴西、萨尔瓦多、哥斯达黎加等5 个国家批准,世界卫生组织也推荐在登革热流行地区使用该疫苗。另外一种登革热嵌合病毒4 价疫苗DENVax 由美国CDC、美国Viragen 公司、日本Takeda 公司联合研发,其使用减毒的2 型登革热病毒株作为疫苗骨架,其他登革热血清型的prM/E基因代替登革热2 型减毒株的相应基因[4]。该疫苗的Ⅱ期临床试验在波多黎各、哥伦比亚、新加坡和泰国进行。
日本脑炎嵌合病毒疫苗由赛诺菲·巴斯德公司研发,其包含日本脑炎病毒的prM/E 基因,替代了黄热病毒疫苗株YFV-17D 的相应基因,用Vero 细胞培养。2010 年,该疫苗在澳大利亚和泰国获得批准[4]。
赛诺菲·巴斯德公司基于黄热病毒疫苗株YFV-17D 研发的西尼罗病毒嵌合病毒疫苗表达西尼罗病毒的prM/E 基因[31],完成了Ⅱ期临床试验。美国过敏与感染性疾病研究所 (NIAID)研发的西尼罗病毒嵌合病毒疫苗基于4 型登革热病毒骨架,表达西尼罗病毒prM 和E 蛋白,完成了Ⅰ期临床试验[5]。
NIAID 与巴西的Butantan 研究所合作,正在研发一种寨卡病毒减毒活疫苗,其基于嵌合疫苗技术,将寨卡病毒保护性抗原嵌合入登革热病毒疫苗株。
2.4 核酸疫苗核酸疫苗是指使用能够表达抗原的基因本身,即核酸制成的疫苗。核酸疫苗的显著特点是疫苗制剂的主要成分不是基因表达产物,而是基因本身[24]。目前已有常规技术很难研制的3种兽用DNA 疫苗上市,包括2005 年美国农业部批准的辉瑞公司下属的Fort Dodge AnimalHealth 公司研发的西尼罗病毒DNA 疫苗等[24]。
美国海军医学研究中心和Vical Inc 公司联合研发的D1ME100 是一种包含登革热病毒的prM/E基因的单价登革热DNA 疫苗,已完成了Ⅰ期临床试验。
目前,没有批准的人用西尼罗病毒疫苗。第1 个进入临床试验的人用西尼罗病毒疫苗是一种DNA 疫苗,其编码西尼罗病毒的prM 和Env 蛋白,由加利福尼亚Vical 公司和NIAID 联合研发,开展了Ⅰ期临床试验[32]。
美国Inovio 公司和韩国Gene One LifeScience 公司合作开发寨卡病毒DNA 疫苗GLS5700,其针对寨卡病毒包膜prM 和E 蛋白。Inovio 公司2016 年2 月宣布该疫苗在小鼠试验取得了很好的效果,5 月宣布其在猴的实验中取得了很好的效果,在两剂疫苗接种后,所有的受试猴血液中均检测到特异的抗体。该DNA 疫苗在2016 年6 月份获得FDA 批准进行人体试验。在40 人的临床试验中,主要试验该疫苗的不同剂量,评价安全性、免疫原性。Inovio 公司基于电穿孔的DNA 递送设备Cellectra 将被用于疫苗接种。2016 年8 月29 日,Inovio 宣布将在波多黎各开始160 人的寨卡疫苗临床试验。
NIAID 研发的寨卡病毒DNA 疫苗在小鼠和恒河猴动物试验中表现出了很好的效果。该疫苗来源于巴西的寨卡病毒分离株 (BeH815744),采用prM-Env 作为疫苗抗原,但缺失了prM 起始端的93 个氨基酸序列,该序列在病毒自然感染过程中被切除[33]。该疫苗2016 年8 月开始在美国国立卫生研究院 (NIH) 疫苗研究中心、马里兰大学和埃默里大学开展Ⅰ期临床试验。试验包括80 名18-35 岁的志愿者,评价了疫苗的安全性和免疫原性。试验结果显示该疫苗安全且可诱导有效的免疫反应。
哈佛大学研发的寨卡病毒DNA疫苗基于巴西来源寨卡病毒株 (BeH815744),在小鼠试验中,小鼠接受单剂的含有寨卡病毒prM-Env 成分的DNA 疫苗肌肉接种,3 周后检测到较高的抗体滴度。在免疫4 周后进行寨卡病毒攻毒试验。疫苗接种的小鼠具有100%的保护,未发现病毒血症[26]。在非人灵长类动物试验中,该DNA疫苗免疫了12 只恒河猴,疫苗在0 和4 周进行肌肉注射,所有受试恒河猴均检测到特异性中和抗体。在攻毒试验中,疫苗对所有的受试猴均产生保护作用[27]。
NIAID在2016 年7 月宣布与葛兰素史克合作发展一种基于甲病毒的自复制寨卡病毒mRNA疫苗。DNA 疫苗需要进入细胞核,而mRNA 疫苗仅需要进入细胞质。
马萨诸塞州剑桥的Moderna Therapeutics 公司研发的寨卡病毒疫苗是基于mRNA 的疫苗,可以通过机体产生免疫原性蛋白,刺激机体的免疫系统。2016 年9 月,美国生物医学高级研究与发展计划局 (BARDA) 与ModernaTherapeutics 公司签订了820 万美元的合同,加速寨卡疫苗的研发。根据4 年的合同,BARDA将支持疫苗Ⅰ期临床试验。如果进展顺利,合同可延长到5 年,包括1.255 亿美元支持Ⅱ期和Ⅲ期临床试验。
另外,位于美国西雅图的感染性疾病研究所 (Infectious disease research institute) 正在开展寨卡病毒RNA 疫苗的研究,该研究得到了NIAID 的资助。
2.5 载体疫苗载体疫苗是指利用微生物作为载体,将保护性抗原基因重组到微生物载体制成的疫苗。根据在人体内繁殖的特点,载体疫苗可分为复制型和非复制型两类。
Meria 公司 (现属于赛诺菲·巴斯德公司)研发的马用西尼罗病毒疫苗Recombitek®Equine WNV 在2004 年获得批准,其通过金丝雀痘病毒表达西尼罗病毒的的prM/E。
奥地利的Themis Bioscience 公司正在研发麻疹病毒载体寨卡病毒疫苗,寨卡病毒相关抗原基因插入麻疹病毒基因组,麻疹病毒直接将抗原递送到巨噬细胞和树突状细胞产生针对寨卡病毒的免疫反应。Themis Bioscience 公司有研发基孔肯雅病毒和登革热病毒疫苗的经验,其麻疹疫苗载体技术平台从巴斯德研究所获得授权。
NIAID 正在研发水泡性口炎病毒 (VSV)作为载体的寨卡病毒疫苗,NIAID 用该技术研发了埃博拉疫苗。
哈佛大学进行了52 型猴腺病毒载体 (Rhesusadenovirus serotype 52,RhAd 52) 寨卡病毒疫苗的研究,其在非人灵长类动物试验取得了较好的效果,疫苗免疫了12 只恒河猴,1 次接种,在2 周后均检测到特异性中和抗体,免疫4 周后进行攻毒试验,疫苗对所有的受试猴均产生保护作用[27]。
英国Jenner 研究所的寨卡病毒疫苗通过猿腺病毒载体 (Simian adenoviral vector) 表达寨卡病毒结构蛋白。猿腺病毒载体疫苗较人腺病毒载体疫苗的优势在于针对载体的人群预存免疫较弱。另外Jenner 研究所的猿腺病毒载体寨卡病毒疫苗在人体内不复制,其复制作用的基因被寨卡病毒的结构蛋白所代替。
澳大利亚Sementis 公司使用复制缺陷的痘苗病毒载体平台研发疫苗,其将病原体抗原插入到复制缺陷的痘苗病毒载体。当前,其正在利用该技术进行寨卡病毒疫苗的研发。
美国康涅狄格大学也正在开展基于复制缺陷型痘苗病毒载体的寨卡病毒研究,该研究获得了NIAID 的资助。
2.6 亚单位疫苗基因工程亚单位疫苗是指将基因工程表达的蛋白抗原纯化后制成的疫苗。至今,正在研发的人用基因工程亚单位疫苗至少有几十种,已研制成功并注册上市的有基因工程乙型肝炎疫苗、基因工程人乳头瘤疫苗和基因工程戊型肝炎疫苗等[24]。
美国夏威夷生物技术公司 (现属于默克公司) 成立于1982 年,位于檀香山。夏威夷生物技术公司用昆虫细胞表达重组蛋白。当前研发的疫苗包括西尼罗病毒疫苗、蜱传脑炎疫苗、寨卡病毒疫苗、刚果克里米亚出血热病毒疫苗和基孔肯雅病毒疫苗。夏威夷生物技术公司研发的登革热疫苗通过果蝇S2 细胞表达4 种登革热病毒的全长prM 及80%的E 蛋白,其优点是可以减少不同型疫苗接种的干扰,该疫苗已经完成了Ⅰ期临床试验[4]。其研发的西尼罗病毒亚单位疫苗由果蝇S2 细胞表达,基于E 蛋白,已完成Ⅰ期临床试验[5]。目前该公司正在进行寨卡病毒亚单位疫苗的研发。
Protein Sciences 公司位于美国康涅狄格州的梅里登,使用基因工程杆状病毒昆虫细胞表达技术研发针对流感及其他疾病的疫苗。2013年,美国FDA 批准了其Flublok 流感疫苗。
Protein Sciences 公司正在与阿根廷Sinergium 公司合作进行寨卡病毒疫苗研发。Sinergium 公司提供Protein Sciences 公司研发生产资金,Sinergium 公司获得该疫苗在阿根廷商业化的权利。该疫苗为重组E 蛋白疫苗。
VaxInnate 公司位于美国新泽西州,进行细菌鞭毛蛋白融合蛋白疫苗研究,其可以刺激机体先天免疫系统。该平台可以显著提高疫苗的免疫原性和有效性。该公司正在NIAID 资助下进行寨卡病毒融合蛋白疫苗研发。
2.7 病毒样颗粒疫苗近年来发现一些病毒仅表达病毒的部分结构蛋白就可以在细胞内装配成病毒样颗粒(Virus like particle,VLP),病毒样颗粒通常由两个或更多的蛋白组成,为不含病毒核酸的空壳结构,这种空壳表面有构象依赖表位,如果单独表达这些蛋白往往不能形成这类表位[34]。病毒样颗粒疫苗具有模拟天然病毒的结构,但是没有病毒基因组,更为安全[35]。乙肝和人乳头瘤病毒样颗粒疫苗已经批准,其他正在研发的病毒样颗粒疫苗针对的病原体包括流感病毒、细小病毒和诺瓦克病毒等[35]。
美国GeoVax 公司2001 年成立于乔治亚州亚特兰大,目前正在进行艾滋病疫苗的Ⅱ期临床试验。GeoVax 公司使用改良的痘苗病毒载体平台 (Modified vaccinia virus ankara—virus likeparticle,MVA-VLP) 进行疫苗研发。GeoVax研发的疫苗包括针对HIV、埃博拉病毒、马尔堡病毒和拉沙病毒等。2016 年2 月,GeoVax宣布与乔治亚大学和CDC 合作基于MVA-VLP疫苗平台进行寨卡病毒疫苗的研发。该疫苗在被接种者的细胞表达自组装非感染的病毒样颗粒。
2.8 合成肽疫苗合成肽疫苗是指将化学合成的多肽作为疫苗,这些多肽序列根据病毒的保护性抗原设计。对病毒保护性抗原的生物信息学分析,可以提供对保护性抗原结构在分子水平上的解析[34]。
美国Replikins 公司基于软件分析技术研发寨卡病毒合成肽疫苗。合成肽疫苗可以产生新的、目标特异性的多肽序列,保护作用更为有效,且相对传统疫苗具有较低的副作用。
另外,2016 年6 月,BARDA 与总部位于马里兰州的Emergent Biosolutions 公司签订了2 200 万美元为期30 个月的合同,进行寨卡病毒疫苗的研究,该疫苗预计在2017 年进行临床试验。
3 展望2015 年12 月,世界卫生组织基于埃博拉疫情应对的教训,组织专家讨论最需加强应对研发的病原体清单,确定了8 种最危险病原体及3种次危险病原体,其中寨卡病毒为3 种次危险病原体之一。
疫苗研发是应对感染性疾病的重要手段,但面临巨大挑战,很多新发及生物威胁病原体目前尚没有理想的疫苗。这一方面与对病原体特点认识不是非常清楚有关,同时与一些商业公司从利润考虑不愿全力投入研发有关[36]。另外疫苗研发需要进行详细的安全性和有效性评估,包括大范围人群接种的风险和收益分析。特别是对可导致神经系统疾病及具有神经致畸效应的病原体[37]。
值得庆幸的是,与登革热疫苗不同,在小鼠的研究表明,虽然存在遗传差异,但所有的寨卡病毒具有相同的血清型[38]。研究人员从在南美洲地区感染寨卡病毒的人群中提取血清,将其与实验室中不同寨卡病毒株混合观察抗体对病毒的中和作用,结果表明其可同时中和亚洲谱系以及非洲谱系的寨卡病毒株[38]。这可以避免疫苗研发中不同型疫苗同时接种相互干扰的问题。
近期,寨卡病毒中和抗体作用位点方面的一些研究进展可以为安全有效的寨卡病毒疫苗研发提供支持。研究表明,寨卡病毒E 蛋白与其他黄病毒属病毒的同源性较高[39]。在对登革热病毒等黄病毒属病毒E 蛋白的研究中,发现其存在3 个结构域。结构域I 与病毒入胞的构象变化有关,结构域Ⅱ 与膜融合有关,结构域Ⅲ与病毒与细胞受体结合有关[40]。结构域Ⅲ 在之前一些黄病毒属病毒疫苗和抗体研究中被应用[41-42]。我国科研人员研究确定了寨卡病毒E蛋白的晶体结构,发现与其他黄病毒属病毒类似,其具有明确的3 个结构域[43]。一些研究认为,寨卡病毒膜蛋白E 的结构域Ⅲ 是特异性中和抗体的结合位点,是寨卡病毒抗体和疫苗研发的重要靶点[44]。另外一些研究表明,针对寨卡病毒E 蛋白结构域Ⅲ 的抗体中和特异性高,而针对I/Ⅱ 结构域的抗体可以产生交叉反应,中和特性较弱,并且可能与潜在的感染增强有关[45]。
近期一些研究表明寨卡病毒和登革热病毒具有共同的中和表位,认为接种登革热病毒疫苗可能会对寨卡病毒具有保护作用[46]。另外一些体外细胞实验表明,登革热病毒的免疫血清与寨卡病毒有交叉反应,并且可以产生寨卡病毒抗体依赖的感染增强效应 (ADE),表明登革热病毒抗体具有潜在的增强寨卡病毒复制的作用。这对于寨卡病毒疫苗研发带来了更为复杂的问题,需要考虑到登革热病毒与寨卡病毒免疫血清交叉反应的问题。包括寨卡病毒疫苗免疫后潜在促进登革热病毒感染以及登革热病毒疫苗免疫后潜在促进寨卡病毒感染的作用,需要进一步明确交叉反应抗体起到保护作用还是潜在增强病毒的致病性[47-48]。一些研究人员认为登革热在中美洲和南部美洲地区流行了超过30 年,与当前寨卡疫情暴发可能存在一定的关联[12]。但目前尚无明确的流行病学证据表明在当前的寨卡疫情中,登革热病毒抗体的负面作用[49]。对于这个问题需要更为深入的动物模型试验研究,以及流行病学研究[50]。我国广泛接种乙脑疫苗,人群预存免疫普遍,其对寨卡病毒的感染及疫苗免疫保护作用的影响有必要深入研究。
从本文的分析可以看出能力储备是新发传染病疫苗研发的关键。当前对于寨卡病毒疫苗进行研发的机构,很多之前都有黄病毒属病毒疫苗研发基础或是建立了较为成熟的疫苗研发平台。现在疫苗研发手段越来越多样化,在传统疫苗研发效果不理想的情况下,必须建立起新型疫苗研发技术平台。
基于寨卡病毒的特点以及既往黄病毒属其他病毒疫苗的研发分析,寨卡病毒灭活疫苗、嵌合病毒疫苗应该是很有希望获得成功的疫苗,而载体疫苗、核酸疫苗和亚单位疫苗等的研发将会进一步推动这些疫苗类型的研发进步。
| [1] | WHO. Zika virus situation report (data as of 2november 2016). [EB/OL]. [2016-11-7].http://www.who.int/emergencies/zika-virus/situation-report/3-november-2016/en/. |
| [2] | PAHO. Cumulative Zika cases reported bycountries and territories in the Americas, 2015 -2016 (data as of 2 november 2016) [EB/OL].[2016-11-7]. http://www.paho.org/hq/index.php?option=com_docman&task=doc_view&Itemid=270&gid=36752&lang=en. |
| [3] | Bogoch II, Brady OJ, Kraemer MUG, et al. Potential for Zika virus introduction andtransmission in resource-limited countries in Africaand the Asia-Pacific region: a modelling study. Lancet Infect Dis, 2016, 16 (11) : 1237–1245. DOI: 10.1016/S1473-3099(16)30270-5 |
| [4] | Ishikawa T, Yamanaka A, Konishi E. A review ofsuccessful flavivirus vaccines and the problemswith those flaviviruses for which vaccines are notyet available. Vaccine, 2014, 32 (12) : 1326–1337. DOI: 10.1016/j.vaccine.2014.01.040 |
| [5] | Amanna IJ, Slifka MK. Current trends in West Nilevirus vaccine development. Expert Rev Vaccines, 2014, 13 (5) : 589–608. DOI: 10.1586/14760584.2014.906309 |
| [6] | Wikan N, Smith DR. Zika virus: history of a newlyemerging arbovirus. Lancet Infect Dis, 2016, 16 (7) : e119–e126. DOI: 10.1016/S1473-3099(16)30010-X |
| [7] | Fernandez-Garcia MD, Mazzon M, Jacobs M, et al. Pathogenesis of flavivirus infections: using andabusing the host cell. Cell Host Microbe, 2009, 5 (4) : 318–328. DOI: 10.1016/j.chom.2009.04.001 |
| [8] | Hilgenfeld R. Zika virus NS1, a pathogenicityfactor with many faces. EMBO J. 2016 Oct 27. pii:e201695871. |
| [9] | Hamel R, Dejarnac O, Wichit S, et al. Biology ofZika virus infection in human skin cells. J Virol, 2015, 89 (17) : 8880–8896. DOI: 10.1128/JVI.00354-15 |
| [10] | Haddow AD, Schuh AJ, Yasuda CY, et al. Geneticcharacterization of Zika virus strains: geographicexpansion of the Asian lineage. PLoS Negl TropDis, 2012, 6 (2) : e1477. DOI: 10.1371/journal.pntd.0001477 |
| [11] | Deckard DT, Chung WM, Brooks JT, et al.Male-to-male sexual transmission of Zikavirus-Texas, January 2016. MMWR Morb MortalWkly Rep, 2016, 65(14): 372-374. |
| [12] | Lessler J, Chaisson LH, Kucirka LM, et al. Assessing the global threat from Zika virus. Science, 2016, 353 (6300) : aaf8160. DOI: 10.1126/science.aaf8160 |
| [13] | Duffy MR, Chen TH, Hancock WT, et al. Zikavirus outbreak on Yap Island, Federated States ofMicronesia. N Engl J Med, 2009, 360 (24) : 2536–2543. DOI: 10.1056/NEJMoa0805715 |
| [14] | Cao-Lormeau VM, Roche C, Teissier A, et al. Zikavirus, French polynesia, south Pacific, 2013. EmergInfect Dis, 2014, 20(6): 1085-1086. |
| [15] | Campos GS, Bandeira AC, Sardi SI. Zika virusoutbreak, Bahia, Brazil. Emerg Infect Dis, 2015, 21 (10) : 1885–1886. DOI: 10.3201/eid2110.150847 |
| [16] | Faria NR, da Silva Azevedo RDS, Kraemer MUG, et al. Zika virus in the Americas: earlyepidemiological and genetic findings. Science, 2016, 352 (6283) : 345–349. DOI: 10.1126/science.aaf5036 |
| [17] | Fauci AS, Morens DM. Zika virus in the Americas—yet another arbovirus threat. N Engl J Med, 2016, 374 (7) : 601–604. DOI: 10.1056/NEJMp1600297 |
| [18] | Cao-Lormeau VM, Blake A, Mons S, et al. Guillain-Barré syndrome outbreak associated withZika virus infection in French Polynesia: acase-control study. Lancet, 2016, 387 (10027) : 1531–1539. DOI: 10.1016/S0140-6736(16)00562-6 |
| [19] | Alshekhlee A, Hussain Z, Sultan B, et al. Guillain-Barré syndrome: incidence and mortalityrates in US hospitals. Neurology, 2008, 70 (18) : 1608–1613. DOI: 10.1212/01.wnl.0000310983.38724.d4 |
| [20] | Ventura CV, Maia M, Bravo-Filho V, et al. Zikavirus in Brazil and macular atrophy in a child withmicrocephaly. Lancet, 2016, 387 (10015) : 228. |
| [21] | Victora CG, Schuler-Faccini L, Matijasevich A, etal. Microcephaly in Brazil: how to interpret reportednumbers? Lancet, 2016, 387(10019): 621-624. |
| [22] | Cugola FR, Fernandes IR, Russo FB, et al. TheBrazilian Zika virus strain causes birth defects inexperimental models. Nature, 2016, 534 (7606) : 267–271. |
| [23] | Mysorekar IU, Diamond MS. Modeling Zika virusinfection in pregnancy. N Engl J Med, 2016, 375 (5) : 481–484. DOI: 10.1056/NEJMcibr1605445 |
| [24] |
Zhao K. Vaccine Research and Application.Beijing: People's Medical Publishing House, 2013:250-260, 287-295, 396-411, 407-408 (in Chinese). 赵铠. 疫苗研究与应用. 北京: 人民卫生出版社,2013: 250-260, 287-295, 396-411, 407-408. |
| [25] | Monath TP, Fowler E, Johnson CT, et al. Aninactivated cell-culture vaccine against yellowfever. N Engl J Med, 2011, 364 (14) : 1326–1333. DOI: 10.1056/NEJMoa1009303 |
| [26] | Larocca RA, Abbink P, Peron JPS, et al. Vaccineprotection against Zika virus from Brazil. Nature, 2016, 536 (7617) : 474–478. DOI: 10.1038/nature18952 |
| [27] | Abbink P, Larocca RA, de La Barrera RA, et al. Protective efficacy of multiple vaccine platformsagainst Zika virus challenge in rhesus monkeys. Science, 2016, 353 (6304) : 1129–1132. DOI: 10.1126/science.aah6157 |
| [28] | Roukens AH, Visser LG. Yellow fever vaccine:past, present and future. Expert Opin Biol Ther, 2008, 8 (11) : 1787–1795. DOI: 10.1517/14712598.8.11.1787 |
| [29] | Recker M, Blyuss KB, Simmons CP, et al. Immunological serotype interactions and theireffect on the epidemiological pattern of dengue. Proc Biol Sci, 2009, 276 (1667) : 2541–2548. DOI: 10.1098/rspb.2009.0331 |
| [30] | Guy B, Guirakhoo F, Barban V, et al. Preclinicaland clinical development of YFV 17D-basedchimeric vaccines against dengue, West Nile andJapanese encephalitis viruses. Vaccine, 2010, 28 (3) : 632–649. DOI: 10.1016/j.vaccine.2009.09.098 |
| [31] | Biedenbender R, Bevilacqua J, Gregg AM, et al. PhaseII, ran-domized, double-blind, placebo-controlled,multicenter study to investigate the immunogenicityand safety of a West Nile virus vaccine in healthyadults. J Infect Dis, 2011, 203 (1) : 75–84. DOI: 10.1093/infdis/jiq003 |
| [32] | Martin JE, Pierson TC, Hubka S, et al. A West Nilevirus DNA vaccine induces neutralizing antibody inhealthy adults during a phase 1 clinical trial. JInfect Dis, 2007, 196 (12) : 1732–1740. DOI: 10.1086/527364 |
| [33] | Dowd KA, Ko SY, Morabito KM, et al. Rapiddevelopment of a DNA vaccine for Zika virus. Science, 2016, 354 (6309) : 237–240. DOI: 10.1126/science.aai9137 |
| [34] |
Jin Q.
Medical Molecular Virology. Beijing: Science Press, 2001 : 90 -92(in Chinese).
金奇. 医学分子病毒学. 北京: 科学出版社, 2001 : 90-92. |
| [35] | Rold?o A, Mellado MCM, Castilho LR, et al. Virus-like particles in vaccine development. ExpertRev Vaccines, 2010, 9 (10) : 1149–1176. DOI: 10.1586/erv.10.115 |
| [36] | Hoyt K, Hatchett R. Preparing for the next Zika. Nat Biotechnol, 2016, 34 (4) : 384–386. DOI: 10.1038/nbt.3532 |
| [37] | Malone RW, Homan J, Callahan MV, et al. Zikavirus: medical countermeasure development challenges. PLoS Negl Trop Dis, 2016, 10 (3) . |
| [38] | Dowd KA, DeMaso CR, Pelc RS, et al. Broadlyneutralizing activity of Zika virus-immune seraidentifies a single viral serotype. Cell Rep, 2016, 16 (6) : 1485–1491. DOI: 10.1016/j.celrep.2016.07.049 |
| [39] | Sirohi D, Chen ZG, Sun L, et al. The 3.8 ?resolution cryo-EM structure of Zika virus.Science, 2016, 352(6284): 467-470. |
| [40] | Modis Y, Ogata S, Clements D, et al. Aligand-binding pocket in the dengue virus envelopeglycoprotein. Proc Natl Acad Sci USA, 2003, 100 (12) : 6986–6991. DOI: 10.1073/pnas.0832193100 |
| [41] | Schneeweiss A, Chabierski S, Salomo M, et al. ADNA vaccine encoding the E protein of West Nilevirus is protective and can be boosted byrecombinant domain DIII. Vaccine, 2011, 29 (37) : 6352–6357. DOI: 10.1016/j.vaccine.2011.04.116 |
| [42] | Beltramello M, Williams KL, Simmons CP, et al. The human immune response to Dengue virus isdominated by highly cross-reactive antibodiesendowed with neutralizing and enhancing activity. Cell Host Microbe, 2010, 8 (3) : 271–283. DOI: 10.1016/j.chom.2010.08.007 |
| [43] | Dai LP, Song J, Lu XS, et al. Structures of the Zikavirus envelope protein and its complex with aFlavivirus broadly protective antibody. Cell HostMicrobe, 2016, 19 (5) : 696–704. |
| [44] | Zhao HY, Fernandez E, Dowd KA, et al. Structuralbasis of Zika virus-specific antibody protection. Cell, 2016, 166 (4) : 1016–1027. DOI: 10.1016/j.cell.2016.07.020 |
| [45] | Stettler K, Beltramello M, Espinosa DA, et al. Specificity, cross-reactivity, and function ofantibodies elicited by Zika virus infection. Science, 2016, 353 (6301) : 823–826. DOI: 10.1126/science.aaf8505 |
| [46] | Swanstrom JA, Plante JA, Plante KS, et al. Denguevirus envelope dimer epitope monoclonal antibodiesisolated from dengue patients are protective againstZika virus. mBio, 2016, 7 (4) : e01123–16. |
| [47] | Priyamvada L, Quicke KM, Hudson WH, et al. Human antibody responses after dengue virusinfection are highly cross-reactive to Zika virus. Proc Natl Acad Sci USA, 2016, 113 (28) : 7852–7857. DOI: 10.1073/pnas.1607931113 |
| [48] | Dejnirattisai W, Supasa P, Wongwiwat W, et al. Dengue virus sero-cross-reactivity drives antibodydependentenhancement of infection with zikavirus. Nat Immunol, 2016, 17 (9) : 1102–1108. DOI: 10.1038/ni.3515 |
| [49] | Durbin AP. Dengue antibody and Zika: friend orfoe? Trends Immunol, 2016, 37(10): 635-636. |
| [50] | Harrison SC. Immunogenic cross-talk betweendengue and Zika viruses. Nat Immunol, 2016, 17 (9) : 1010–1012. DOI: 10.1038/ni.3539 |
 2017, Vol. 33
2017, Vol. 33