中国科学院微生物研究所、中国微生物学会主办
文章信息
- 孙溢华, 张春莉, 施定基, 贾晓会, 贾睿, 何培民
- Sun Yihua, Zhang Chunli, Shi Dingji, Jia Xiaohui, Jia Rui, He Peimin
- 光质对工程聚球藻7002生长及psbA启动子的调控
- Effects of light quality on cell growth and psbA promoter of engineered Synechococcus sp. PCC7002
- 生物工程学报, 2016, 32(9): 1286-1290
- Chin J Biotech, 2016, 32(9): 1286-1290
- 10.13345/j.cjb.160002
-
文章历史
- Received: January 3, 2016
- Accepted: January 29, 2016
2 Department of Molecular Membrane Biology, Max Planck Institute of Biophysics, Max-von-Laue-Str.3, D-60438 Frankfurt am Main, Germany
3 中国科学院植物研究所,北京 100093
2 Department of Molecular Membrane Biology, Max Planck Institute of Biophysics, Max-von-Laue-Str.3, D-60438 Frankfurt am Main, Germany ;
3 Institute of Botany, Chinese Academy of Sciences, Beijing 100093, China
随着蓝藻的产业化发展,光质调控已成为提高生物量及目的产物表达的重要途径[1-3],转录因子介导的光调控机制逐步被揭示[4]。光质是光源所包含的所有单色光的光强及波长的总称,直接影响藻细胞的光合作用及代谢途径。聚球藻光系统Ⅱ的捕光天线主要受psbA基因的调控[5],psbA基因对光质具有较敏感的响应机制[6]。同时,工程蓝藻常用的载体启动子PpsbA[7]与蓝藻的psbA基因同源[8],蓝光与红光分别诱导的信号通路可同时调节蓝藻本身的psbA基因及其载体启动子PpsbA[9]。然而,相对于野生蓝藻,转基因蓝藻的最适光合条件已有显著改变[10],若要研究光质对于psbA基因及PpsbA的调控,必须先排除光合作用的干扰因素(总光强、温度与pH),以达到最大光合效率。
新型光生物反应器(SDJ,上海联环生物工程设备有限公司)可对总光强、温度、pH、光质进行精确调控,能够使藻细胞达到最大光合效率,是工程蓝藻研究及产业化探索的重要工具。光生物反应器配备的LED光源可提供稳定的光质(红光615-630 nm,蓝光440-475 nm),已普遍应用于微藻培养[11]。研究发现,相同LED光质对于不同藻种的影响显示出差异,例如蓝光促进拟绿球藻Nannochloropsis sp.细胞增殖[12],却会抑制小球藻Chlorella sp.的生长并促进其油脂积累[13]。因此,研究LED光质对工程蓝藻生长的影响是产业化的必要途径。
白斑综合症病毒(WSSV)于1992年首先在中国台湾地区发现,20年来WSSV在亚洲、南北美洲、欧洲和非洲造成的经济损失已超过70亿美元,尚未见在规模生产中应用有效药物来防治[14]。Witteveldt等[15]首次用大肠杆菌表达的VP28 (WSSV被膜中的结构蛋白),经口服和注射接种,可提高对虾抗WSSV的能力。Jia等[10]使用转vp28基因蓝藻,经口服后攻毒,成功提高了对虾的成活率,证明口服转基因蓝藻能有效抵抗WSSV。工程蓝藻口服剂的研制已进入中试阶段,其中工程蓝藻的规模培养是产业化的基础。聚球藻属Synechococcus sp.由于适合光反应器培养,已被广泛用于规模培养的研究[16],因此转vp28基因聚球藻7002[17]在产业化上非常具有前景。
1 材料与方法 1.1 转vp28基因聚球藻的摇床培养转vp28基因聚球藻S. PCC7002由中国科学院植物研究所提供,装在含150 mL BG-11培养基[18]的250 mL摇瓶中进行培养,温度为30 ℃,摇床转速为130 r/min,光照为50 μmol/(m2·s),连续光照。
1.2 净光合作用的单因素试验聚球藻7002的叶绿素浓度通过公式(1)[19]测定:
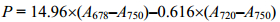
|
(1) |
式中,P表示叶绿素浓度(mg/ml);A750、A720、A678分别表示750 nm、720 nm、678 nm处的吸光值。将待测藻液的浓度调整至每毫升样品所含叶绿素为10 μg。
净光合速率使用氧电极(Hansatech,UK)测定,温度由恒温水浴箱(Julubo,Germany)通过循环水控制。测定样品在不同条件下的净光合速率(光强,温度,pH)[20]。净光合速率计算采用公式(2):
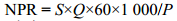
|
(2) |
式中,NPR (μmol O2/mg Chlah)表示净光合速率(Net photosynthetic rate);S为记录纸走的斜率(/min);Q为常数,表示一定温度下水中的溶氧量(mol O2/mL);P为样品的叶绿素浓度(mg/mL);60表示60 min;1 000表示记录纸的满量程为1 000。
1.3 转vp28基因聚球藻的光生物反应器培养封闭式光生物反应器为SDJ-5L型光合发酵系统(上海联环生物工程设备有限公司),由全自动圆柱形玻璃反应器及外置LED光源构成。该系统可对pH、温度、光照进行恒定控制,培养条件(光照、温度、pH)按照优化后的指标((300±10) μmol/(m2·s),37 ℃,pH 7.5)进行设置。工作体积为3.5 L,初始接种量使藻液A750达到0.1±0.02,平均空气流量为1 L/min,平均CO2的体积分数为0.5%。培养时长为72 h。LED光源采用白、红、蓝进行调控,平均光强测定采用公式(3)[21]:

|
(3) |
式中,Iav为平均光强(μmol/(m2·s));I为入射光强(μmol/(m2·s));K为光衰减系数;R为反应器半径(m)。聚球藻7002的光衰减系数计算采用如下公式(4)[22]:

|
(4) |
式中,K为光衰减系数;A750为藻液吸光值。
调控白光、红光、蓝光的配比并设置White、Red、Blue、Balance共4个实验组(表 1),通过公式(3)测定并调控平均光强,使得平均光强符合优化的标准((300±10) μmol/(m2·s))。
| Item | White light: Red light: Blue light | Iav (μmol/(m2·s)) |
| White | 6:0:0 | 294-146 |
| Red | 3:2:1 | 308-138 |
| Blue | 3:1:2 | 292-171 |
| Balance | 2:2:2 | 303-154 |
Trizol法提取转vp28基因聚球藻7002的总RNA。以总RNA为模板,用试剂盒反转录为cDNA(Tiangen,China)。vp28序列参照文献[17]并设计vp28的qPCR引物(表 2)。管家基因16s rRNA的引物采用已有模板[23]。20 μL PCR反应体系包括2 μL cDNA,0.6 μL正向引物与反向引物,10 μL SYBRFast qPCR Master Mix (2X) (KAPA,USA)。参照Jia等[10]的方法,计算vp28表达率并用Western blotting检测蛋白条带。
| Primer name | Primer sequence (5'–3') |
| vp28-FW | AACCTCCGCATTCCTGTGACTG |
| vp28-RV | TCCGCATCTTCTTCCTTCATCTGTG |
| psbAI-FW | CGTATTCCAGGCAGAGCACAACAT |
| psbAI-RV | GCAGTGAACCAGATACCGACTACAG |
| psbAⅡ-FW | ATGTTGTGCTCTGCCTGGAATACG |
| psbAⅡ-RV | TCACTGCCACCACCTGCTTCA |
| psbAⅢ-FW | GCGACTGCTGTGCTCTTGGTT |
| psbAⅢ-RV | TCCGTTTCTGTGGTCTCCCGAAT |
在NCBI (http://www.ncbi.nlm.nih.gov/)上找到对应的蛋白序列psbAI (ID: 501262777)、psbAⅡ (ID: 501264014)、psbAⅢ (ID: 501264746),并利用tblastn反向定位到聚球藻7002基因组全序列(CP000951)的对应片段psbAI (region: 1489906-1490985)、psbAⅡ (region: 161804-162883)、psbAⅢ (region: 2245055-2246134)。分别设计qPCR引物(表 2)。取接种前的样品(藻种)作为参照,每隔24 h对White、Red、Blue三个实验组的样品进行检测,其中qPCR方法及反应体系同1.5。
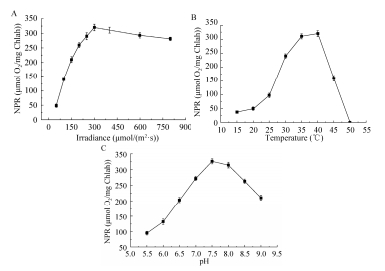
2 结果与讨论 2.1 pH、光强、温度对藻细胞光合作用的影响光合作用中,除了光强直接供给电子激活的能量,温度与pH对酶活力的影响决定了光合作用的效率[24]。因此,必须首先排除温度与pH的干扰,使得光强的能量最大限度地输入光系统Ⅱ,才能进一步分析出光的成分(光质)对于捕光效果的影响。在温度为35 ℃、pH为7.3的条件下,研究光强(50-800 μmol/(m2·s))对净光合速率的影响(图 1A)。随着光强的增加,净光合速率不断增加。当光强达到400 μmol/(m2·s)时,净光合速率出现下降,从320 μmol O2/mg Chlah左右下降至281 μmol O2/mg Chlah。在光强为300 μmol/(m2·s),pH为7.3的条件下,研究温度(15-50 ℃)对净光合速率的影响(图 1B)。随着温度增加,净光合速率不断增加。当温度达到40 ℃后,净光合速率突然下降,50 ℃时净光合速率从320 μmol O2/mg Chlah变为0。在光强为300 μmol/(m2·s),温度为35 ℃的条件下,研究pH 5.5-9.0对净光合速率的影响(图 1C)。随着pH增加,净光合速率不断增加。当pH达到7.5后,净光合速率开始下降,净光合作用从326 μmol O2/mg Chlah下降至210 μmol O2/mg Chlah。
|
| 图 1 光强、温度、pH对净光合速率的影响 Figure 1 Effect of irradiance, temperature and pH on net photosynthetic rates. (A) Irradiance. (B) Temperature. (C) pH. |
| |
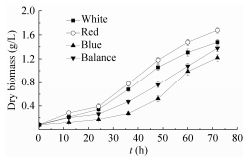
光生物反应器培养的实验中,我们尝试用单色光(蓝光)来培养聚球藻,但细胞生长速度极慢,细胞样品的采集与处理遇到较大困难,并且细胞浓度过低严重影响到基因与蛋白的检测。因此,为了方便实验以及产业化生产的需要,本研究以3 d内干生物量达到1 g/L为最低标准,进行光质配比的设定。随着细胞密度的升高,入射光强并不能实时反映藻细胞的光能利用率[22]。从开始培养到结束,藻细胞的光能利用率处于一个由高至低的动态的变化过程。本研究采用平均光强代替入射光作为计量参数[26],计算出了平均光强的变化范围(表 1),以求反应实际的光能利用率[11]。White、Red、Blue、Balance四个实验组72 h的干生物量分别为1.48 g/L、1.68 g/L、1.22 g/L、1.38 g/L。图 3中,培养前36 h内,4组藻细胞进入对数生长期,干生物量积累速度差异不显著。培养36 h后,Red组与Blue、Balance组的干生物量积累速度差异显著,Red组生长速度最快;Red与Blue组差异极显著,Blue组明显生长较慢;White组与Balance组差异不显著,生长速度较接近。光生物反应器的验证培养结果表明,在生物量积累上,已经超过了同类实验[22, 25],3 d内平均干重超过1.2 g/L。
|
| 图 2 不同光质组成下干生物量积累曲线 Figure 2 Variations of dry biomass with various proportions of light quality. |
| |
|
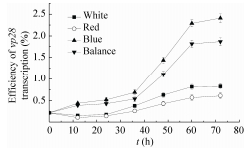
| 图 3 不同光质组成下vp28表达率变化曲线 Figure 3 Variations of vp28 transcription with various proportions of light quality. |
| |
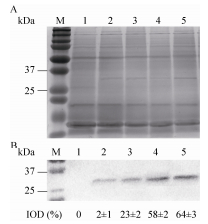
宁文艳等[27]提出光调控启动子PpsbA是鱼腥藻的高效表达载体,未经光调控的PpsbA表达效率是IPTG调控下Ptac的1.17倍。然而尚未有报道指出转基因鱼腥藻的载体启动子PpsbA可接受光质调控,未经光调控的转vp28基因鱼腥藻7120的表达效率只有0.1%-1%[10]。转基因聚球藻7002所用表达载体为prl-489,启动子为PpsbA[17]。本文中高比例蓝光促进了vp28基因的表达,并促进了psbAⅡ、psbAⅢ的转录,这与Tsinoremas等[9]研究转基因聚球藻7942结果一致。图 3与图 5的结果证明,载体启动子PpsbA与光合基因psbA的转录在时空效应上具有一致性,均受到蓝光的诱导作用。然而外源蛋白(VP28)的积累量(图 4)差异不如外源基因表达差异明显(图 3),这可能是DNA转录与mRNA翻译的时空差异造成的。图 3中,White、Red、Blue、Balance四组vp28基因表达率总体均呈现上升趋势,前36 h内4组vp28表达率都较低。其中,Blue与Balance组表达率较高,White与Red组表达率较低,36 h后前两组与后两组相比差异明显。Blue与Balance组在前36 h及60 h后差异不显著,而在36 h至60 h之间差异明显。White与Red组在72 h内差异都不明显。Blue组中vp28基因表达率最高达到2.41%,出现于第72 h。Red组中vp28基因表达率最低达到0.11%,出现于12 h。图 4中,总蛋白条带在PAGE上无明显差别,而VP28条带在PVDF上差异较为明显。灰度值从少到多分别为Red、White、Balance、Blue,说明Blue组蛋白积累量最高,Red组蛋白积累量最少,并且Blue组与Red组差异明显。

|
| 图 5 不同光质组成下psbA的相对表达量 Figure 5 Relative transcription of psbA genes with various proportions of light quality. |
| |
|
| 图 4 同光质组成下VP28的相对含量 Figure 4 Relative accumulation of VP28 in engineered Synechococcus sp. PCC7002 with various proportions of light quality. (A) SDS-PAGE analysis of total protein. (B) Western blotting of VP28. M: marker; 1: wild type; 2: red; 3: white; 4: balance; 5: blue. |
| |
图 5显示,接种后光能利用率较高,psbA转录效率比接种前提高了50%-75%。White与Red组psbA的总mRNA表达量高于Blue组。随时间变化,总psbA mRNA含量呈下降趋势。psbAI、psbAⅡ、psbAⅢ在3组中都呈下降趋势,其中psbAⅡ、psbAⅢ在White与Red组中下降速度较快,psbAⅡ分别从第1天的0.72、0.48下降至第3天的0.32、0.28,psbAⅢ分别从0.72、0.42下降至0.21、0.11。而在Blue组中,psbAⅡ与psbAⅢ的下降速度明显较慢,从第1天的0.34、0.78分别下降至第3天的0.20、0.40。Blue组的psbAⅡ与psbAⅢ始终高于White与Red组,而Red组的psbAⅡ与psbAⅢ始终处于较低水平。与纯白光相比,高比例红光并不影响psbA基因总mRNA含量,但最终提高了转基因聚球藻7002的干生物量积累;高比例蓝光抑制了psbA总mRNA的含量,从而抑制了干生物量的积累,但促进了psbAⅡ与psbAⅢ的转录。这可能是由于不同比例的红光、蓝光影响了Rubisco与碳酸酐酶的活性[28],从而影响了碳循环途径。本文中高比例红光促进了生物量的积累,这可能是因为红光诱导了一种以钙调蛋白为二级信使的信号通路[29],并促进了psbAI的表达。
3 结论本文研究了光质调控对工程聚球藻7002生长及vp28表达的影响,确定最优光能利用条件,使得生物量在3 d内突破1.2 g/L。当白光,红光与蓝光的光强比为3:1:2时,重组蛋白VP28表达翻倍。发现蓝光可促进启动子PpsbA表达vp28,红光可提高生物量的积累。通过检测基因转录及目的蛋白表达,证明psbA基因响应了光质调控。研究结果对工程蓝藻的规模培养、重组蛋白的高效表达、转基因生物制药具有重要的参考价值。
| [1] | Aguilera J, Francisco J, Gordillo L. Light quality effect on photosynthesis and efficiency of carbon assimilation in the red alga Porphyra leucosticta. J Plant Physiol,2000, 157 (1) : 86 –92. DOI: 10.1016/S0176-1617(00)80140-6 |
| [2] | Niizawa I, Heinrich JM, Irazoqui HA. Modeling of the influence of light quality on the growth of microalgae in a laboratory scale photo-bio-reactor irradiated by arrangements of blue and red LEDs. Biochem Eng J,2014, 90 (5) : 214 –223. |
| [3] | Rashid N, Rehman MSU, Han JI. Enhanced growth rate and lipid production of freshwater microalgae by adopting two-stage cultivation system under diverse light and nutrients conditions. Water Environ J,2015, 29 (4) : 533 –540. DOI: 10.1111/wej.12110 |
| [4] | Nesbit AD, Whippo C, Hangarter RP. Translation initiation factor 3 families: what are their roles in regulating cyanobacterial and chloroplast gene expression?. Photosynth Res,2015, 126 (1) : 147 –159. DOI: 10.1007/s11120-015-0074-4 |
| [5] | Zouni A, Witt HT, Kern J, et al. Crystal structure of photosystem Ⅱ from Synechococcus elongatus at 3.8 Å resolution. Nature,2001, 409 (6821) : 739 –743. DOI: 10.1038/35055589 |
| [6] | Tsinoremas NF, Schaefer M, Golden SS. Blue and red light reversibly control psbA expression in the cyanobacterium Synechococcus sp. strain PCC 7942. J Biol Chem,1994, 269 (23) : 16143 –16147. |
| [7] | Ma WM, Shi DJ, Wang QX, et al. Exogenous expression of the wheat chloroplastic fructose-1, 6-bisphosphatase gene enhances photosynthesis in the transgenic cyanobacterium, Anabaena PCC7120. J Appl Phycol,2005, 17 (3) : 273 –280. DOI: 10.1007/s10811-005-4850-y |
| [8] | Bergsland KJ, Haselkorn R. Evolutionary relationships among eubacteria, cyanobacteria, and chloroplasts: evidence from the rpoC1 gene of Anabaena sp. strain PCC7120. J Bacterial,1991, 173 (11) : 3446 –3455. |
| [9] | Tsinoremas NF, Kawakami A, Christopher DA. High-fluence blue light stimulates transcription from a higher plant chloroplast psbA promoter expressed in a cyanobacterium, Synechococcus (sp. strain PCC7942). Plant Cell Physiol,1999, 40 (4) : 448 –452. DOI: 10.1093/oxfordjournals.pcp.a029562 |
| [10] | Jia XH, Zhang CL, Shi DJ, et al. Oral administration of Anabaena-expressed VP28 for both drug and food against white spot syndrome virus in shrimp. J Appl Phycol,2015 . DOI: 10.1007/s10811-015-0607-4 |
| [11] | Cornet JF, Dussap CG, Gros JB. Kinetics and energetics of photosynthetic micro-organisms in photobioreactors// Bioprocess and Algae Reactor Technology, Apoptosis. Berlin Heidelberg: Springer,2007 : 153 –224. DOI: 10.1007/BFb0102299 |
| [12] | Das P, Wang L, Sarah AS, et al. Enhanced algae growth in both phototrophic and mixotrophic culture under blue light. Bioresour Technol,2011, 102 (4) : 3883 –3887. DOI: 10.1016/j.biortech.2010.11.102 |
| [13] | Shu CH, Tsai CC, Liao WH, et al. Effects of light quality on the accumulation of oil in a mixed culture of Chlorella sp. and Saccharomyces cerevisiae. J Chem Technol Biotechnol,2012, 87 (5) : 601 –607. DOI: 10.1002/jctb.v87.5 |
| [14] | Seibert CH, Pinto AR. Challenges in shrimp aquaculture due to viral diseases: distribution and biology of the five major penaeid viruses and interventions to avoid viral incidence and dispersion. Braz J Microbiol,2012, 43 (3) : 857 –864. DOI: 10.1590/S1517-83822012000300002 |
| [15] | Witteveldt J, Cifuentes CC, Vlak JM, et al. Protection of Penaeus monodon against white spot syndrome virus by oral vaccination. J Virol,2004, 78 (4) : 2057 –2061. DOI: 10.1128/JVI.78.4.2057-2061.2004 |
| [16] | Niki K, Aikawa S, Yokono M, et al. Differences in energy transfer of a cyanobacterium, Synechococcus sp. PCC 7002, grown in different cultivation media. Photosynth Res,2015, 125 (1/2) : 201 –210. |
| [17] |
Zhang CL. Cloning of envelope protein vp28 gene of WSSV and its expression in cyanobacteria[D]. Qingdao: Institute of Oceanology, Chinese Academy of Sciences, 2002 (in Chinese). 张春莉. WSSV囊膜蛋白VP28基因在蓝藻中克隆和表达[D].青岛:中国科学院海洋研究所, 2002. http://cdmd.cnki.com.cn/article/cdmd-80068-2002128073.htm |
| [18] | Stanier RY, Kunisawa R, Mandel M, et al. Purification and properties of unicellular blue-green algae (order Chroococcales). Bacteriol Rev,1971, 35 (2) : 171 –205. |
| [19] | Packer L, Glazer AN. Methods in Enzymology: Cyanobacteria. San Diego: Academic Press,1988 : 766 –778. |
| [20] | Shi DJ, Zhou GF, Fang SX, et al. Studies on photosynthesis, respiration and morphology of Nostoc flagelliforme. Acta Bot Sin,1992, 34 (7) : 507 –514. |
| [21] | Grima EM, Camacho FG, Pérez JAS, et al. Evaluation of photosynthetic efficiency in microalgal cultures using averaged irradiance. Enzyme Microb Tech,1997, 21 (5) : 375 –381. DOI: 10.1016/S0141-0229(97)00012-4 |
| [22] |
Kang RJ, Zhou WQ, Cai ZL, et al. Photoautotrophic cultivation of Synechococcus sp. PCC7002 in photobioreactor.
Chin J Biotech,2000, 16 (5) : 618 –622.
(in Chinese). 康瑞娟, 周文齐, 蔡昭铃, 等. 聚球藻7002在光生物反应器中的光自养培养. 生物工程学报, 2000 , 16 (5) : 618-622. |
| [23] | Pinto F, Pacheco CC, Ferreira D, et al. Selection of suitable reference genes for RT-qPCR analyses in cyanobacteria. PLoS ONE,2012, 7 (4) : e34983 . DOI: 10.1371/journal.pone.0034983 |
| [24] | Moore LR, Goericke R, Chisholm SW. Comparative physiology of synechococcus and prochlorococcus-influence of light and temperature on growth, pigments, fluorescence and absorptive properties. Mar Ecol Prog Ser,1995, 116 : 259 –275. DOI: 10.3354/meps116259 |
| [25] |
Zeng WL, Zhao FF, Cao ZG, et al. Medium optimization by response surface method for transgenic Synechococcus sp. PCC 7002 with mouse metallothionein-I gene.
Chin J Biotech,2008, 24 (1) : 130 –136.
(in Chinese). 曾文炉, 赵飞飞, 曹照根, 等. 利用响应面方法优化转小鼠金属硫蛋白-I基因聚球藻7002的培养基成分. 生物工程学报, 2008 , 24 (1) : 130-136. |
| [26] | Camacho-Rubio F, Padial-Vico A, Martinez-Sancho ME. The effect of the mean intensity of light on the cultivation of Chlorella pyrenoidosa. Int Chem Eng,1985, 25 (2) : 283 –288. |
| [27] |
Ning WY, Wu XM, Wang CM, et al. Efficiency comparison of promoters Ptac & PsbA driving hG-CSF expression in Anabaena sp. PCC7120.
J Mirobiol,2014, 34 (3) : 36 –41.
(in Chinese). 宁文艳, 吴先敏, 王春梅, 等. 启动子Ptac与PsbA在鱼腥藻7120中表达hG-CSF的效率比较. 微生物学杂志, 2014 , 34 (3) : 36-41. |
| [28] | Roscher E, Zetsche K. The effects of light quality and intensity on the synthesis of ribulose-1, 5-bisphosphate carboxylase and its mRNAs in the green alga Chlorogonium elongatum. Planta,1986, 167 (4) : 582 –586. DOI: 10.1007/BF00391236 |
| [29] | Alizadeh D, Cohen A. Red light and calmodulin regulate the expression of the psbA binding protein genes in Chlamydomonas reinhardtii. Plant Cell Physiol,2010, 51 (3) : 312 –322. |
 2016, Vol. 32
2016, Vol. 32




