服务
文章信息
- 王雷, 袁京, 姚培圆, 程丽华, 解美仙, 贾荣荣, 冯进辉, 王敏, 吴洽庆, 朱敦明
- Wang Lei, Yuan Jing, Yao Peiyuan, Cheng Lihua, Xie Meixian, Jia Rongrong, Feng Huijin, Wang Min, Wu Qiaqing, Zhu Dunming
- 一种来源于运动替斯崔纳菌KA081020-065的新型卤醇脱卤酶的表达纯化及性质分析
- Expression and characterization of a novel halohydrin dehalogenase from Tistrella mobilis KA081020-065
- 生物工程学报, 2015, 31(5): 659-669
- Chin J Biotech, 2015, 31(5): 659-669
- 10.13345/j.cjb.140427
-
文章历史
- Received: August 26, 2014
- Accepted: November 14, 2014
2. 中国科学院天津工业生物技术研究所 工业酶国家工程实验室 天津市生物催化技术工程中心,天津 300308;
3. 河北诚信有限责任公司,河北 石家庄 051130
2. Tianjin Engineering Center for Biocatalytic Technology, National Engineering Laboratory for Industrial Enzymes, Tianjin Institute of Industrial Biotechnology, Chinese Academy of Sciences, Tianjin 300308, China;
3. Hebei Chengxin Co., LTD, Shijiazhuang 051130, Hebei, China
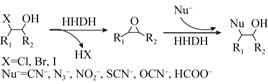
卤醇脱卤酶 (EC 4.5.1.X) 又叫作卤代醇环氧酶或卤代醇卤化氢裂解酶[1],与卤代烷脱卤酶和卤代酸脱卤酶一样,卤醇脱卤酶对于含氯污染物的生物降解、净化环境具有重要意义。卤醇脱卤酶催化反应时不需要任何辅酶,通过分子内亲核取代机制催化碳-卤键断裂进行脱卤反应,邻卤醇转化为相应的环氧化物并释放出卤化氢 (图1),可用于手性的环氧化物的合成[2, 3];在亲核试剂(CN-,N3-,NO2-,SCN-,OCN-,HCOO-等) 存在的条件下,继续催化环氧化物开环反应[4, 5, 6],合成一系列光学纯的β-取代醇[4],因此,卤醇脱卤酶也是一类在有机合成中非常重要的生物催化剂。
|
| 图1 卤醇脱卤酶催化邻卤醇脱卤反应和环氧化物开环反应 Fig.1 The dehalogenation of a vicinal halohydrin and epoxide ring opening by halohydrin dehalogenase. |
1968年首次以2,3-二溴丙醇作为唯一碳源,从土壤中分离出产卤醇脱卤酶的微生物菌株——黄杆菌Flavobaterium sp.[7],随后人们从土壤和淡水沉积物中相继筛选得到多种产卤醇脱卤酶的微生物,但来源于微生物的卤醇脱卤酶仅有10余种。根据序列同源性,卤醇脱卤酶通常被分为HheA、HheB、HheC 3类[8],研究较多的卤醇脱卤酶包括来源于节杆菌Arthrobacter sp. AD2的卤醇脱卤酶HheA-AD2[9, 10, 11],来源于棒状杆菌Corynebacterium strain N-1074的卤醇脱卤酶HheA和HheB[12],来源于土壤杆菌Agrobacterium strain NHG3的卤醇脱卤酶DehB[13, 14],来源于分枝杆菌Mycobacerium sp. strain GP1的卤醇脱卤酶HheB-GP1[8],以及来源于放射形土壤杆菌Agrobacterium radiobacter AD1的卤醇脱卤酶HheC[8]等。其中,卤醇脱卤酶HheC和HheA-AD2的蛋白晶体结构已经被解析,结果显示两种酶均为四聚体[15, 16]。进一步对其反应机理推断,认为卤醇脱卤酶是通过催化三联体丝氨酸-酪氨酸-精氨酸 (S-Y-R) 进行脱卤反应和开环反应[17, 18]。根据其蛋白质的三级结构信息并结合模拟计算,对两种卤醇脱卤酶都已进行了分子改造[10, 19, 20]。目前报道的卤醇脱卤酶分子量大小为20-35 kDa,在pH 8.0-9.5范围内保持较高的活性,最适的温度范围为40-50 ℃,并且某些金属离子 (如Cu2+、Zn2+、Hg+等) 会抑制其活性[1];卤醇脱卤酶已应用于(R)-4-氰基-3-羟基丁酸乙酯 (Ethyl(R)-4-cyano-3-hydroxy-butyrate,(R)-HN) 的生物催化合成中[20, 21],而(R)-HN是合成阿托伐他汀[22] (Atorvastatin,商品名Lipitor,年销售额百亿美元的降血脂处方药) 手性侧链的关键中间体。
由于卤醇脱卤酶数量较少,并且同一类卤醇脱卤酶之间的序列同源性很高,所以寻找与已有3类卤醇脱卤酶同源性低的新一类卤醇脱卤酶具有重要意义。本文通过基因数据挖掘 (Genome mining),获得一种来源于运动替斯崔纳菌[23] Tistrella mobilis KA081020-065的新型卤醇脱卤酶HheTM,根据序列同源性分类,该酶不属于已有的3类卤醇脱卤酶。我们将该酶进行了表达纯化,并对其酶学性质进行了研究。为了进一步确认该酶是一种新的卤醇脱卤酶,利用该酶进行生物催化(S)-4-氯-3-羟基丁酸乙酯 (Ethyl(S)-4-chloro-3-hydroxybutyrate,(S)-ECHB) 的脱氯反应,反应过程中添加亲核试剂CN-,获得了阿托伐他汀的关键中间体(R)-HN。
1 材料与方法 1.1 材料 1.1.1 质粒、菌株及主要试剂pET-32a(+) 质粒购自Novagen公司;FastDigest限制性内切酶购自Fermentas公司;蛋白胨和酵母提取物均购自BD公司;Bradford BCA蛋白浓度试剂盒购自康为世纪公司;考马斯亮蓝R250购自Solarbio公司;(S)-4-氯-3-羟基丁酸乙酯、(R)-4-氰基-3-羟基丁酸乙酯等试剂均购自国药集团。
1.1.2 主要仪器蛋白纯化仪:ÄKTA purifier 10,所用层析柱均为GE公司;APV 2000高压匀浆破碎仪购自德国APV公司;RC6+高速冷冻离心机购自Thermo公司;气相色谱仪Agilent 7890A购自Agilent公司。
1.2 目的基因的合成在美国国立生物技术信息中心 (NCBI) 数据库(http://www.ncbi.nlm.nih.gov/protein) 中以“halohydrin dehalogenase”或“halohydrin hydrogen-halide-lyase”为检索词进行检索,得到可能的卤醇脱卤酶相关信息。通过BioEdit分析软件的ClustalW多序列比对,分析候选的卤醇脱卤酶的保守序列,最终确定一种来源于运动替斯崔纳菌Tistrella mobilisKA081020-065的卤醇脱卤酶 (GenBank登录号为AFK51877.1) 为研究对象,将此卤醇脱卤酶命名为HheTM。通过在线的jcat密码子优化程序 (http://www.jcat.de) 对HheTM的原始基因序列进行了针对E. coli中表达的密码子优化,在C端加上6×His标签,目的基因由上海旭冠生物科技发展有限公司合成。
1.3 目的蛋白的表达纯化目的基因构建至pET-32a(+) 载体的NdeⅠ(346 bp) 和Hind Ⅲ酶切位点之间,重组质粒转化E. coli BL21 (DE3) 感受态细胞。将成功转化的单克隆接种于20 mL含有终浓度100 μg/mL氨苄青霉素的LB液体培养基中,于37 ℃、200 r/min培养过夜,然后转接到800 mL的LB培养基 (100 μg/mL氨苄青霉素) 中,培养至OD600为1.0左右,向培养基中添加IPTG至终浓度为0.1 mmol/L,25 ℃诱导10 h;于4 ℃、6 000×g离心15 min收集菌体。用4 ℃预冷的缓冲液A (50 mmol/L Na2HPO4-NaH2PO4,pH 7.5,500 mmol/L NaCl) 洗涤菌体一次,收集菌体进行破碎或-20 ℃保存。
上述菌体用缓冲液A重悬,4 ℃高压匀浆破碎。12 000 r/min离心30 min,收集上清液,用0.45 μm的滤膜过滤,Ni-NTA柱纯化。先用缓冲液A洗涤,再用缓冲液B (50 mmol/L Na2HPO4-NaH2PO4,pH 7.5,500 mmol/L NaCl,500 mmol/L 咪唑) 进行梯度洗脱。选择梯度为50 mmol/L、75 mmol/L、200 mmol/L咪唑,收集200 mmol/L咪唑的洗脱峰。所得纯酶用Amicon Ultra-15超滤管 (截留分子量:10 kDa) 浓缩,缓冲液C (50 mmol/L Na2HPO4-NaH2PO4,pH 7.5) 脱盐后,用于后续的酶学性质检测。蛋白质浓度用BCA试剂盒检测,使用牛血清白蛋白作为标准蛋白。
1.4 酶学性质测定 1.4.1 分子量和酶活性测定卤醇脱卤酶HheTM在溶液中的聚集状态通过凝胶层析和SDS-PAGE来进行确定。所用层析柱为Superdex 200 10/300 GL。流动相为20 mmol/L磷酸盐缓冲液,150 mmol/L NaCl,pH 7.2,流速为0.5 mL/min。蛋白的分子量大小通过和标准蛋白的保留体积进行计算得到,标准蛋白为:Ovalbumin (43.0 kDa),Conalbumin (75.0 kDa),Conalbumin (158.0 kDa),Ferritin (440.0 kDa),Thyroglobulin (669.0 kDa)。
以(S)-ECHB作为底物进行酶活的检测,(S)-ECHB在卤醇脱卤酶作用下生成(S)-3,4-环氧丁酸乙酯 (Ethyl(S)-3,4-expoxybutyrate,(S)-EEB)。缓冲液为Na2HPO4-NaH2PO4 (50 mmol/L,pH 8.0),1 mL反应体系中,包括40 mmol/L的底物(S)-ECHB以及合适的酶量,30 ℃条件下反应10 min,加入50 µL 1 mol/L盐酸终止反应,等体积乙酸乙酯萃取,所得有机相用无水硫酸钠干燥后进行气相色谱分析。一个酶活单位 (U) 定义为每分钟消耗1 µmol底物(S)-ECHB所需的酶量。气相色谱检测条件为:Agilent 7890A,色谱柱19091J-413 HP-5 (30 m×0.32 mm×0.25 µm),FID检测温度220 ℃,升温程序:80 ℃保持3 min,20 ℃/min升高到160 ℃保持1 min。此气相条件下得到的(S)-ECHB和(S)-EEB的保留时间分别为2.3 min和4.4 min。
1.4.2 最适pH及pH稳定性HheTM的最适反应pH通过在不同pH的缓冲液中测定酶的活力确定。缓冲液分别为50 mmol/L的Na2HPO4-NaH2PO4缓冲液 (pH 6.0-8.0),Tris-H2SO4缓冲液 (pH 8.0-9.0),Glycine-NaOH缓冲液 (pH 9.0-10.0),Na2HPO4-NaOH缓冲液 (pH 10.0-11.0)。空白对照为不添加酶的反应,每个pH值的实验均设置空白对照。以所测定不同pH缓冲液中的最高酶活作为100%酶活对照,其他pH条件下所测酶活以对照酶活的百分比表示。
HheTM的pH稳定性是将酶在不同pH的缓冲液 (如上所述) 中,于25 ℃条件下孵育24 h,然后测定酶残余活力,以不同pH下最初的酶活为100%酶活对照。
1.4.3 最适温度及热稳定性HheTM的最适反应温度通过测定底物(S)-ECHB在Na2HPO4-NaH2PO4 (50 mmol/L,pH 8.0) 缓冲液中不同温度 (20-70 ℃) 下的酶活来确定。空白对照为不添加酶的反应,每个温度的实验均设置空白对照。以所测的不同反应温度下最高酶活为100%酶活 (对照),其他温度条件下所测酶活以对照酶活的百分比表示。
HheTM的热稳定性是用Na2HPO4-NaH2PO4 (50 mmol/L,pH 8.0) 缓冲液配制适宜浓度的酶液,在不同温度下分别孵育不同时间,然后检测残余酶活力。以不同温度下最初的酶活为100%酶活对照。
1.4.4 底物特异性和动力学分析HheTM的底物特异性通过替换反应体系中的底物(S)-ECHB为(R)-ECHB、1,3-二氯-2-丙醇(1,3-Dichloro-2-propanol,1,3-DCP)、4-氯-3-羟基丁腈(4-Chloro-3-hydroxybutyronitrile),浓度均为40 mmol/L,按照1.4.1中酶活检测方法进行测定,底物1,3-DCP和4-氯-3-羟基丁腈的检测采用相应的气相色谱分析方法进行,以底物(S)-ECHB的酶活为100%对照。1,3-DCP及其环氧产物的气相色谱分析条件为:Agilent 7890A,色谱柱19091J-413 HP-5 (30 m×0.32 mm×0.25 µm),FID检测温度220 ℃,升温程序:50 ℃保持1 min,10 ℃/min升高到100 ℃保持1 min。1,3-DCP及其环氧产物的保留时间分别为4.1 min和2.3 min。4-氯-3-羟基丁腈检测方法与(S)-ECHB和(R)-ECHB的气相条件一样,其保留时间为3.3 min,其环氧产物没有标品,但进行酶活检测发现,HheTM对其活性很低。
卤醇脱卤酶HheTM的动力学参数测定以(S)-ECHB为底物,选用纯化后的HheTM,底物浓度从10-60 mmol/L,按照1.4.1中酶活检测方法进行测定。
1.4.5 不同金属离子及化学物质对酶活的影响不同的金属离子和化学物质加入到反应体系中,并预先在30 ℃孵育30 min,然后按照1.4.1酶活检测方法测定酶的残余活力,空白对照 (100%) 为未添加任何物质的酶活。金属离子包括Fe2+、Mg2+、Zn2+、Ni2+、Mn2+、Cu2+,均为硫酸盐,其终浓度分别为1 mmol/L和5 mmol/L。化学物质包括Tween-80 (1%和5%)、EDTA (1 mmol/L和10 mmol/L)、SDS (1 mmol/L和10 mmol/L)。
1.5 利用卤醇脱卤酶HheTM生物合成(R)-HN利用卤醇脱卤酶HheTM作为催化剂,从(S)-ECHB生物合成(R)-HN。反应体系为20 mL,选择Tris-H2SO4缓冲液 (50 mmol/L,pH 9.0),底物(S)-ECHB浓度为10 g/L和20 g/L,使用pH在线调控系统,自动流加10%的NaCN溶液,控制反应体系的pH维持在8.0-9.0,加入一定量纯化后的卤醇脱卤酶HheTM (200 mg/L) 于30 ℃条件下进行反应,每隔一定的时间取样200 µL,用800 µL的乙酸乙酯萃取,所得有机相用无水硫酸钠干燥后进行气相色谱仪分析。气相色谱检测条件与酶活测定方法中检测条件一致,得到(S)-ECHB和(R)-HN的保留时间分别为4.4 min和5.6 min。
2 结果与分析 2.1 卤醇脱卤酶序列比对及分析通过对已有的卤醇脱卤酶进行序列Blast分析后发现,同一类卤醇脱卤酶之间蛋白序列同源性很接近,其相似性为91%-98%;不同类的卤醇脱卤酶之间的Identity为24%-33% (表1)。然而我们新挖掘的HheTM与已有的3类卤醇脱卤酶的Identity在30%-38%之间,由此推测HheTM可能不属于已有的3类卤醇脱卤酶,是一种新的卤醇脱卤酶。利用BioEdit软件的ClustalW多重比对功能对以上所述的7种卤醇脱卤酶进行序列比对。序列比对的结果如图2所示,7种卤醇脱卤酶都含有卤醇脱卤酶的保守区-催化三联体Ser-Tyr-Arg (S-Y-R)。由此推测HheTM可能具有卤醇脱卤酶的性质,能够催化邻卤醇类化合物的脱卤反应及其逆反应 (环氧化物开环)。
| Group | Name | GenBank Accession No. | Identity (%) | ||||||
| HheA | HheA-AD2 | HheB | HheB-GP1 | HheC | HalB | HheTM | |||
| A | HheA | BAA14361 | 100 | ||||||
| HheA-AD2 | AAK92100 | 97 | 100 | ||||||
| B | HheB | BAA14362 | 24 | 24 | 100 | ||||
| HheB-GP1 | AAK73175 | 26 | 26 | 98 | 100 | ||||
| C | HheC | AAK92099 | 33 | 33 | 26 | 27 | 100 | ||
| HalB | AAD34609 | 31 | 31 | 26 | 26 | 91 | 100 | ||
| This work | HheTM | AFK51877 | 38 | 38 | 30 | 30 | 34 | 32 | 100 |

|
| 图2 卤醇脱卤酶序列比对结果 Fig.2 Amino acid sequence alignment of halohydrin dehalogenases from Arthrobacter sp. AD2 (HheA-AD2,GenBank Accession No. AAK92100),Corynebacterium strain N-1074 (HheA,GenBank Accession No. BAA14361),Mycobacterium sp. strain GP1 (HheB-GP1,GenBank Accession No. AAK73175),Corynebacterium strain N-1074 (HheB,GenBank Accession No. BAA14362),Agrobacterium radiobacter strain AD1 (HheC,GenBank Accession No. AAK92099),Agrobacterium tumefaciens (HalB,GenBank Accession No. AAD34609),and Tistrella mobilis KA081020-065 (HheTM,GenBank Accession No. AFK51877). |
将全基因合成的HheTM基因序列构建重组质粒pET32a(+)-HheTM,在大肠杆菌BL21 (DE3)中进行表达,Ni-NTA 纯化得到高纯度的目的蛋白。HheTM的表达及纯化结果见图3,纯化参数如表2所示。由图3可知,HheTM单体的分子量约为26.0 kDa,凝胶层析结果显示酶的分子量大约为101.2 kDa,说明其在溶液中以四聚体形式存在。

|
| 图3 HheTM蛋白纯化SDS-PAGE图 Fig.3 SDS-PAGE analysis of purified HheTM. M: standard proteins marker of different molecular weights; 1: HheTM before induction; 2: crude HheTM; 3: purified HheTM. |
| Purification step | Total protein (mg) | Total activity (U) | Specific activity (U/mg) | Purification (fold) | Yield (%) |
| Crude HheTM | 334.5 | 3 311.6 | 9.9 | 1.0 | 100.0 |
| Ni-NTA purified HheTM | 67.0 | 1 567.8 | 23.4 | 2.4 | 47.3 |
卤醇脱卤酶催化邻卤醇形成相应的环氧化物并导致卤化氢的生成,导致pH值的下降,而卤醇脱卤酶发挥催化作用的pH条件为碱性条件,所以研究pH对卤醇脱卤酶HheTM的影响时,选择的pH范围为6.0-11.0。以 (S)-ECHB为底物,卤醇脱卤酶HheTM在不同pH的缓冲液中酶活差异较大,在pH 10.0的条件下酶活最高,而在pH<7.0的条件下,HheTM的活性很低 (图4A)。HheTM的pH稳定性显示,在pH<7.0的条件下,HheTM孵育后的残余活力基本为零,说明HheTM可能已经失活。在pH >7.0的条件下,HheTM可以保持很高的稳定性,24 h后酶残余活力大于90% (图4B)。

|
| 图4 pH对卤醇脱卤酶HheTM的影响 Fig.4 Effect of pH on HheTM. (A) pH activity. (B) pH stability. For activity,the buffers were 50 mmol/L Na2HPO4-NaH2PO4 (pH 6.0-8.0),Tris-H2SO4 (pH 8.0-9.0),Glycine-NaOH (pH 9.0-10.0),and Na2HPO4-NaOH (pH 10.0-11.0). For pH stability,the purified HheTM was pre-incubated in different buffers at 25 °C for 24 h. |
HheTM在50 ℃表现出最高的活性,在35-50 ℃范围内,酶活力为峰值酶活的80%以上 (图5A)。HheTM的温度稳定性显示,HheTM在30 ℃条件下有很好的稳定性,孵育12 h,酶活无损失,在40 ℃条件下,HheTM的半衰期约为8 h,而在50 ℃条件下孵育2 h,HheTM基本失活 (图5B),说明HheTM在50 ℃条件下酶活很高,但其稳定性很差。

|
| 图5 温度对卤醇脱卤酶HheTM的影响 Fig.5 Effect of temperature on HheTM. (A) Activity. (B) Thermostability. For activity,the temperatures were 20-70 °C. For thermostability analysis,HheTM were incubated for 12 h at temperatures 30-50 °C,the activity of enzyme without pre-incubation was taken as 100%. |
HheTM对于不同底物活性检测结果见表3,HheTM对于(R)-ECHB和(S)-ECHB底物均有活性。在检测的4种底物中,HheTM对于底物(R)-ECHB的活性最高,而对于底物4-氯-3-羟基丁腈活性很低。以(S)-ECHB为底物测定动力学参数Km和kcat,结果如表4所示。
| Substrate | Relative activity (%) |
| (S)-ECHB | 100.0 |
| (R)-ECHB | 146.1 |
| 1,3-DCP | 50.4 |
| 4-chloro-3-hydroxybutyronitrile | 3.1 |
| Substrate | Km (mmol/L) | Kcat (s-1) | kcat/Km (L/(s·mmol)) |
| (S)-ECHB | 35.38±1.57 | 19.28±0.56 | 0.54 |
不同金属离子对HheTM活性的影响结果如表5所示,不同的金属二价离子均抑制了HheTM的活性,Fe2+、Zn2+、Cu2+离子对HheTM活性的影响作用尤为明显。表6显示,10 mmol/L的SDS的加入可以完全抑制HheTM的活性,而5%的Tween-80对HheTM的活性基本无影响,EDTA轻度抑制了HheTM的活性。
| Metal ions | Concentration (mmol/L) | Relative activity (%) |
| Control | 100.0±0.0 | |
| Fe2+ | 1 | 29.8±1.1 |
| 5 | 10.7±1.2 | |
| Mg2+ | 1 | 78.4±1.8 |
| 5 | 75.8±4.6 | |
| Zn2+ | 1 | 43.4±3.7 |
| 5 | 23.3±2.4 | |
| Mn2+ | 1 | 66.7±2.1 |
| 5 | 58.5±4.0 | |
| Cu2+ | 1 | 20.5±1.7 |
| 5 | 17.8±0.6 | |
| Ni2+ | 1 | 51.9±3.0 |
| 5 | 22.5±1.8 |
| Surfactants | Concentration | Relative activity (%) |
| Control | 100.0±0.0 | |
| Tween-80 | 1% (V/V) | 97.4±2.2 |
| 5% (V/V) | 97.1±1.3 | |
| SDS | 1 mmol/L | 1.2±0.2 |
| 10 mmol/L | 0.0 | |
| EDTA | 1 mmol/L | 87.8±2.4 |
| 10 mmol/L | 56.5±3.4 |
本文中介绍的卤醇脱卤酶HheTM与文献中报道的几个卤醇脱卤酶简单的性质比较见表7。通过比较发现,新的卤醇脱卤酶HheTM分子量与HheB-GP1相近;最适温度与HheA-AD2和HheC的最适温度相同,均为50 ℃;与卤醇脱卤酶DehB一样,Zn2+和Cu2+也是HheTM的抑制 剂。
| Microorganisms | Enzyme | Molecular weight (kDa) | Temperature optimum (℃) | pH optimum | Inhibitors | References |
| Arthrobacter sp. AD2 | HheA-AD2 | 29.0 | 50 | 8.5 | 2-Chloracetic acid | [11] |
| Mycobacerium sp. strain GP1 | HheB-GP1 | 26.2 | / | / | / | [8] |
| Agrobacterium strain NHG3 | DehB | 27.9 | 40-60 | 8.8-9.5 | 2-Chloracetic acid, Zn2+, Cu2+ | [13, 14] |
| Agrobacterium radiobacter AD1 | HheC | 27.9 | 50 | 8.0-9.0 | / | [8] |
| Tistrella mobilis KA081020-065 | HheTM | 26.0 | 50 | 9.0-10.0 | Zn2+, Cu2+, SDS | This work |
| /not mentioned. | ||||||
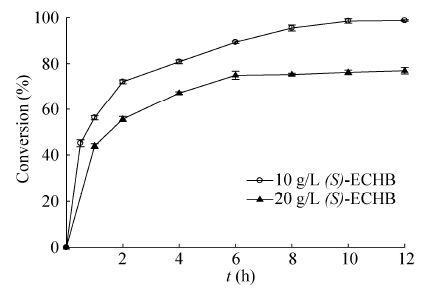
碱性是卤醇脱卤酶发挥脱卤作用以及形成亲核试剂氰离子 (HCN的pKa值大约为9) 的必要条件。然而,(S)-ECHB和 (R)-HN都是对碱性敏感的化合物,从而导致反应过程中副产物的产生[21]。由于HheTM 是新挖掘到的卤醇脱卤酶,选择较低的底物浓度 (10 g/L和20 g/L) 进行实验。结果发现,200 mg/L的酶量可以实现10 g/L的底物 (S)-ECHB转化为目的产物(R)-HN,30 ℃反应10 h,(S)-ECHB转化率达到98%。然而,对于20 g/L的底物,(S)-ECHB转化率只能达到75%左右 (图6)。
|
| 图6 (R)-HN的生物合成时间曲线图 Fig.6 The biosynthesis time course of (R)-HN by HheTM. Reaction condition: 50 mmol/L of Tris-H2SO4 (pH 9.0) 10 g/L and 20 g/L (S)-ECHB,200 mg/L HheTM with a final volume of 20 mL at 30 °C for 12 h. |
通过基因挖掘获得了来源于运动替斯崔纳菌Tistrella mobilis KA081020-065的新型卤醇脱卤酶基因,该酶与已有的3类卤醇脱卤酶同源性很低,属于新的卤醇脱卤酶。将该酶在大肠杆菌中进行表达纯化,并对其酶学性质进行了研究。结果表明,HheTM是一种同源四聚体;最适温度为50 ℃;不同的pH值缓冲液对其活性有较大影响;在碱性、30 ℃以下的条件下稳定性高。该酶能够催化(S)-4-氯-3-羟基丁酸乙酯,反应过程中加入CN-,可以合成阿托伐他汀关键中间体(R)-4-氰基-3-羟基丁酸乙酯。生物催化反应体系的底物浓度为10 g/L,酶浓度为200 mg/L,30 ℃反应10 h,底物转化率达到98%。HheTM对于(S)-4-氯-3-羟基丁酸乙酯的催化活性与文献中利用分子改造后的卤醇脱卤酶HheC [18]相比还有一定的差距。该酶与已知卤醇脱卤酶同源性较低,可能具有独特的底物谱和催化性质,在其他β-取代醇的合成中可能具有更好的应用价值和潜力,对底物谱进行扩大研究,也许有新发现。
| [1] | You ZY, Liu ZQ, Zheng YG. Properties and biotechnological applications of halohydrin dehalogenases: current state and future perspectives. Appl Microbiol Biotechnol, 2013, 97(1): 9-21. |
| [2] | Assis HMS, Bull AT, Hardman DJ. Synthesis of chiral epihalohydrins using haloalcohol dehalogenase A from Arthrobacter erithii H10a. Enzyme Microb Technol, 1998, 22(7): 545-551. |
| [3] | Jin HX, Hu ZC, Liu ZQ, et al. Nitrite-mediated synthesis of chiral epichlorohydrin using halohydrin dehalogenase from Agrobacterium radiobacter AD1. Biotechnol Applied Biochem, 2012, 59(3): 170-177. |
| [4] | Hasnaoui DG, Majeric EM, Lutje Spelberg JH, et al. Catalytic promiscuity of halohydrin dehalogenase and its application in enantioselective epoxide ring opening. Chembiochem, 2008, 9(7): 1048-1051. |
| [5] | Hasnaoui DG, Lutje Spelberg JH, De Vries EJ, et al. Nitrite-mediated hydrolysis of epoxides catalyzed by halohydrin dehalogenase from Agrobacterium radiobacter AD1: a new tool for the kinetic resolution of epoxides. Tetrahedron Asymmetry, 2005, 16(9): 1685-1692. |
| [6] | Hopmann KH, Himo F. Cyanolysis and azidolysis of epoxides by haloalcohol dehalogenase theoretical study of the reaction mechanism and origins of regioselectivity. Biochemistry, 2008, 47(17): 4973-4982. |
| [7] | Castro CE, Bartnicki EW. Biodehalogenation, epoxidation of halohydrins, epoxide opening, and transhalogenation by a Flavobacterium sp.. Biochemistry, 1968, 7(9): 3213-3218. |
| [8] | van Hylckama Vlieg JET, Tang LX, Lutje Spelberg JH, et al. Halohydrin dehalogenases are structurally and mechanistically related to short-chain dehydrogenases/reductases. J Bacteriol, 2001, 183(17): 5058-5066. |
| [9] | Tang LX, Jiang RC, Zheng K, et al. Enhancing the recombinant protein expression of halohydrin dehalogenase HheA in Escherichia coli by applying a codon optimization strategy. Enzyme Microb Technol, 2011, 49(4): 395-401. |
| [10] | Tang LX, Zhu XC, Zheng HY, et al. Key residues for controlling enantioselectivity of halohydrin dehalogenase from Arthrobacter sp. strain AD2, revealed by structure-guided directed evolution. Appl Environ Microbiol, 2012, 78(8): 2631-2637. |
| [11] | Vandenwijngaard AJ, Reuvekamp PTW, Janssen DB. Purification and characterization of haloalcohol dehalogenase from Arthrobacter sp. strain AD2. J Bacteriol, 1991, 173(1): 124-129. |
| [12] | Nakamura T, Nagasawa T, Yu F, et al. Characterization of a novel enantioselective halohydrin hydrogen-halide-lyase. Appl Environ Microbiol, 1994, 60(4): 1297-1301. |
| [13] | Higgins KH, Hope SJ, Effendi AJ, et al. Biochemical and molecular characterisation of the 2,3-dichloro-1-propanol dehalogenase and stereospecific haloalkanoic dehalogenases from a versatile Agrobacterium sp.. Biodegradation, 2005, 16(5): 485-492. |
| [14] | Effendi AJ, Greenaway SD, Dancer BN. Isolation and characterization of 2,3-dichloro-1-propanol- degrading Rhizobia. Appl Environ Microbiol, 2000, 66(7): 2882-2887. |
| [15] | de Jong RM, Kalk KH, Tang L, et al. The X-ray structure of the haloalcohol dehalogenase HheA from Arthrobacter sp. strain AD2: insight into enantioselectivity and halide binding in the haloalcohol dehalogenase family. J Bacteriol, 2006, 188(11): 4051-4506. |
| [16] | de Jong RM, Rozeboom HJ, Kalk KH, et al. Crystallization and preliminary X-ray analysis of an enantioselective halohydrin dehalogenase from Agrobacterium radiobacter AD1. Acta Crystallogr D, 2002, 58(1): 176-178. |
| [17] | Tang LX, Lutje Spelberg JH, Fraaije MW, et al. Kinetic mechanism and enantioselectivity of halohydrin dehalogenase from Agrobacterium radiobacter. Biochemistry, 2003, 42(18): 5378-5386. |
| [18] | de Jong RM, Tiesinga JJW, Rozeboom HJ, et al. Structure and mechanism of a bacterial haloalcohol dehalogenase: a new variation of the short-chain dehydrogenase_reductase fold without an NAD(P)H binding site. Embo J, 2003, 22(19): 4933-4944. |
| [19] | Tang LX, Pazmino DET, Fraaije MW, et al. Improved catalytic properties of halohydrin dehalogenase by modification of the halide-binding site. Biochemistry, 2005, 44(17): 6609-6618. |
| [20] | Fox RJ, Davis SC, Mundorff EC, et al. Improving catalytic function by ProSAR-driven enzyme evolution. Nat Biotechnol, 2007, 25(3): 338-344. |
| [21] | Ma SK, Gruber J, Davis C, et al. A green-by-design biocatalytic process for atorvastatin intermediate. Green Chem, 2010, 12(1): 81-86. |
| [22] | Patel JM. Biocatalytic synthesis of atorvastatin intermediates. J Mol Catal B Enzym, 2009, 61(3/4): 123-128. |
| [23] | Xu Y, Kersten RD, Nam SJ, et al. Bacterial biosynthesis and maturation of the didemnin anti-cancer agents. J Am Chem Soc, 2012, 134(20): 8625-8632. |
 2015, Vol. 31
2015, Vol. 31




