服务
文章信息
- 郭磊, 孔建强
- Guo Lei, Kong Jianqiang
- 匹诺塞林合成生物学研究进展
- Progress in synthetic biology of pinocembrin
- 生物工程学报, 2015, 31(4): 451-460
- Chin J Biotech, 2015, 31(4): 451-460
- 10.13345/j.cjb.140367
-
文章历史
- Received: July 14, 2014
- Accepted: September 17, 2014
匹诺塞林 (Pinocembrin) 属于二氢黄酮,是黄酮类化合物生物合成途径中重要的中间产物,经过羟基化、烷基化、糖基化或氧化等反应可生成其他黄酮。匹诺塞林最早发现于蜂胶,在蜂胶所含的黄酮类化合物中其含量最丰富[1]。由于具有一个手性中心,匹诺塞林存在一对光学异构体,自然界中发现的均为S构型。
1 匹诺塞林生物活性匹诺塞林具有良好的生物活性,如神经保护、抗菌、抗氧化等,其中神经保护方面活性使其具有极高的成药性,在2009年匹诺塞林被CFDA批准为Ⅰ类注射新药,主要适应症为急性脑卒中[2]。
1.1 神经保护匹诺塞林对急性脑缺血具有良好的保护作用,可以减小脑梗塞面积,保护脑线粒体结构,减轻缺血再灌注后对血脑屏障的损伤及舒张血管。
在发生缺血再灌注时,因供氧不足会导致脑线粒体呼吸链损伤[3]。对于急性脑缺血模型[4, 5, 6, 7],匹诺塞林可以保护线粒体结构形态,改善线粒体氧化磷酸化偶联程度,增强氧化磷酸化效率,促进线粒体呼吸功能,提高线粒体ATP合成能力而发挥脑缺血保护作用。在细胞水平,匹诺塞林能促进SH-SY5Y细胞中ATP的生成;在动物试验中发现它能够显著增加急性脑缺血模型大鼠脑线粒体的ADP/O、V3及RCI、OPR等参数值,保护线粒体结构完整性。对于慢性脑缺血模型[8, 9],匹诺塞林可以改善大鼠认知障碍,减少脑线粒体内活性氧生成,提高线粒体膜膜电位,降低线粒体肿胀程度。此外,匹诺塞林对全脑缺血再灌注模型大鼠血脑屏障具有保护作用[10]。
研究还发现匹诺塞林对阿尔茨海默氏病相关缺陷神经血管单元具有保护作用。Liu等[11]对APP/PS1转基因小鼠连续给药,发现匹诺塞林能够保护神经纤维超微架构、减少活化的胶质细胞、降低炎症因子水平、改善胆碱能系统和RAGE介导的转导功能、减轻纤维状β1-42淀粉样蛋白对神经血管单元 (NVU) 的损害等。另外,匹诺塞林还具有舒张血管作用[12]。
1.2 抗菌匹诺塞林和许多黄酮类化合物均具有抗菌活性。Koo等[13]对蜂胶中的天然化合物进行了抗菌活性实验,结果表明 (2S)-匹诺塞林抗菌活性最高。随后科学家们采取平皿稀释法、纸碟法和Denlay多点接种法等对匹诺塞林进行了大量体内外抑菌实验,结果表明匹诺塞林对革兰氏阳性菌的抑制能力要强于革兰氏阴性菌,同时对某些耐药菌也有抑制作用[14, 15]。
1.3 抗氧化匹诺塞林抗氧化作用表现在能清除自由基、抑制脂质过氧化和清除二价金属阳离子等。Santos等[16]在研究天然类黄酮对脂质过氧化作用时,发现匹诺塞林对其具有抑制作用,特别是ADP/Fe (Ⅱ)-诱导的脂质过氧化。Estevinho等[17]从蜂胶分离出酚类化合物,并研究了其生物活性,结果表明匹诺塞林可以减少DPPH自由基和降低Fe3+/铁氰化合物的比值。
1.4 其他匹诺塞林具有抗癌活性,能杀伤结肠癌细胞系 (HCT116),可能是通过依赖Bax蛋白的线粒体凋亡机制来诱导肿瘤细胞凋亡[18, 19]。匹诺塞林还具有其他药理活性,例如抗原虫、抗诱变、抑制睾丸酮5-还原酶、抑制酪氨酸酶、抑制葡萄糖基转移酶、抑制肥大细胞及中性粒细胞分泌和局部麻醉等[16, 17, 20]。
2 匹诺塞林的生物合成目前,匹诺塞林可以通过化学合成、植物提取以及合成生物学技术进行制备。匹诺塞林常采用查尔酮闭环合成法进行化学合成[14],虽然该方法可以快速得到产物,但需要使用大量有毒化学试剂,反应条件较苛刻,能源消耗大且该方法的产物是消旋体,然而只有S构型产物具有生物活性。匹诺塞林广泛存在于植物中,Rasul等[21]归纳了匹诺塞林在植物界和在植物组织中的分布。尽管匹诺塞林在植物中广泛分布,但含量低、植物组织中物质成分复杂和分离纯化困难等一系列问题大大限制植物提取方法的应用。此外,植物资源的保护也是必须考虑的因素。
相比于化学合成和植物提取,生物合成方法具有原料价廉、反应要求较低、能耗低和环境友好等特点,具有很好的发展前景。此外,匹诺塞林生物合成途径较短,利用微生物合成相对容易。
匹诺塞林生物合成途径的解析及关键酶的研究是应用合成生物学技术制备该化合物的基础。现已知黄酮类化合物的生物合成主要经由莽草酸途径和多酮化途径。如图1所示,莽草酸途径来源的苯丙氨酸和酪氨酸作为前体物质,分别经苯丙氨酸裂解酶 (Phenylalanine ammonia lyase,PAL) 和酪氨酸裂解酶 (Tyrosine ammonia lyase,TAL) 裂解后生成肉桂酸和对香豆酸[22]。肉桂酸也可以在肉桂酸4-羟化酶 (Cinnamate 4-hydroxylase,C4H) 作用下形成对香豆酸[23]。对香豆酸辅酶A连接酶 (4-Coumaroyl CoA ligase,4CL) 可同时催化肉桂酸和对香豆酸在其羰基上连接CoA分别生成肉桂酰CoA和对香豆酰CoA,二者在查尔酮合酶 (Chalcone synthase,CHS) 催化下与丙二酰CoA缩合环化分别生成匹诺塞林查尔酮 (Pinocembrin chalcone) 和柚皮素查尔酮 (Naringenin chalcone),随后经查尔酮异构酶 (Chalcone isomerase,CHI) 作用生成S构型的匹诺塞林 ((2S)-Pinocembrin) 和柚皮素 ((2S)-Naringenin)。二者作为黄酮代谢中间产物可以生成其他类黄酮,例如异黄酮合成酶 (Isoflavone synthase,IFS) 将其催化为异黄酮,黄酮合成酶 (Flavone synthase,FNS) 可以催化其生成黄酮,黄烷酮3-羟化酶 (Flavanone 3-hydroxylase,F3H) 和黄酮醇合成酶 (Flavonol synthase,FLS) 联合作用下生成黄酮醇等。

|
| 图1 黄酮类化合物生物合成途径 Fig.1 The pathway of flavonoids biosynthsis. |
构建匹诺塞林工程菌是应用合成生物学技术进行生产的首要问题。匹诺塞林的代谢途径如图1所示,运用基因工程的方法将不同物种来源的关键酶基因,如PAL、4CL、CHS和CHI等,按照最适优化的原则构建成不同模块,然后导入底盘细胞,在这些宿主中重构一条匹诺塞林的生物合成途径,通过这些构建的工程菌,制备匹诺塞林。高效的合成途径往往不仅受限于单一的限速酶促反应,而是需要多个酶促反应之间的相互协调。利用代谢工程手段对代谢网络进行调节,使代谢流最大程度流向匹诺塞林[24]。最后,从生理性能和生产环境适应能力方面对工程菌进行优化,使之成为实际生产可用的高产菌株[25]。
3 提高匹诺塞林生物合成的策略随着代谢工程和合成生物学的发展,利用微生物进行异源合成黄酮类化合物成为研究热点,自2003年起人们对利用微生物异源合成黄酮类化合物表现出极大的兴趣[26]。虽然生物合成法具有很大优势,但产量低这一难题严重阻碍了该法在大规模生产中的应用。科研人员进行了大量实验,采取了多种方法让代谢流最大程度流向黄酮类化合物。本文将从以下几点来阐述提高微生物合成匹诺塞林的策略。
3.1 选择高活性的酶来自同一家族的酶,由于物种来源不同其催化活性往往不同,在构建工程菌时一般选择酶活性高的物种[27, 28, 29]。Lonard等[30]以大肠杆菌为底盘细胞,构建工程菌E1,选取矮牵牛Petunia hybrid来源的CHI,同时构建菌株E2,其CHI来源于紫花苜蓿Medicago sativa,经发酵发现菌株E2的匹诺塞林产量远高于菌株E1,紧接着将紫花苜蓿的CHI活性和其他物种来源的CHI活性进行了对比,发现仍是前者活性高。Park等[31]发现拟南芥的CHS活性高于矮牵牛的CHS,前者匹诺塞林的产量为6.0 mg/L,后者的产量却小于0.1 mg/L。
此外,由于密码子偏爱性会对蛋白异源性表达产生影响,从而降低其催化能力。为了提高异源蛋白表达水平,在选定酶物种来源后,常采取密码子优化的方法来解决异源性表达降低所带来酶活性降低这一问题[32]。Santos等[33]利用类球红细菌Rhodobacter glutinis 的RgTAL、拟南芥AtCHS、链霉菌Streptomyces coelico的Sc4CL和葛根Pueraria lobata的PlCHI构建了工程菌pCS204,表达后发现蛋白表达量不高。对上述4种蛋白表达所需密码子进行分析后发现在参与翻译RgTAL的密码子中有41个是稀有密码子,AtCHS为33个,Sc4CL为32个。紧接着对RgTAL进行优化,优化后的RgTALsyn催化生成对香豆酸的产量为104 mg/L,而未优化组产量仅为5.5 mg/L。
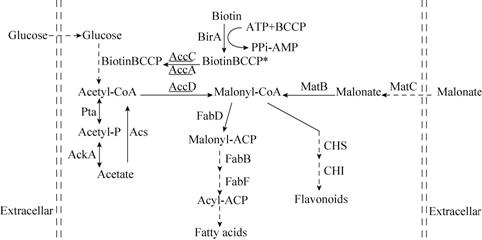
3.2 提高丙二酰CoA的含量利用微生物合成黄酮化合物面临诸多挑战,底盘细胞内前体物质的供给就是其中之一,如丙二酰CoA的供给。三分子丙二酰CoA和一分子的肉桂酰CoA在CHS催化下生成匹诺塞林查尔酮,该步是微生物合成黄酮类化合物的关键步骤[34]。丙二酰CoA代谢途径如图2所示:1) 由葡萄糖代谢产生的乙酰CoA在乙酰CoA羧化酶 (Acetyl-CoA carboxylase,ACC) 作用下生成丙二酰CoA;2) 丙二酸盐在丙二酸盐载体蛋白 (Malonate carrier protein,MatC) 作用下进行跨膜运输,进入细胞后经丙二酰CoA合酶 (Malonyl-CoA synthase,MatB) 催化生成丙二酰CoA;3) 丙二酰CoA降解途径,除了参与黄酮类化合物合成外,还可以以丙二酰-ACP为中间体形式参与TAC循环。研究表明微生物胞内丙二酰CoA含量非常低且无法外源性添加,Takamura 等[35]研究表明在以葡萄糖为碳源时,E. coli细胞内的乙酰CoA的含量为200-600 μmol/L,而丙二酰CoA含量仅为4-90 μmol/L。围绕如何提高细胞内丙二酰CoA含量而采取的策略可归纳为对丙二酰CoA代谢的开源节流。
|
| 图2 丙二酰CoA生物合成途径 Fig.2 The pathway of malonyl CoA biosynthsis. |
乙酰CoA经ACC催化直接生成丙二酰基CoA,首先选取该酶作为调控目标。ACC含有4个亚单位,分别由accA、accB、accC和accD编码。Leonard等[30]选择革兰氏阴性菌发光杆菌Photorhabdus luminescens来源的accA和accD,将二者构建在一个质粒 (由一个T7启动子控制)上,accB和accC构建在另一质粒 (由独立的T7启动子控制) 上,两质粒与欧洲芹Pc4CL2、PhCHS和紫花苜蓿来源MsCHI共转表达后匹诺塞林的产量可以达到196 mg/L。ACC是一种生物素依赖的羧化酶,其功能的发挥需要生物素作为辅助因子,由ACC-生物素连接酶 (BPL,birA编码) 介导二者相互连接。为了提高ACC的催化效率,研究人员通过构建含有birA的质粒来上调BPL的表达。通过共表达ACC、BPL和上述3种酶,匹诺塞林产量可以高达367 mg/L。
提高乙酰CoA的含量可以增加胞内丙二酰CoA的含量,故抑制乙酰CoA代谢可以达到开源的效果。生成乙酸是乙酰CoA代谢去路之一,另外在发酵过程中乙酸还会对大肠杆菌产生生长抑制[36],故对乙酸生成途径进行抑制具有一举两得之效。乙酰CoA与乙酸之间相互转化有两种途径,如图2所示:1) 磷酸转乙酰基酶催化乙酰CoA生成Acetyl-P,再经乙酸激酶催化生成乙酸;2) 乙酸可以由乙酰CoA合成酶催化生成乙酰CoA。质粒pCOLADuet-ackA-pta和质粒pCOLADuet-acs分别与由PlACC、Pc4CL2、PhCHS和MsCHI构成的上游模块共转后进行发酵,检测乙酸和匹诺塞林的含量,实验表明AckA-Pta途径所产生的乙酸比Acs途径高,其原因可能是前者为可逆途径。实验中还发现在含有葡萄糖的培养基中添加2 g/L乙酸,上述菌株的匹诺塞林产量可高达429 mg/L[30]。
3.2.2 开源2——提高MatC和MatB的表达如图2所示,细胞外的丙二酸盐由MatC进行跨膜运输,进入细胞后在MatB催化下生成丙二酰基CoA[37]。将由4CL、CHS和CHI构建的上游代谢模块与由MatB和MatC构成的丙二酰CoA合成模块进行适配性组装,在含有2 g/L丙二酸盐的M9培养基中培养,与仅有上游代谢模块的工程菌相比,匹诺塞林产量从29 mg/L升高到480 mg/L,增加了14.6倍[38]。
3.2.3 节流——抑制脂肪酸代谢丙二酰CoA除了参与黄酮生物合成还可以在FabD、FabB和FabF等酶作用下生成acyl-ACP参与TAC循环。浅蓝菌素 (Cerulenin) 可以抑制FabB和FabF,将含有匹诺塞林基础代谢途径菌株E2在M9培养基上培养,虽然添加浅蓝菌素后生物量会降低,但匹诺塞林产量会大大提高,高达710 mg/L,这是目前利用微生物合成匹诺塞林所有文献中产量最高的报道[38]。令人遗憾的是浅蓝菌素价格昂贵大大限制了这一方法的应用。
3.3 选择经济的底物通过合成生物学技术合成匹诺塞林时,底物的选择取决于代谢途径中相关酶种类的选择。底物的价格是实际生产中必须考虑的一个因素。Santos等[33]构建了一条经济的合成途径,无需直接添加前体氨基酸,而是使用更为廉价的葡萄糖作为碳源就可直接合成黄酮类物质。首先在大肠杆菌中构建酪氨酸代谢途径,使其能够产生较高浓度的酪氨酸,然后以此为底盘细胞并嵌入密码子优化的RgTAL、Sc4CL、PhCHS和MsCHI构建黄酮合成模块。Wu等[39]构建4个质粒模块,模块1包含糖代谢相关基因3-脱氧-D-阿拉伯庚酮糖酸-7-磷酸合酶基因和预苯酸脱水酶基因,模块2包含将苯丙氨酸转化为肉桂酰CoA的PAL和4CL,模块3包含将肉桂酰CoA转化为匹诺塞林的CHS和CHI,模块4含有将丙二酸盐催化为丙二酰基CoA的MatB和MatC。工程菌只需在仅有葡萄糖的MOPS培养基中培养,采用一步发酵法就可以达到生物量和匹诺塞林产量均很高的效果。
3.4 减弱中间产物的抑制作用一条代谢通路往往由多个酶构成,中间产物可能会对上游酶活性产生抑制。中间产物含量往往与相关的酶表达水平直接相关,故通过调控相关蛋白的表达水平以降低中间产物含量,进而削弱抑制作用。蛋白的表达水平可以由表达载体拷贝数和启动子强度综合决定,即由二者的乘积来量化[40]。质粒pACYCDuet-1、pCDFDuet-1、pETDuet-1和pRSFDuet-1的拷贝数分别是10、20、40和100,T7启动子的强度为5。由于4CL的催化产物会对TAL/PAL的催化能力产生抑制,Wu等[39]针对这一现象构建了均由T7启动子控制的4个质粒模块,将4CL克隆到拷贝数低的pACYCDuet-1载体上,而将CHS和CHI克隆到拷贝数最高的pRSFDuet-1载体上,这样4CL表达水平为50而CHS和CHI为500,结果为4CL产物肉桂酰CoA会被相对过量CHS及时代谢而避免对PAL产生的反馈抑制,该组匹诺塞林产量较对照组 (PAL表达水平为200,CHS和CHI表达水平为100) 提升了3.4倍。
3.5 其他宿主菌会对产率产生一定影响。在这一问题上,人们几乎都选择了大肠杆菌作为匹诺塞林的表达宿主菌。基因工程中常用的真核生物酵母菌可以对蛋白进行翻译后修饰,但是在黄酮的生物合成过程中很少选择酵母菌。Jiang等[41]利用酵母构建了匹诺塞林工程菌,其产量仅为0.8 mg/L。酵母细胞与植物细胞进化关系更近,其含有的内质网系统能够进行NADPH的质子传递,这为C4H的表达及活性的保持提供了良好的条件,但是人们在选择黄酮代谢途径时往往绕开C4H,这可能是较少选择酵母表达系统的一个原因。链霉菌具有细胞内营养丰富、生长较快和基因操作简单等优点,研究人员也尝试选择其作为匹诺塞林的宿主菌[31, 42]。
此外,随着计算机技术的进步,人们不再局限在与目的产物直接相关的代谢途径上,而是整个代谢网络。尽管细胞内物质代谢网络具有复杂性和代谢流动态性,但计算机完全可以模拟胞内情况,以便在更大范围找到可调控点[43]。Fowler等[44]建立了CiED模型,通过模拟找到了18种提高丙二酰CoA的敲除基因方法并进行了实验验证。Xu等[45]利用Optforce方法对大肠杆菌的碳代谢途径进行分析优化,发现在对某些基因敲除后可以大大提升产量。
4 结论与展望随着基因工程和代谢工程的发展,合成生物学取得了巨大进步,利用微生物合成黄酮类化合物也取得了令人瞩目的成果,然而利用微生物发酵仍存在异源性表达效果不好、产率不高和代谢途径各个环节之间不能最优化适配等问题。研究人员正积极地运用现代技术寻求提高黄酮类化合物产量的方法。作为我国自主研发的Ⅰ类新药,匹诺塞林现已经以注射剂的剂型进入Ⅱ期临床试验。对于这一具备成药前景的化合物,利用微生物合成方法进行生产不仅会大大降低市场价格,且有利于环境的可持续发展。合成生物学技术合成匹诺塞林的研究具有很好的科研价值和社会意义,如何更好地改善微生物合成方法合成匹诺塞林,将是研究者们亟待解决的下一个问题。
| [1] | Bankova VS, Popov SS, Marekov NL. High-performance liquid chromatographic analysis of flavonoids from propolis. J Chromatogr A, 1982, 242(1): 135-143. |
| [2] |
Cai XB, Cao GY, Sun TH, et al. The absorption text of classⅠnew drug pinocembrin (DL0108) for injection in vivo. Chin J Hosp Pharm, 2012, 32(19): 1582-1583 (in Chinese). 蔡小兵, 曹国颖, 孙韬华, 等. Ⅰ类新药注射用匹诺塞林 (DL0108) 体外吸附性试验. 中国医院药学杂志, 2012, 32(19): 1582-1583. |
| [3] |
Zhu XM. Studies on the discovery of new drugs for preventing and treating vascular diseases [D]. Beijing: Peking Union Medical College, 2008 (in Chinese). 竺晓鸣. 血管源性疾病新型防治药物发现的研究[D]. 北京: 北京协和医学院, 2008. |
| [4] | Simpkins AN, Rudic RD, Schreihofer DA, et al. Soluble epoxide inhibition is protective against cerebral ischemia via vascular and neural protection. Am J Pathol, 2009, 174(6): 2086-2095. |
| [5] | Zhang W, Koerner IP, Noppens R, et al. Soluble epoxide hydrolase: a novel therapeutic target in stroke. J Cereb Blood Flow Metab, 2007, 27(12): 1931-1940. |
| [6] | Wang SB, Pang XB, Gao M, et al. Pinocembrin protects rats against cerebral ischemic damage through soluble epoxide hydrolase and epoxyeicosatrienoic acids. Chin J Nat Med, 2013, 11(3): 207-213. |
| [7] |
Shi LL, Qiang GF, Du GH. Effect of pinocembrin on brain mitochondrial respiratory function. Acta Pharm Sin, 2011, 46(6): 642-649 (in Chinese). 时丽丽, 强桂芬, 杜冠华. 匹诺塞林对脑线粒体呼吸功能的促进作用. 药学学报, 2011, 46(6): 642-649. |
| [8] | Wang Y, Gao J, Miao Y, et al. Pinocembrin protects SH-SY5Y cells against MPP+-induced neurotoxicity through the mitochondrial apoptotic pathway. J Mol Neurosci, 2014, 53(4): 537-545. |
| [9] |
Guang HM, Gao M, Zhu SY, et al. The effect of pinocembrin on the mitochondria in brain after acute focal cerebral ischemia in rats. Chin Pharmacol Bull, 2012, 28(1): 24-29 (in Chinese). 光红梅, 高梅, 朱深银, 等. 匹诺塞林对急性局灶性脑缺血大鼠脑线粒体功能的影响. 中国药理学通报, 2012, 28(1): 24-29. |
| [10] | Meng F, Liu R, Gao M, et al. Pinocembrin attenuates blood-brain barrier injury induced by global cerebral ischemia-reperfusion in rats. Brain Res, 2011, 1391: 93-101. |
| [11] | Liu R, Gao M, Yang ZH, et al. Pinocembrin protects rat brain against oxidation and apoptosis induced by ischemia-reperfusion both in vivo and in vitro. Brain Res, 2008, 1216: 104-115. |
| [12] | Li L, Yang HG, Yuan TY, et al. Rho kinase inhibition activity of pinocembrin in rat aortic rings contracted by angiotensin II. Chin J Nat Med, 2014, 11(3): 258-263. |
| [13] | Koo H, Rosalen PL, Cury JA, et al. Effects of compounds found in propolis on Streptococcus mutans growth and on glucosyltransferase activity. Antimicrob Agents Chemother, 2002, 46(5): 1302-1309. |
| [14] |
Duan YB, Qi Y, Wu S. Synthesis and antimicrobial activity of pinocembrin and its derivatives. Chin J Med Chem, 2006, 16(6): 342-346 (in Chinese). 段亚波, 戚燕, 吴松. 松属素及其衍生物的合成与抗菌活性. 中国药物化学杂志, 2006, 16(6): 342-346. |
| [15] | Fukui H, Goto K, Tabata M. Two antimicrobial flavanones from the leaves of Glycyrrhiza glabra. Chem Pharm Bull, 1988, 36(10): 4174-4176. |
| [16] | Santos AC, Uyemura SA, Lopes JL, et al. Effect of naturally occurring flavonoids on lipid peroxidation and membrane permeability transition in mitochondria. Free Radic Biol Med, 1998, 24(9): 1455-1461. |
| [17] | Estevinho L, Pereira AP, Moreira L, et al. Antioxidant and antimicrobial effects of phenolic compounds extracts of Northeast Portugal honey. Food Chem Toxicol, 2008, 46(12): 3774-3779. |
| [18] | Kumar M, Nair M, Hema P, et al. Pinocembrin triggers Bax-dependent mitochondrial apoptosis in colon cancer cells. Mol Carcinog, 2007, 46(3): 231-241. |
| [19] | Žižič JB, Vukovič NL, Jadranin MB, et al. Chemical composition, cytotoxic and antioxidative activities of ethanolic extracts of propolis on HCT-116 cell line. J Sci Food Agric, 2013, 93(12): 3001-3009. |
| [20] | Sala A, Recio MC, Schinella GR, et al. Assessment of the anti-inflammatory activity and free radical scavenger activity of tiliroside. Eur J Pharmacol, 2003, 461(1): 53-61. |
| [21] | Rasul A, Millimouno FM, Ali Eltayb W, et al. Pinocembrin: a novel natural compound with versatile pharmacological and biological activities. Biomed Res Int, 2013, 2013: 379850. |
| [22] | Wang ZB, Chen X, Wang W, et al. Transcriptome-wide identification and characterization of Ornithogalum saundersiae phenylalanine ammonia lyase gene family. RSC Advances, 2014, 4(52): 27159-27175. |
| [23] | Kong JQ, Lu D, Wang ZB. Molecular cloning and yeast expression of cinnamate 4-hydroxylase from Ornithogalum saundersiae baker. Molecules, 2014, 19(2): 1608-1621. |
| [24] | Cho A, Yun H, Park JH, et al. Prediction of novel synthetic pathways for the production of desired chemicals. BMC Syst Biol, 2010, 4(1): 35. |
| [25] |
Dai ZB, Zhu XN, Zhang XL. Synthetic biology for construction of microbial cell factories. Chin Bull Life Sci, 2013, 25(10): 943-951 (in Chinese). 戴住波, 朱欣娜, 张学礼. 合成生物学在微生物细胞工厂构建中的应用. 生命科学, 2013, 25(10): 943-951. |
| [26] | Kaneko M, Hwang EI, Ohnishi Y, et al. Heterologous production of flavanones in Escherichia coli: potential for combinatorial biosynthesis of flavonoids in bacteria. J Ind Microbiol Biotechnol, 2003, 30(8): 456-461. |
| [27] | Fowler ZL, Koffas MA. Biosynthesis and biotechnological production of flavanones: current state and perspectives. Appl Microbiol Biotechnol, 2009, 83(5): 799-808. |
| [28] | Seo SW, Kim SC, Jung GY. Synthetic regulatory tools for microbial engineering. Biotechnol Bioprocess Eng, 2012, 17(1): 1-7. |
| [29] | Zhou YJ, Gao W, Rong Q, et al. Modular pathway engineering of diterpenoid synthases and the mevalonic acid pathway for miltiradiene production. J Am Chem Soc, 2012, 134(6): 3234-3241. |
| [30] | Leonard E, Lim KH, Saw PN, et al. Engineering central metabolic pathways for high-level flavonoid production in Escherichia coli. Appl Environ Microbiol, 2007, 73(12): 3877-3886. |
| [31] | Park SR, Yoon JA, Paik JH, et al. Engineering of plant-specific phenylpropanoids biosynthesis in Streptomyces venezuelae. J Biotechnol, 2009, 141(3/4): 181-188. |
| [32] | Kane JF. Effects of rare codon clusters on high-level expression of heterologous proteins in Escherichia coli. Curr Opin Biotechnol, 1995, 6(5): 494-500. |
| [33] | Santos CNS, Koffas M, Stephanopoulos G. Optimization of a heterologous pathway for the production of flavonoids from glucose. Metab Eng, 2011, 13(4): 392-400. |
| [34] | Zha W, Rubin-Pitel SB, Shao Z, et al. Improving cellular malonyl-CoA level in Escherichia coli via metabolic engineering. Metab Eng, 2009, 11(3): 192-198. |
| [35] | Takamura Y, Nomura G. Changes in the intracellular concentration of acetyl-CoA and malonyl-CoA in relation to the carbon and energy metabolism of Escherichia coli K12. J Gen Microbiol, 1988, 134(8): 2249-2253. |
| [36] | Russell JB, Diez-Gonzalez F. The effects of fermentation acids on bacterial growth. Adv Microb Physiol, 1998, 39: 205-234. |
| [37] | An JH, Kim YS. A gene cluster encoding malonyl-CoA decarboxylase (MatA), malonyl-CoA synthetase (MatB) and a putative dicarboxylate carrier protein (MatC) in Rhizobium trifolii. Eur J Biochem, 1998, 257(2): 395-402. |
| [38] | Leonard E, Yan Y, Fowler ZL, et al. Strain improvement of recombinant Escherichia coli for efficient production of plant flavonoids. Mol Pharm, 2008, 5(2): 257-265. |
| [39] | Wu J, Du G, Zhou J, et al. Metabolic engineering of Escherichia coli for (2S)-pinocembrin production from glucose by a modular metabolic strategy. Metab Eng, 2013, 16: 48-55. |
| [40] | Ajikumar PK, Xiao WH, Tyo KE, et al. Isoprenoid pathway optimization for Taxol precursor overproduction in Escherichia coli. Science, 2010, 330(6000): 70-74. |
| [41] | Jiang H, Wood KV, Morgan JA. Metabolic engineering of the phenylpropanoid pathway in Saccharomyces cerevisiae. Appl Environ Microbiol, 2005, 71(6): 2962-2969. |
| [42] | Park SR, Park JW, Jung WS, et al. Heterologous production of epothilones B and D in Streptomyces venezuelae. Appl Microbiol Biotechnol, 2008, 81(1): 109-117. |
| [43] | Tepper N, Shlomi T. Predicting metabolic engineering knockout strategies for chemical production: accounting for competing pathways. Bioinformatics, 2010, 26(4): 536-543. |
| [44] | Fowler ZL, Gikandi WW, Koffas MA. Increased malonyl coenzyme A biosynthesis by tuning the Escherichia coli metabolic network and its application to flavanone production. Appl Environ Microbiol, 2009, 75(18): 5831-5839. |
| [45] | Xu P, Ranganathan S, Fowler ZL, et al. Genome-scale metabolic network modeling results in minimal interventions that cooperatively force carbon flux towards malonyl-CoA. Metab Eng, 2011, 13(5): 578-587. |
 2015, Vol. 31
2015, Vol. 31