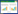服务
文章信息
- 蒋晓燕, 陆强, 董晓晨, 陈晨, 董长青
- Jiang Xiaoyan, Lu Qiang, Dong Xiaochen, Chen Chen, Dong Changqing
- α-O-4型木质素二聚体模型物热解解聚机理
- Pyrolytic depolymerization mechanism of a lignin model compound with α-O-4 linkage
- 生物工程学报, 2015, 31(10): 1512-1519
- Chin J Biotech, 2015, 31(10): 1512-1519
- 10.13345/j.cjb.140535
-
文章历史
- Received: November 9, 2014
- Accepted: January 26, 2015
生物质是一种廉价、储量丰富的可再生资源,其高效清洁制备燃料与化学品有着广阔的应用前景[1]。快速热解是一种重要的生物质转化技术,通过在中温条件下对生物质进行快速热解可将其主要转化为液体产物生物油[2, 3],与生物质相比,液体生物油不仅具有易储存、易运输和能量密度高等优点,而且还可以作为液体燃料或者化工原料进行广泛应用[4, 5]。
木质素是生物质的重要组成成分,也是自然界中可再生芳基化合物的重要来源[5, 6];此外,造纸等工业生产会产生大量的木质素副产物,目前利用率极低[7]。在生物质或工业木质素的快速热解过程中,木质素会形成大量的酚类产物,是一种重要的芳香族资源。为了更好地调控木质素热解过程以实现选择性制备特定的酚类衍生物,需要首先深入了解木质素的热解机理与产物形成途径,从而为开发高效的生物质/木质素选择性热解技术提供理论依据。然而,由于木质素的组成结构极为复杂,现阶段对其热解机理还缺乏深入了解。密度泛函理论计算是一种行之有效的生物质热解机理分析方法,目前,国内外一些学者采用该方法,已经针对一些木质素模型化合物,研究了其热解反应机理[8, 9, 10, 11, 12],所采用的模型化合物主要是β-O-4连接的木质素二聚体,这是由于β-O-4是木质素结构单元之间最主要的连接方式[5]。α-O-4也是一种较为重要的连接方式,一般是仅次于β-O-4的醚键连接方式[13, 14],但目前对于这种连接方式的木质素二聚体的热解研究报道则很少。基于此,本文以4-(3-羟基-1-苯氧基丙基)-苯酚为α-O-4型木质素二聚体模型物 (图1),通过密度泛函理论方法,全面分析其热解反应机理以及产物形成途径,为深入了解木质素中α-O-4连接部分的热解机理提供依据。
1 计算方法本文中所有计算均采用Gaussian 09[15]程序完成。采用密度泛函理论中的M06-2X/6-31+ G (d,p) 方法,对裂解过程中的反应物、中间体、过渡态、产物进行几何结构的完全优化,再经过同一理论水平上的频率计算获得298.15 K下的标准热力学参数,并对热力学量考虑了零点振动能 (ZPE) 校正[16];在频率计算过程中,确保反应物、中间体以及产物没有虚频,确认过渡态有唯一虚频,并且用IRC计算来验证过渡态连接着正确的反应物和产物;在构建反应坐标图时,所用的能量均是气相吉布斯自由能,气相的标准状态是298.15 K和101.325 kPa。
|
| 图1 木质素二聚体模型化合物4-(3-羟基-1-苯氧基丙基)-苯酚 Fig.1 Lignin dimer model compound of 4-(3-hydroxy -1-phenoxypropyl)-phenol. |
下文讨论中所用的物理量是反应 (1) 的吉布斯自由能变。
\[A - B(g) \to A \cdot (g) + B \cdot (g)\]
(1)
对上述反应的键解离能计算公式[17]如下:
\[\begin{gathered}
{D_0}(A - B) \to E(A \cdot ) + {E_{ZP}}(A \cdot ) + E(B \cdot ) + {E_{ZP}}(B \cdot ) \\
- E(AB) - {E_{ZP}}(AB) \\
\end{gathered} \]
(2)
式中,D0表示考虑了零点能校正的键解离能,E为分子能量,EZP为零点能校正能量。
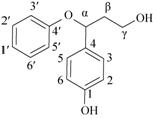
2 结果与讨论 2.1 α-O-4型木质素二聚体模型化合物的初次裂解目前,国内外学者对于β-O-4型木质素的初次裂解机理尚存在分歧,王华静等[8]和Beste等[10, 12]只考虑了以化学键均裂的木质素初次热解机理,Elder等[11]认为协同断裂比化学键均裂的活化能稍低,在初次裂解过程中更易发生。基于此,本文全面考虑了该α-O-4型木质素二聚体模型化合物6种化学键均裂和1种协同断裂的可能反应路径,其中6种化学键的均裂形式 及其对应的键解离能分别如图2及表1所示。D1路径是Cα-O键的均裂,D2路径是C4ʹ-O键的均裂,D3、D4路径分别是Cα-Cβ和Cβ-Cγ键的均裂,D5路径是C4-Cα键的均裂,D6路径是O-H键的均裂。
|
| 图2 木质素二聚体4-(3-羟基-1-苯氧基丙基)-苯酚化学键均裂形式 Fig.2 Homolytic cleavage ways of the lignin dimer. |
| Initial Decomposition mechanism | BDE | Initial Decomposition mechanism | BDE |
| D1 (Cα-O) | 193.4 | D4 (Cβ-Cγ) | 311.3 |
| D2 (C4`-O) | 375.2 | D5 (C4-Cα) | 360.7 |
| D3 (Cα-Cβ) | 269.7 | D6 (O-H) | 334.6 |
由表1可知,在6种均裂反应中,D1路径的键解离能最小,为193.4 kJ/mol,而其余5种路径的键解离能都较大,分布在270−375 kJ/mol之间,因此该模型化合物的化学键均裂形式以D1方式为主,即Cα-O键均裂。此外,在协同断裂反应中,Cβ位氢原子向醚键氧原子移动,同时Cα-O键断开,反应能垒为234.5 kJ/mol,因此也是热解反应初期较为容易发生的反应。总结上述7种反应路径,该模型化合物在初次热解过程中将主要以Cα-O键均裂及协同断裂的方式进行。
2.2 α-O-4型木质素二聚体模型化合物的后续裂解 2.2.1 基于Cα-O键均裂机理的后续裂解路径该木质素二聚体mc通过Cα-O键均裂生成自由基a和b,该步的能垒是193.4 kJ/mol,自由基a和b可能发生的后续反应以及相应的反应势能如图3所示。

|
| 图3 基于Cα-O键均裂的后续热解反应势能图 Fig.3 Subsequent pyrolysis pathways based on Cα-O homolysis of the lignin dimer. |
自由基a后续主要有5条可能的反应路径。在路径a-1中,自由基a的Cβ-Cγ键断裂,生成产物a-1-i1 (4-乙烯基苯酚) 和自由基·CH2OH,·CH2OH与氢自由基发生偶合反应生成甲醇,mc→a-1-i1的活化能为275.9 kJ/mol。在路径a-2中,自由基a的Cβ位失去一个氢,生成中间体a-2-i1,再经过四元环氢转移过渡态a-2-ts1,生成产物a-1-i1 (4-乙烯基苯酚)和甲醛,mc→a-2-ts1的活化能为681.2 kJ/mol。在路径a-3中,自由基a经过过渡态a-3-ts1,将Cβ位上的一个氢转移到了Cα上,生成自由基a-3-i1,接着经历Cγ位的脱羟基反应,得到产物a-3-i2 (4-烯丙基苯酚),mc→a-3-ts1的活化能为380.9 kJ/mol。自由基a-3-i1可以发生如路径a-3中的脱羟基反应,也可以发生C4-Cα键断裂反应,如路径a-4所示,并生成自由基a-4-i1和丙烯醇,自由基a-4-i1再进一步与氢自由基发生偶合反应得到产物b-1-i1 (苯酚),mc→a-3-ts1的活化能为380.9 kJ/mol。在路径a-5中,自由基a与氢自由基发生偶合反应得到中间体a-5-i1 (3-(4-羟基苯基)-1-丙醇),a-5-i1可经过Cα-Cβ键的均裂发生进一步的裂解反应,生成自由基a-5-i2和·CH2CH2OH,再与氢自由基发生偶合反应得到产物a-5-i3 (4-甲基苯酚) 和乙醇,a-5-i1→a-5-i2的活化能为272.2 kJ/mol。中间体a-5-i1的其他可能后续反应将在2.3节中讨论。根据上述各反应路径的活化能大小,可以判断这5条路径的反应活性顺序依次是路径a-5>a-1>a-3>a-4>a-2。因此,自由基a的主要裂解路径是a-5和a-1,相应的主要产物是4-甲基苯酚、4-乙烯基苯酚、甲醇和乙醇。
从自由基b出发的后续反应路径只有1条,即路径b-1,自由基b与氢自由基发生偶合反应得到产物b-1-i1 (苯酚),该路径的活化能为193.4 kJ/mol。从动力学的计算结果来看该路径很容易发生,相应的主要产物是苯酚。
由此可知,该木质素二聚体热解过程中,基于Cα-O键均裂的后续反应路径主要是路径a-5、a-1和b-1,主要产物是苯酚、4-甲基苯酚、4-乙烯基苯酚、甲醇和乙醇。
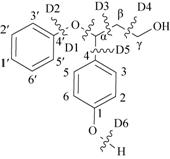
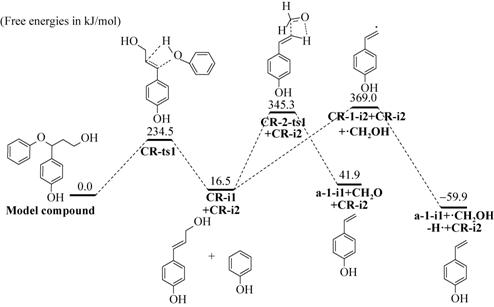
2.2.2 基于协同断裂机理的后续裂解路径如图4所示,在协同断裂机理中,木质素二聚体模型化合物的Cβ位氢原子向醚键氧原子移动,经过四元环过渡态CR-ts1,Cα-O键断开的同时,Cα-Cβ键长缩短并形成双键,得到产物CR-i1 (香豆醇) 和CR-i2 (苯酚)。其中,产物CR-i1可能进一步发生裂解反应,因此考虑了其可能发生的2条裂解路径 (路径CR-1和CR-2)。在路径CR-1中,CR-i1的Cβ-Cγ键均裂,得到自由基CR-1-i2和·CH2OH,再结合氢自由基生成产物a-1-i1 (4-乙烯基苯酚) 和甲醇,mc→CR-1-i2的活化能为369.0 kJ/mol。在路径CR-2中,CR-i1经过四元环氢转移过渡态CR-2-ts1,直接生成产物a-1-i1和甲醛,mc→CR-2-ts1的活化能为345.3 kJ/mol。综上,路径CR-1和CR-2的活化能都较高,因此CR-i1发生二次裂解反应的可能性很低,也就表明该木质素二聚体基于协同断裂机理最可能生成的产物是CR-i1 (香豆醇) 和CR-i2 (苯酚)。该结论与Amen-Chen等[18]的研究结果一致,在木质素热解过程中,木质素单体较为稳定,即使在高温下也很难进一步反应。
|
| 图4 基于协同断裂的后续热解反应势能图 Fig.4 Subsequent pyrolysis pathways based on the concerted decomposition of the lignin dimer. |
路径a-5的中间体3-(4-羟基苯基)-1-丙醇(a-5-i1) 是木质素3种单体结构 (香豆醇型、松柏醇型和芥子醇型) 中香豆醇型的一种[19],其进一步的裂解反应有多种可能的形式。通过全面考虑协同断裂、化学键均裂、分子内脱水及脱氢这四类反应,共分析了7条可能的后续反应路径,反应路径及反应势能如图5所示。

|
| 图5 3-(4-羟基苯基)-1-丙醇 (a-5-i1) 的裂解反应势能图 Fig.5 Pyrolysis pathways of 3-(4-hydroxyphenyl)-1-propanol. |
在路径a-5中,a-5-i1的Cα-Cβ键发生均裂反应,得到自由基a-5-i2和·CH2CH2OH,再与氢自由基发生偶合反应生成产物a-5-i3 (4-甲基苯酚) 和乙醇,该路径的活化能为272.2 kJ/mol;在路径a-6中,a-5-i1发生协同断裂反应,它经过氢转移过渡态a-6-ts1直接得到产物a-5-i3和乙烯醇,该路径的活化能为434.1 kJ/mol;比较路径a-5和a-6可知,路径a-5更容易发生,即a-5-i1的Cα-Cβ键更可能发生均裂而非协同断裂。在路径a-7中,a-5-i1的Cβ-Cγ键发生均裂反应,得到自由基a-7-i1和·CH2OH,再与氢自由基发生偶合反应生成产物a-7-i2 (4-乙基苯酚)和甲醇,该路径的活化能为305.9 kJ/mol;在路径a-8中,a-5-i1发生协同断裂反应,它经过氢转移过渡态a-8-ts1直接得到产物a-7-i2和甲醛,该路径的活化能为364.9 kJ/mol;比较路径a-7和a-8可知,路径a-7更容易发生,即a-5-i1的Cβ-Cγ键更可能发生均裂而非协同断裂;进一步与路径a-5相比可知,Cα-Cβ键比Cβ-Cγ键易发生均裂反应,a-5-i1进一步裂解更易得到产物4-甲基苯酚和乙醇,而非4-乙基苯酚和甲醇。在路径a-9中,a-5-i1失去2个氢原子,生成产物a-9-i1 (4-羟基苯丙醛),该路径的活化能为442.9 kJ/mol。在路径a-10中,a-5-i1经历四元环过渡态a-10-ts1,发生分子内脱水反应,生成产物a-3-i2 (4-烯丙基苯酚),该路径的活化能为278.0 kJ/mol。在路径a-11中,a-5-i1经历过渡态a-11-ts1,生成产物a-1-i1 (4-乙烯基苯酚) 和甲醇,该路径的活化能为445.2 kJ/mol。根据反应的活化能大小,可以判断这7条路径的反应活性顺序依次是路径a-5>a-10>a-7>a-8>a-6>a-9>a-11,因此该中间体最可能发生的路径是Cα-Cβ键均裂和分子内脱水反应,相应的主要产物是4-甲基苯酚、4-烯丙基苯酚、乙醇和水。
3 结论采用密度泛函理论M06-2X/6-31+G(d,p) 方法系统研究了α-O-4型木质素二聚体模型化合物的热解机理和主要产物。该α-O-4型木质素二聚体的初次裂解主要通过Cα-O键均裂和协同断裂进行;基于Cα-O键均裂的后续热解反应主要生成苯酚、4-甲基苯酚和4-乙烯基苯酚;而基于协同断裂的后续热解反应主要生成苯酚和香豆醇;除了酚类物质,热解过程还会生成乙醇、甲醇、甲醛等小分子物质;基于Cα-O键均裂而生成的3-(4-羟基苯基)-1-丙醇,进一步发生的热解反应主要以Cα-Cβ键均裂和分子内脱水反应为主。
| [1] | Zakzeski J, Bruijnincx PCA, Jongerius AL, et al. The catalytic valorization of lignin for the production of renewable chemicals. Chem Rev, 2010, 110(6): 3552-3599. |
| [2] | Huber GW, Iborra S, Corma A. Synthesis of transportation fuels from biomass: chemistry, catalysts, and engineering. Chem Rev, 2006, 106(9): 4044-4098. |
| [3] | Bridgwater AV, Peacocke GVC. Fast pyrolysis processes for biomass. Renew Sust Energ Rev, 2000, 4(1): 1-73. |
| [4] | Qi WY, Hu CW, Li GY, et al. Catalytic pyrolysis of several kinds of bamboos over zeolite Na Y. Green Chem, 2006, 8(2): 183-190. |
| [5] |
Huang JB, Wu D, Tong H, et al. Theoretical calculation of bond dissociation energies for β-O-4 linkage lignin dimer. Mater Rev, 2013, 27(22): 108-110 (in Chinese). 黄金保, 伍丹, 童红, 等. β-O-4型木质素二聚体中键离解能的理论计算. 材料导报, 2013, 27(22): 108-110. |
| [6] | Lora J, Glasser W. Recent industrial applications of lignin: a sustainable alternative to nonrenewable materials. J Polym Environ, 2002, 10(1/2): 39-48. |
| [7] |
Qu YS, Luo H, Li HQ, et al. Pretreatment of industrial lignin and catalytic conversion into phenol. Chin J Biotech, 2014, 30(5): 765-773 (in Chinese). 曲永水, 罗皓, 李宏强, 等. 工业木质素预处理及催化转化苯酚. 生物工程学报, 2014, 30(5): 765-773. |
| [8] |
Wang HJ, Zhao Y, Wang C, et al. Theoretical study on the pyrolysis process of lignin dimer model compounds. Acta Chim Sin, 2009, 67(9): 893-900 (in Chinese). 王华静, 赵岩, 王晨, 等. 木质素二聚体模型物裂解历程的理论研究. 化学学报, 2009, 67(9): 893-900. |
| [9] | Younker JM, Beste A, Buchanan AC. Computational study of bond dissociation enthalpies for substituted β-O-4 lignin model compounds. Chem Phys Chem, 2011, 12(18): 3556-3565. |
| [10] | Beste A, Buchanan AC. Computational study of bond dissociation enthalpies for lignin model compounds. Substituent effects in phenethyl phenyl ethers. J Org Chem, 2009, 74(7): 2837-2841. |
| [11] | Elder T, Beste A. Density functional theory study of the concerted pyrolysis mechanism for lignin models. Energ Fuel, 2014, 28(8): 5229-5235. |
| [12] | Beste A, Buchanan AC. Kinetic simulation of the thermal degradation of phenethyl phenyl ether, a model compound for the beta-O-4 linkage in lignin. Chem Phys Lett, 2012, 550: 19-24. |
| [13] | Kim KH, Bai X, Brown RC. Pyrolysis mechanisms of methoxy substituted α-O-4 lignin dimeric model compounds and detection of free radicals using electron paramagnetic resonance analysis. J Anal Appl Pyro, 2014, 110: 254-263. |
| [14] | Fingel D, Wegener G. Wood: chemistry, ultrastructure, reactions. Berlin: Walter de Gruyter, 1984: 26-65. |
| [15] | Frisch MJ, Trucks GW, Schlegel HB, et al. Gaussian 09, Revision D.01, Gaussian, Inc., Pittsburgh, PA, 2009. |
| [16] |
Huang JB, Liu C, Ren LR, et al. Studies on pyrolysis mechanism of syringol as lignin model compound by quantum chemistry. J Fuel Chem Technol, 2013, 41(6): 657-666 (in Chinese). 黄金保, 刘朝, 任丽蓉, 等. 木质素模化物紫丁香酚热解机理的量子化学研究. 燃料化学学报, 2013, 41(6): 657-666. |
| [17] |
Zhang FP, Cheng XL, Liu ZJ, et al. Density functional studies on the bond dissociation energy and pyrolysis mechanism of propyl nitrate. Chin J High Pressure Phys, 2005, 19(2): 189-192 (in Chinese). 张芳沛, 程新路, 刘子江, 等. 硝酸丙酯键离解能和热解机理的密度泛函理论研究. 高压物理学报, 2005, 19(2): 189-192. |
| [18] | Amen-Chen C, Pakdel H, Roy C. Production of monomeric phenols by thermochemical conversion of biomass: a review. Bioresour Technol, 2001, 79(3): 277-299. |
| [19] | Chakar FS, Ragauskas AJ. Review of current and future softwood kraft lignin process chemistry. Ind Crop Prod, 2004, 20(2): 131-141. |
 2015, Vol. 31
2015, Vol. 31